Vaikuttavat aineet: Centella asiatican triterpeenifraktio
Centellase 30 mg tabletit
Miksi Centellasea käytetään? Mitä varten se on?
Centellase on lääke, joka perustuu Centella asiaticaan, joka on lääke suonien suojaamiseen.
Centellase on tarkoitettu seuraavien hoitoon:
- laskimoiden vajaatoiminnasta johtuva nilkkojen ja jalkojen turvotus, jalkojen raskauden tunne, pistely ja kutina jaloissa, öiset jalkakrampit ja näkyvät hiussuonet;
- kapillaarien hauraus.
Keskustele lääkärisi kanssa, jos et voi paremmin tai tunnet olosi huonommaksi.
Vasta -aiheet Milloin Centellasea ei tule käyttää
Älä ota Centellasea
- jos olet allerginen vaikuttavalle aineelle tai tämän lääkkeen jollekin muulle aineelle
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Centellasea
Tämän lääkkeen käyttöön ei ole erityisiä varotoimia.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Centellase -valmisteen vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Varoitukset On tärkeää tietää, että:
Raskaus, imetys ja hedelmällisyys
Älä käytä tätä lääkettä raskauden ja imetyksen aikana, koska sen vaikutuksia ei tunneta.
jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Centellase ei vaikuta ajokykyyn tai koneiden käyttökykyyn.
Annos, antotapa ja antotapa Centellase -valmisteen käyttö: Annostus
Käytä tätä lääkettä aina tässä pakkausselosteessa kuvatulla tavalla tai lääkärin tai apteekkihenkilökunnan ohjeiden mukaan. Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Suositeltu annos on 1-2 tablettia päivässä mieluiten aterioiden yhteydessä.
Käyttö: Tabletit niellään kokonaisina veden kanssa
Hoidon kesto: Käytä tätä lääkettä vain lyhyitä hoitojaksoja. Ota yhteys lääkäriisi, jos häiriö ilmenee toistuvasti tai jos olet havainnut äskettäisiä muutoksia sen ominaisuuksissa.
Sivuvaikutukset Mitkä ovat Centellasen sivuvaikutukset?
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Lääkkeen käyttö voi aiheuttaa kutinaa tai aiheuttaa herkkyyttä auringonvalolle ja UV -säteille (valoherkistyminen) punoituksen ja punaisten ja / tai turvonnut (ihottumat).
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan verkkosivuston kautta: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkkeen turvallisuudesta.
Vanhentuminen ja säilyttäminen
Tämä lääke ei vaadi erityisiä säilytysolosuhteita.
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän "EXP" jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Mitä Centellase sisältää
- Vaikuttava aine on: Centella asiatican triterpeenifraktio
- Muut aineet ovat: kaksiemäksinen kalsiumfosfaattidihydraatti, dokusaattinatrium, povidoni, kroskarmelloosinatrium, karmelloosinatrium, magnesiumstearaatti.
Lääkevalmisteen kuvaus ja pakkaus
Centellase on pahvilaatikossa, joka sisältää 30 tablettia läpipainopakkauksissa.
Lähdepakkaus: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
CENTELLASE TABLETIT
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
1 tabletti sisältää: gotu kolan triterpeenifraktion kokonaisfraktio (asiaticoside 40% - aasialainen happo + madecassic acid 60%) 30 mg.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Tabletit.
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Laskimon vajaatoimintaan liittyvät oireet; kapillaarien haurauden tilat.
04.2 Annostus ja antotapa
Annostus
1-2 tablettia päivässä, mieluiten aterian yhteydessä.
Lääkettä tulee käyttää vain lyhyen ajan.
Antotapa: suun kautta.
04.3 Vasta -aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Ei erityisiä varotoimia tuotteen käytössä.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Yhteisvaikutuksia muiden lääkkeiden kanssa ei tunneta.
04.6 Raskaus ja imetys
Eläinkokeet eivät ole osoittaneet lisääntymistoksisuutta. Ei ole olemassa riittävästi tietoa lääkkeen käytöstä raskaana oleville tai imettäville naisille. Centellasea ei tule käyttää raskauden ja imetyksen aikana.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Centellase ei vaikuta ajokykyyn tai koneiden käyttökykyyn.
04.8 Haittavaikutukset
Kutinaa ja valoherkkyysreaktioita, joihin liittyy punoitusta ja ihottumaa, on raportoitu lääkkeen oraalisen annon jälkeen.
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeää, koska sen avulla voidaan jatkuvasti seurata lääkkeen hyöty -haitta -tasapainoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta. "Osoite: http : //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Yliannostus
Yliannostustapauksia ei ole raportoitu.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: vasoprotektorit.
ATC -koodi: C05CX.
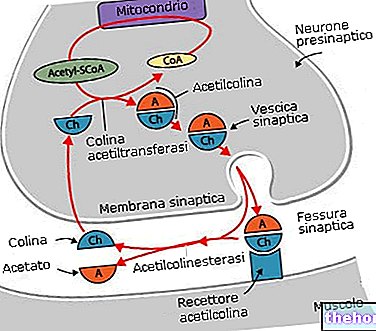
Toimintamekanismi
Centella asiatican (FTTCA) triterpeenifraktiolla on moduloivia ominaisuuksia sidekudoksen kehittymiselle, mikä parantaa laskimoiden seinämän sävyä ja kimmoisuutta.Tämä mahdollistaa endoteelin läpäisevyyden vähenemisen kapillaaritaso), jotta ajan myötä palautetaan hemodynaaminen tasapaino kudoksen mikroverisuonijärjestelmän tasolla, jonka muutos aiheuttaa suonikohjujen oireyhtymän oireita.
05.2 Farmakokineettiset ominaisuudet
Imeytyminen
Oraalisen annon jälkeen FTTCA imeytyy nopeasti ja saavuttaa huippupitoisuuden noin 4 tunnissa. Epikutaanisen annon jälkeen valmiste näyttää veren piikin 6. ja 12. tunnin välillä.
Biotransformaatio ja eliminaatio
Vaikuttavat aineet eivät metaboloidu elimistössä ja eliminoituvat sellaisina ulosteen kautta.
Entero-maksan verenkierto on osoitettu.
05.3 Prekliiniset tiedot turvallisuudesta
Ei ole prekliinisten tietojen perusteella lääkärille merkittävää tietoa, jota ei ole jo raportoitu valmisteyhteenvedon muissa osissa.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Kaksiemäksinen kalsiumfosfaattidihydraatti, dokusaattinatrium, povidoni, kroskarmelloosinatrium, karmelloosinatrium, magnesiumstearaatti.
06.2 Yhteensopimattomuus
Ei oleellinen.
06.3 Voimassaoloaika
5 vuotta.
06.4 Säilytys
Tämä lääke ei vaadi erityisiä säilytysolosuhteita.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Tabletit on pakattu muovimateriaaliin, joka on kuumasaumattu alumiinilla (läpipainopakkaus) ja sijoitettu pahvilaatikkoon pakkausselosteen kanssa.
30 tabletin laatikko.
06.6 Käyttö- ja käsittelyohjeet
Ei erityisiä hävitysohjeita.
07.0 MYYNTILUVAN HALTIJA
Farmaseuttinen laboratorio SIT S.r.l. - Via Cavour, 70-27035 Mede (PV)
08.0 MYYNTILUVAN NUMERO
AIC: 016222073
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Myyntiluvan myöntämisen päivämäärä: marraskuu 1982.
Viimeisimmän uudistamisen päivämäärä: toukokuu 2010.
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
AIFA: n päätös 21. heinäkuuta 2014.