Vaikuttavat aineet: Budesonidi
Budexan 0,25 mg / ml suspensio sumutusta varten
Budexan 0,5 mg / ml suspensio sumutusta varten
Miksi Budexania käytetään? Mitä varten se on?
Budexan sisältää vaikuttavana aineena budesonidia.
Budexan kuuluu lääkeryhmään, jota kutsutaan glukokortikosteroideiksi.
Budexan on tarkoitettu seuraavien sairauksien hoitoon:
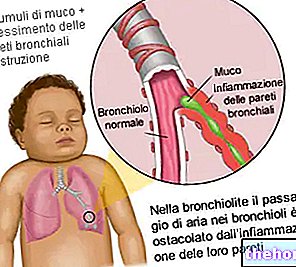
- tulehduksellinen sairaus, jolle on tunnusomaista keuhkoputkien tukkeutuminen (keuhkoastma);
- sairaus, jolle on tunnusomaista kurkun (kurkunpään) tukos, joka vaikeuttaa ilman kulkua ja jonka hoitoon tarvitaan sairaalahoitoa (erittäin vaikea subglottinen kurkunpään tulehdus (pseudoryhmä)).
Vasta -aiheet Milloin Budexania ei tule käyttää
Älä ota Budexania, jos olet allerginen vaikuttavalle aineelle tai tämän lääkkeen jollekin muulle aineelle.
Käyttöön liittyvät varotoimet Mitä sinun on tiedettävä, ennen kuin otat Budexania
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Budexania, jos:
- sinulla on heikentynyt maksan toiminta;
- käytät samanaikaisesti ketokonatsolia (sienisairauksien lääke) tai HIV -proteaasin estäjiä (aidsin lääkkeitä) tai muita sytokromi CYP3A4: n (eniten entsyymi lääkkeiden hajoamiseen osallistuvia) estäjiä;
- sinulla on aktiivinen tai lepotilassa oleva keuhkotuberkuloosi tai sinulla on sieni- tai virusinfektio hengitysteissä;
- sinulla on sieni- ja virusinfektioita (tuhkarokko ja vesirokko)
- on glaukooma (jolle on tunnusomaista krooninen vaurio silmän hermolle) ja kaihi (silmän osan läpinäkyvyyden menetys linssi).
Budexan ei paranna nopeasti äkillisiä (akuutteja) astmajaksoja, joihin on käytettävä muita lääkkeitä, kuten lyhytvaikutteisia keuhkoputkia laajentavia aineita.
Lääkärisi on arvioitava huolellisesti, ettet ole hyötynyt lyhytvaikutteisten keuhkoputkia laajentavien lääkkeiden käytöstä, jolloin hän voi päättää lisätä budesonidi-inhalaatioiden määrää tavalliseen verrattuna tai aloittaa suun kautta otettavien glukokortikosteroidien käytön.
Näissä kahdessa tapauksessa lääkärin on arvioitava lisämunuaisen kutsuman rauhasen mahdolliset vaarat ja / tai vajaatoiminta.
Lääkärin on arvioitava huolellisesti suspensio suun kautta otettavista glukokortikosteroideista, koska harvinaisissa tapauksissa voi esiintyä yleistä huonovointisuutta, kuten lihas- ja nivelkipuja, väsymystä, päänsärkyä (päänsärkyä), masennusta, pahoinvointia ja oksentelua, vaikka keuhkojen toiminta saattaa parantua.
Hoidon korvaaminen glukokortikosteroideilla, jotka jakautuvat koko kehoon (systeeminen) inhalaatiohoidolla, voi joskus johtaa allergioihin, kuten nenän tulehdukseen (nuha) ja ihoon (ekseema).
Inhaloitavan hoidon aikana voi kehittyä sienitauti, jota kutsutaan suun kandidiaasiksi. Tämä infektio saattaa vaatia asianmukaista sienilääkitystä ja joissakin tapauksissa hoito on ehkä lopetettava (ks. Kohta "Miten Budexania otetaan").
Pitkäaikaisessa hoidossa paikallisia ja koko kehon vaikutuksia voi esiintyä suurilla Budexan-annoksilla (Cushingin oireyhtymä, Cushingoid-näkökulma, lisämunuaisen vajaatoiminta, luun mineraalitiheyden väheneminen, kaihi, glaukooma, harvoin psykologiset ja käyttäytymisvaikutukset, mukaan lukien hyperaktiivisuus, psykomotorinen toiminta, unihäiriöt, ahdistuneisuus, masennus, aggressio, käyttäytymishäiriöt).
Kun astma on saatu hallintaan, lääkäri määrää pienimmän tehokkaan ylläpitoannoksen.Älä suurenna tai pienennä annostasi keskustelematta ensin lääkärisi kanssa.
Samoin kuin muilla inhalaatiolla annettavilla hoidoilla, siihen voi liittyä keuhkoputkien supistuminen (paradoksaalinen bronkospasmi), ja hengitysvaikeudet (hengityksen vinkuminen) lisääntyvät välittömästi annon jälkeen. Tässä tapauksessa sinun on välittömästi lopetettava inhaloitavan budesonidin käyttö ja lääkäri arvioi tilanteen ja tarvittaessa vaihtoehtoisen hoidon.
Lapset ja nuoret
Budexania tulee käyttää varoen lapsilla.
Vaikutus kasvuun
Pituus on tarkistettava säännöllisesti, jos lapsi saa pitkäaikaista inhaloitavaa glukokortikosteroidihoitoa. Jos kasvu hidastuu, lääkäri harkitsee lääkkeen annoksen pienentämistä. Hoidon hyödyt ja mahdollinen kasvun hidastumisriski on tehtävä huolellisesti. arvioi lääkäri, joka voi lähettää lapsen lasten keuhkosairaalaan.
Käyttäytymishäiriöitä voi esiintyä pitkäaikaisessa Budexan-annoksessa.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Budexanin vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Budesonidin yhteisvaikutuksia muiden astman hoitoon käytettävien lääkevalmisteiden kanssa ei ole havaittu.
Sinun on vältettävä lääkkeen ottamista samanaikaisesti tai annettava mahdollisimman pitkä aika hoitojen välillä, jos sinun on otettava:
- ketokonatsoli ja itrakonatsoli, sienitautien hoitoon käytettävät lääkkeet, koska ne voivat lisätä budesonidin määrää elimistössäsi (ks. kohta "Varoitukset ja varotoimet") .Lääkärisi voi myös harkita Budexan -annoksen pienentämistä.
Budexan häiritsee:
- ehkäisypillereissä käytettäviä estrogeeneja ja hormoneja, koska näissä tapauksissa budesonidin määrä veressä kasvaa ja siitä seuraa vaikutuksia elimistöön.
Budexan voi muuttaa joidenkin laboratoriokokeiden tuloksia, joita käytetään diagnosoimaan "aivolisäkkeen nimeltä tulevan rauhan vajaatoiminta (ACTH -stimulaatiotesti aivolisäkkeen vajaatoiminnan diagnosoimiseksi voi antaa vääriä tuloksia alhaisten arvojen havaitsemiseksi).
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Raskaus
Inhaloidulla budesonidilla ei havaittu haitallisia terveysvaikutuksia sikiölle / vastasyntyneelle raskauden aikana. Raskauden aikana lääkäri arvioi sinulle odotetut hyödyt ja sikiöön kohdistuvat riskit.
Ruokinta-aika
Budesonidi voi erittyä rintamaitoon. Budexanin terapeuttisilla annoksilla ei odoteta olevan vaikutuksia imettävään lapseen. Budesonidia voidaan käyttää imetyksen aikana.
Ajaminen ja koneiden käyttö
Budexan ei vaikuta ajokykyyn ja koneiden käyttökykyyn.
Annostus ja käyttötapa Budexanin käyttö: Annostus
Ota tätä lääkettä juuri siten kuin lääkäri tai apteekki on määrännyt.
Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Keuhkoastma
Aikuiset ja vanhukset
Aloitusannos:
Budexan -annos on yksilöllinen.
Suositeltu aloitusannos on 0,5-1 mg kahdesti vuorokaudessa.
Tapauksissa, joissa tarvitaan suurempaa terapeuttista vaikutusta, voidaan määrätä suurempia Budexan -annoksia.
Ylläpitoannos:
Ylläpitoannos on yksilöllinen.
Kun halutut kliiniset tulokset on saavutettu, lääkäri pienentää annosta, kunnes oireiden hallintaan tarvittava vähimmäismäärä on saavutettu.
Vaikutuksen alku
Astman hallintaa voidaan parantaa Budexan -hoidon jälkeen 3 päivän kuluessa hoidon aloittamisesta, vaikka suurin hyöty saavutetaan 2–4 viikon kuluttua.
Potilaat, joita hoidetaan suun kautta otettavilla glukokortikosteroideilla (ks. Kohta "Varoitukset ja varotoimet")
Budexan saattaa korvata suun kautta otettavan glukokortikosteroidiannoksen tai vähentää sitä merkittävästi säilyttäen astman hallinnan.
Lääkärisi harkitsee, miten suun kautta otettavasta glukokortikosteroidihoidosta siirrytään Budexan -sumutinsuspensiohoitoon.
Annoksen jakaminen ja sekoittaminen
Lääkärisi voi pyytää sinua sekoittamaan Budexanin 0,9% suolaliuokseen ja muihin liuoksiin, jotka sisältävät hengitykseen vaikuttavia lääkkeitä, kuten terbutaliinia, salbutamolia, fenoterolia, asetyylikysteiiniä, natriumkromoglykaattia tai ipratropriumbromidia.
Seos tulee käyttää 30 minuutin kuluessa.
Kerta-annospakkauksen sisältö voidaan jakaa annoksen säätämiseksi.
Viiva näkyy selvästi Budexanin kerta-annospakkauksissa.
Kun kerta-annospakkausta pidetään ylösalaisin, viiva osoittaa 1 ml: n tilavuuden.
Jos käytetään vain 1 ml, tyhjennä kerta-annospakkauksen sisältö, kunnes nesteen pinta saavuttaa ilmoitetun viivan.
Ennen jäljellä olevan nesteen käyttöä ravista sisältöä varovasti kiertävällä liikkeellä.
ANNOSTUSTAULUKKO
* Lääkevalmiste on sekoitettava 0,9%: n fysiologiseen liuokseen 2 ml: n tilavuuden saavuttamiseksi.
Käyttö lapsille ja nuorille
Keuhkoastma
6 kuukauden ikäiset ja yli 12 -vuotiaat lapset
Suositeltu kokonaisannos on 0,25-0,5 mg.
Jos saat lapsen suun kautta otettavaa glukokortikosteroidihoitoa, lääkäri voi päättää aloittaa suuremmalla aloitusannoksella, esimerkiksi 1 mg.
Lääkäri harkitsee suurempaa annosta (2 mg vuorokaudessa) vain vaikeaa astmaa sairastavilla lapsilla ja rajoitetun ajan.
Subglottinen kurkunpään tulehdus (kurkun tukos)
Suositeltu annos on 2 mg Budexania, joka voidaan antaa kerta -annoksena tai kahtena 1 mg: n annoksena 30 minuutin välein.
Annostus voidaan toistaa 12 tunnin välein enintään 36 tunnin ajan tai kunnes kliininen paraneminen.
Lapsille suosittelemme käyttämään täysin tiukkaa ja hyvin istuvaa kasvonaamaria, joka pystyy optimoimaan annetun budesonidiannoksen.
BUDEXANIN OIKEAN KÄYTÖN OHJEET
Huomautus:
Sumutusaika ja sumutinlaitteen antama lääkemäärä riippuvat kompressorin virtausnopeudesta ja täyttötilavuudesta.
Budesonidin pienen määrän vuoksi ultraäänisumuttimia ei tule käyttää Budexanin antamiseen.
Ravista injektiopulloa varovasti kiertävällä liikkeellä.
Pidä kerta-annospakkausta pystyasennossa ja avaa kääntämällä luukkua, kunnes säiliö avautuu.
Aseta kerta-annospakkauksen avoin pää hyvin sumuttimen säiliöön ja paina hitaasti.
Huuhtele suu vedellä jokaisen annon jälkeen sieni -infektioiden (suun ja nielun sammas) esiintymisen vähentämiseksi. Jos käytetään kasvonaamaria, on varmistettava, että maski tarttuu hyvin ruiskutuksen aikana. Kasvomaskin käytön jälkeen pese kasvosi vedellä ärsytyksen estämiseksi.
Puhdistus:
Sumutinkammio on puhdistettava jokaisen annon jälkeen. Pese sumutinkammio ja suukappale tai kasvonaamio lämpimällä vesijohtovedellä miedolla pesuaineella tai noudata valmistajan ohjeita. Huuhtele hyvin ja kuivaa kammio yhdistämällä kompressori ja inhalaattori.
Jos unohdat ottaa Budexania
Älä ota kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos lopetat Budexanin käytön
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Budexania
Akuutti Budexan -yliannostus ei edes suurina annoksina saisi aiheuttaa kliinisiä ongelmia. Jos otat vahingossa Budexan -yliannoksen, ilmoita siitä heti lääkärille tai mene lähimpään sairaalaan.
Sivuvaikutukset Mitkä ovat Budexanin sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Seuraavia haittavaikutuksia on havaittu:
Yleinen (voi esiintyä useammalla kuin yhdellä henkilöllä 100: sta)
- sieni -infektiot suussa ja kurkussa (Candida nielussa);
- pahoinvointi;
- yskä, käheys, kurkun ärsytys.
Harvinaiset (voi esiintyä enintään 1 käyttäjällä 1000: sta)
- välittömät tai viivästyneet yliherkkyysreaktiot, mukaan lukien ihottuma, jossa on märkärakkuloita, rakkuloita ja rakkuloita (ihottuma), ihon tulehdus tiettyjen aineiden kanssa (kosketusihottuma), äkillinen enemmän tai vähemmän kutiava ihottuma (nokkosihottuma), nopea ihon turvotus ja limakalvot (angioedeema) ja vaikea ja äkillinen allerginen reaktio (anafylaktinen reaktio);
- lisämunuaisen toiminnan estäminen;
- levottomuus, hermostuneisuus, masennus, käyttäytymismuutokset, unihäiriöt, ahdistuneisuus, psykomotorinen yliaktiivisuus, aggressio;
- mustelmia, ihon raitoja.
Tuntematon (koska saatavissa oleva tieto ei riitä arviointiin)
- krooninen silmähermon vaurio (glaukooma), silmän osan läpinäkyvyyden heikkeneminen (kaihi).
Tuntemattomien mekanismien vuoksi inhaloitavat lääkevalmisteet voivat harvoin aiheuttaa bronkospasmia.
Ärsytyksen estämiseksi kasvojen iho on pestävä vedellä kasvonaamion käytön jälkeen.
Pakkausselosteen ohjeiden noudattaminen vähentää haittavaikutusten riskiä.
Muita haittavaikutuksia lapsilla ja nuorilla
Harvinaiset (voi esiintyä enintään 1 käyttäjällä 1000: sta)
- kasvun hidastuminen;
- psykomotorinen yliaktiivisuus, aggressio;
- bronkospasmi ja äänihäiriöt (dysfonia ja käheys).
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. Yhteystiedot alla) kansallisen ilmoitusjärjestelmän kautta osoitteessa www.agenziafarmaco.
Vanhentuminen ja säilyttäminen
Säilytä alle 25 ° C.
Säilytä alkuperäispakkauksessa suojataksesi lääkettä valolta.
Alumiinipussin avaamisen jälkeen kerta-annospakkaukset on käytettävä 3 kuukauden kuluessa ja tämän ajan jälkeen jäljellä oleva tuote on hävitettävä.
Kalvopussin avaamisen jälkeen käyttämättömät kerta-annospakkaukset on säilytettävä pussissa valolta suojattuna.
Avattu kerta-annospakkaus on käytettävä 12 tunnin kuluessa. Tämän ajan jälkeen tuotejäämät on poistettava.
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän "Käyt. Viim." Jälkeen.
Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Muita tietoja
Mitä Budexan sisältää
Budexan 0,25 mg / ml suspensio sumutusta varten
- Vaikuttava aine on budesonidi. Yksi kerta-annospakkaus sisältää 0,5 mg budesonidia.
- Muut aineet ovat dinatriumedetaatti, natriumkloridi, polysorbaatti 80, vedetön sitruunahappo, natriumsitraatti, injektionesteisiin käytettävä vesi.
Budexan 0,5 mg / ml suspensio sumutusta varten
- Vaikuttava aine on budesonidi. Yksi kerta-annospakkaus sisältää 1 mg budesonidia.
- Muut aineet ovat dinatriumedetaatti, natriumkloridi, polysorbaatti 80, vedetön sitruunahappo, natriumsitraatti, injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkaus
Suspensio ruiskutetaan.
Jokainen pakkaus sisältää 20 kerta-annospakkausta, jotka on jaettu 5 yksikön liuskoihin alumiinipussissa.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
BUDEXAN -JOUSITUS NEBULISOIDAAN
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
1 kerta-annospakkaus sisältää:
vaikuttava aine: budesonidi 0,5 mg
BUDEXAN 0,5 mg / ml suspensio sumutusta varten
1 kerta-annospakkaus sisältää:
vaikuttava aine: budesonidi 1 mg
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Suspensio ruiskutetaan
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
BUDEXAN -sumutinsuspensio on tarkoitettu keuhkoastman hoitoon.
BUDEXAN -sumutinsuspensio on tarkoitettu myös erittäin vaikean subglottisen kurkunpään (pseudoryhmän) hoitoon, jos sairaalahoito on tarpeen.
04.2 Annostus ja antotapa
Keuhkoastma:
Aloitusannos:
Sumutettavan BUDEXAN -suspension suspensio on yksilöllinen.
Aloitusannoksen tulee olla:
6 kuukauden ikäiset ja sitä vanhemmat ja enintään 12 -vuotiaat lapset:
Päivittäinen kokonaisannos 0,25-0,5 mg. Oraalista steroidihoitoa saavilla potilailla on mahdollista aloittaa suuremmalla aloitusannoksella, esimerkiksi 1 mg. Suurempaa annosta (2 mg vuorokaudessa) tulee harkita vain vaikeaa astmaa sairastavilla lapsilla ja vain rajoitetun ajan.
Aikuiset ja vanhukset:
0,5-1 mg kahdesti päivässä. Tarvittaessa annosta voidaan nostaa edelleen.
Tapauksissa, joissa tarvitaan suurempaa terapeuttista vaikutusta, on mahdollista antaa suurempia sumutettavia BUDEXAN -suspensiota; itse asiassa systeemisten vaikutusten riskit ovat pienet verrattuna niihin, jotka voidaan todeta hoidon yhteydessä suun kautta otettavien glukokortikosteroidien kanssa.
Ylläpitoannos:
Ylläpitoannos on yksilöllinen.
Kun halutut kliiniset tulokset on saavutettu, ylläpitoannosta on pienennettävä vähitellen, kunnes oireiden hallintaan tarvittava vähimmäismäärä on saavutettu.
Vaikutuksen alku:
Astman hallinta voi parantua inhaloitavan BUDEXAN-sumutinsuspension jälkeen 3 päivän kuluessa hoidon aloittamisesta, vaikka suurin hyöty saavutetaan 2-4 viikon kuluttua.
Suun kautta otettavilla steroideilla hoidetut potilaat (ks. Myös 4.4):
BUDEXAN -sumutinsuspensio voi mahdollistaa steroidiannoksen korvaamisen tai pienentämisen merkittävästi säilyttäen astman hallinnan.
Kun potilaan on siirryttävä suun kautta otettavasta kortikosteroidihoidosta BUDEXAN -sumutinsuspensioon, sen on oltava suhteellisen vakaassa vaiheessa. Suuri annos sumutettavaa BUDEXAN -suspensiota. sitä annetaan sitten yhdessä aiemmin käytetyn oraalisen annoksen kanssa noin 10 päivän ajan.
Sen jälkeen suun kautta otettavaa steroidiannosta on pienennettävä vähitellen (esim. 2,5 milligrammasta prednisolonia tai vastaavaa kuukausittain) pienimmälle mahdolliselle tasolle. Monissa tapauksissa suun kautta otettava steroidi voidaan korvata kokonaan BUDEXAN -sumutin suspensiolla.
Annoksen jakaminen ja sekoittaminen:
BUDEXAN -sumutinsuspensio voidaan sekoittaa 0,9% suolaliuokseen ja terbutaliinin, salbutamolin, fenoterolin, asetyylikysteiinin, natriumkromoglykaatin tai ipratropriumbromidin sumutusliuoksiin.
Seos tulee käyttää 30 minuutin kuluessa.
Kerta-annospakkauksen sisältö voidaan jakaa annoksen säätämiseksi.
Suihkutettavan BUDEXAN-suspension kerta-annospakkauksissa on selvästi näkyvissä viiva. Kun kerta-annospakkausta pidetään ylösalaisin, viiva osoittaa 1 ml: n tilavuuden. Jos käytetään vain 1 ml, tyhjennä kerta-annospakkauksen sisältö, kunnes nesteen pinta saavuttaa ilmoitetun viivan.
Ennen jäljellä olevan nesteen käyttöä ravista sisältöä varovasti kiertävällä liikkeellä.
ANNOSTUSTAULUKKO
* Tuote on sekoitettava 0,9%: n fysiologiseen liuokseen 2 ml: n tilavuuden saavuttamiseksi.
Subglottinen kurkunpään tulehdus
Imeväisillä ja lapsilla, joilla on subglottinen kurkunpään tulehdus, tavallinen annos on 2 mg BUDEXAN -sumutinpuskuria, joka voidaan antaa kerta -annoksena tai kahtena 1 mg: n annoksena 30 minuutin välein. Annos voidaan toistaa 30 minuutin välein. 12 tuntia enintään 36 tuntia tai kunnes kliininen paraneminen.
OHJEET BUDEXAN -JOUSITUKSEN OIKEAAN KÄYTTÖÖN NEBULIZOITAAN
Ravista kerta-annospakkausta varovasti kiertävällä liikkeellä.
Pidä kerta-annospakkausta pystyasennossa ja avaa kääntämällä luukkua, kunnes säiliö avautuu.
Aseta kerta-annospakkauksen avoin pää hyvin sumuttimen säiliöön ja paina hitaasti.
Huomautus:
Huuhtele suu vedellä jokaisen annon jälkeen suun ja nielun sammasta.
Jos käytetään kasvonaamaria, on varmistettava, että maski tarttuu hyvin ruiskutuksen aikana. Kasvomaskin käytön jälkeen pese kasvosi vedellä ärsytyksen estämiseksi.
Puhdistus:
Sumutinkammio on puhdistettava jokaisen annon jälkeen. Pese sumutinkammio ja suukappale tai kasvonaamio lämpimällä vesijohtovedellä miedolla pesuaineella tai noudata valmistajan ohjeita. Huuhtele hyvin ja kuivaa kammio yhdistämällä kompressori ja inhalaattori.
Sumutusaika ja sumutinlaitteen antama lääkeaine määrä riippuvat kompressorin virtausnopeudesta ja täyttötilavuudesta.
In vitro sumutinlaitteen antama budesonidin määrä vaihtelee välillä 30-70% nimellisannoksesta riippuen sumuttimen ja kompressorin tyypistä, eivätkä kaikki sumuttimet ja kompressorit ole sopivia sumutettavan BUDEXAN-suspension käyttöön.
Budesonidin suurimman annostelun saavuttamiseksi tarvitaan kompressori, joka takaa virtauksen 5-8 litraa / min ja täyttötilavuuden 2-4 ml.
In vivo tehdyt tutkimukset ovat osoittaneet, että potilaille annettava sumutetun budesonidin annos vaihtelee 11--22% nimellisannoksesta.
Lapsille suosittelemme käyttämään täysin tiukkaa ja hyvin istuvaa kasvonaamaria, joka pystyy optimoimaan annetun budesonidiannoksen.
Pienen budesonidimäärän vuoksi BUDEXAN -sumutinsuspensiota ei saa käyttää ultraäänisumuttimilla.
04.3 Vasta -aiheet
Yliherkkyys budesonidille tai apuaineille.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
BUDEXAN-sumutinsuspensiota ei ole tarkoitettu äkillisten astmanvaiheiden nopeaan parantamiseen, jos niitä tarvitaan lyhytvaikutteiseen bronkodilataattoriin. Lääkärin on arvioitava huolellisesti tapaukset potilaista, jotka eivät hyöty lyhytvaikutteisten keuhkoputkien laajentimien käytöstä tai jotka lisäävät inhalaatioiden määrää tavanomaiseen verrattuna. Näissä tapauksissa lääkärin on arvioitava tulehduskipulääkkeiden tehostamisen tarve, esimerkiksi lisäämällä inhaloitavan budesonidin annosta tai aloittamalla suun kautta otettava glukokortikosteroidihoito.
Erityistä huomiota on kiinnitettävä potilaiden siirtämiseen suun kautta otettavasta steroidihoidosta, koska lisämunuaisen vaaran riski voi säilyä pitkään. Potilaat, jotka ovat tarvinneet hätähoitoa suurilla kortikosteroidiannoksilla tai pitkäaikaista hoitoa suurilla annoksilla inhaloitavia kortikosteroideja, voivat myös olla vaarassa. Tällaisilla potilailla voi esiintyä lisämunuaisen vajaatoiminnan merkkejä ja oireita altistuessaan vakavalle stressille. Stressinaikoina tai elektiivisen leikkauksen yhteydessä on harkittava lisäsuojaa systeemisellä kortikosteroidilla. Systeemisen glukokortikosteroidihoidon vaimennusvaiheen aikana joillakin potilailla voi esiintyä yleistä huonovointisuutta, kuten lihas- ja nivelkipuja. Yleistä glukokortikosteroidien vajaatoimintaa tulee epäillä harvinaisissa tapauksissa, kun oireet, kuten väsymys, päänsärky, pahoinvointi ja oksentelu, alkavat. Näissä tapauksissa suun kautta otettavan glukokortikosteroidiannoksen väliaikainen lisääminen voi joskus olla tarpeen.
Joillakin potilailla saattaa esiintyä systeemisen glukokortikosteroidien suppression oireita, kuten nivel- ja / tai lihaskipua, väsymystä ja masennusta huolimatta siitä, että keuhkojen toiminta säilyy tai jopa paranee suun kautta otettavan steroidihoidon aikana. Tällaisia potilaita tulee rohkaista jatkamaan BUDEXAN -sumutinsuspensiohoitoa, mutta heitä on seurattava lisämunuaisen vajaatoiminnan objektiivisten oireiden varalta. Jos on todisteita lisämunuaisen vajaatoiminnasta, systeemisen kortikosteroidiannosta on tilapäisesti lisättävä ja siirtymistä BUDEXAN -sumutinsuspensioon voidaan jatkaa myöhemmin, hitaammin. Stressin aikana tai vaikean astmakohtauksen aikana potilaat, jotka korvaavat systeemisen steroidihoidon inhalaatiohoidolla, saattavat tarvita lisää systeemistä kortikosteroidihoitoa.
Systeemisen steroidihoidon korvaaminen inhalaatiohoidolla voi joskus ilmetä allergioita, kuten nuhaa ja ihottumaa, joita aiemmin hallittiin systeemisellä steroidihoidolla. Näitä allergisia ilmenemismuotoja tulee hallita oireenmukaisesti antihistamiinilääkkeillä ja / tai paikallisilla valmisteilla.
Maksan vajaatoiminta vaikuttaa glukokortikosteroidien eliminaatioon, mikä johtaa hidastuvaan eliminaatioon ja suurempaan systeemiseen altistukseen.Tämä voi olla kliinisesti tärkeää potilaille, joilla on vaikea maksan vajaatoiminta.
On välttämätöntä olla tietoinen mahdollisista systeemisistä sivuvaikutuksista.
Ketokonatsolin, HIV -proteaasin estäjien tai muiden voimakkaiden CYP3A4 -estäjien samanaikaista käyttöä tulee välttää. Jos tämä ei ole mahdollista, kahden hoidon välisen ajan tulee olla mahdollisimman pitkä (ks. Myös kohta 4.5).
Erityistä varovaisuutta on noudatettava potilailla, joilla on aktiivinen tai lepotilassa oleva keuhkotuberkuloosi ja potilailla, joilla on hengitysteiden sieni- tai virusinfektio.
BUDEXANia tulee käyttää varoen potilailla, joilla on sieni- ja virusinfektioita (kuten tuhkarokko ja vesirokko) sekä joilla on glaukooma ja kaihi.
Suun kandidiaasia voi esiintyä inhaloitavan kortikosteroidihoidon aikana. Tämä infektio saattaa vaatia asianmukaista sienilääkehoitoa ja joillekin potilaille hoito on ehkä lopetettava (ks. Myös 4.2).
Systeemisiä vaikutuksia voi esiintyä inhaloitavilla kortikosteroideilla, erityisesti kun niitä määrätään suurina annoksina pitkiä aikoja. Näiden vaikutusten esiintyminen on epätodennäköisempää kuin suun kautta otettavalla kortikosteroidihoidolla. Mahdollisia systeemisiä vaikutuksia ovat Cushingin oireyhtymä, Cushingoid -näkökohta, lisämunuaisen vajaatoiminta, kasvun hidastuminen lapsilla ja nuorilla, luun mineraalitiheyden väheneminen, kaihi, glaukooma ja harvemmin erilaiset psykologiset tai käyttäytymiseen liittyvät vaikutukset, mukaan lukien psykomotorinen yliaktiivisuus, unihäiriöt, ahdistuneisuus, masennus tai aggressio (erityisesti lapsilla). Siksi on tärkeää, että inhaloitavan kortikosteroidiannos on pienin mahdollinen annos, jolla astma saadaan tehokkaasti hallintaan.
Näin ollen yllämainitun perusteella, kun astma on saatu hallintaan, ylläpitohoidossa käytettävän annoksen tulisi olla vähiten tehokas.
BUDEXANia tulee käyttää varoen lapsilla.
Kuten muidenkin inhalaatiohoitojen yhteydessä, paradoksaalinen bronkospasmi voi ilmaantua ja hengityksen vinkuminen lisääntyy välittömästi annon jälkeen. Tässä tapauksessa inhaloitava budesonidi on lopetettava välittömästi, potilas on arvioitava ja vaihtoehtoinen hoito aloitettava tarvittaessa.
Vaikutus kasvuun
On suositeltavaa, että pitkäaikaista inhaloitavaa kortikosteroidihoitoa saavien lasten pituutta seurataan säännöllisesti. Jos kasvu hidastuu, hoito on arvioitava uudelleen inhaloitavien kortikosteroidiannosten pienentämiseksi. Kortikosteroidihoidon hyödyt ja mahdollinen riski kasvun tukahduttamista on harkittava huolellisesti ja harkittava potilaan lähettämistä lasten keuhkosairaalaan.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Budesonidin yhteisvaikutuksia muiden astman hoitoon käytettyjen lääkkeiden kanssa ei ole havaittu.
Budesonidin metabolia välittää pääasiassa CYP3A4, sytokromi p450 -isoentsyymi. Tämän entsyymin estäjät, kuten ketokonatsoli ja itrakonatsoli, voivat siksi moninkertaistaa systeemisen budesonidialtistuksen (ks. 4.4). Koska tietoja ei ole annossuosituksen tueksi, näiden lääkkeiden yhdistelmää tulisi välttää. Jos tämä ei ole mahdollista, kahden hoidon välisen ajan tulee olla mahdollisimman pitkä ja budesonidiannoksen pienentämistä voidaan myös harkita.
Koska tätä vuorovaikutusta koskevia tietoja on saatavilla rajallisesti, kun käytetään suuria inhaloitavia budesonidiannoksia, plasman pitoisuudet voivat nousta merkittävästi (keskimäärin nelinkertaisesti), kun itrakonatsolia, 200 mg kerran vuorokaudessa, annetaan samanaikaisesti inhaloitavan budesonidin kanssa (kerta -annos on 1000 mcg).
Kohonneita plasman pitoisuuksia ja tehostuneita kortikosteroidien vaikutuksia havaittiin naisilla, joita hoidettiin myös estrogeenillä ja ehkäisysteroideilla, kun taas budesonidin käytön ja pieniannoksisten suun kautta otettavien ehkäisyvalmisteiden samanaikaisen käytön yhteydessä ei havaittu vaikutusta.
Koska lisämunuaisen toiminta voi olla estetty, ACTH -stimulaatiotesti "aivolisäkkeen vajaatoiminnan diagnosoimiseksi" voi antaa vääriä (alhaisia arvoja) tuloksia.
Suositelluilla annoksilla simetidiinillä on lievä vaikutus suun kautta annettavan budesonidin farmakokinetiikkaan, mikä ei ole kliinisesti merkittävää.
04.6 Raskaus ja imetys
Laajojen tulevien epidemiologisten tutkimusten tulokset ja markkinoille tulon jälkeiset maailmanlaajuiset kokemukset eivät viittaa haitallisiin vaikutuksiin sikiön / vastasyntyneen terveyteen inhaloitavan budesonidin käytön aikana raskauden aikana.
Kuten muidenkin lääkkeiden kohdalla, odotettua hyötyä äidille on punnittava sikiöön kohdistuvien riskien kanssa, kun budesonidia annetaan raskauden aikana. Budesonidi erittyy äidinmaitoon. Terapeuttisilla budesonidiannoksilla ei kuitenkaan odoteta olevan vaikutuksia imettävään lapseen. Budesonidia voidaan käyttää imetyksen aikana .. Ylläpitohoito inhaloidulla budesonidilla (200 tai 400 mcg kahdesti vuorokaudessa) imettäville astmaatikoille aiheuttaa merkityksettömän systeemisen altistuksen budesonidille imetettävillä imeväisillä.
Farmakokineettisessä tutkimuksessa imeväisen arvioitu vuorokausiannos oli 0,3% äidin päivittäisestä annoksesta molemmilla annostasoilla ja imeväisen keskimääräisten plasmakonsentraatioiden arvioitiin olevan 1/600 äidin plasmassa havaituista pitoisuuksista, olettaen täydellisen suun kautta otettavan imeväisen hyötyosuuden. Imeväisten plasmanäytteistä löydettyjen budesonidipitoisuuksien havaittiin aina olevan kvantifiointirajan alapuolella.
Inhaloitavan budesonidin käytöstä saatujen tietojen ja sen perusteella, että budesonidilla on lineaarinen farmakokineettinen profiili terapeuttisella annosalueella nenän kautta, inhalaationa, suun kautta ja peräsuoleen annetun budesonidin terapeuttisen annoksen jälkeen, imeväisten altistus on oletettavasti pieni.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
BUDEXAN -sumutinjousitus ei vaikuta ajokykyyn ja koneiden käyttökykyyn.
04.8 Haittavaikutukset
Kliiniset tutkimukset, kirjallisuus ja markkinointikokemus viittaavat siihen, että seuraavia haittavaikutuksia voi esiintyä.
Esiintymistiheydet on määritelty seuraavasti: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100 -
* katso "Valikoitujen haittavaikutusten kuvaus"; kasvojen ihoärsytys, lueteltu alla.
** katso alla oleva kohta "Pediatriset potilaat".
Harvoin tuntemattomien mekanismien vuoksi inhalaationa annettavat lääkkeet voivat aiheuttaa bronkospasmin.
Kun glukokortikosteroideja annetaan inhaloituna, systeemisten glukokortikosteroidivaikutusten merkkejä ja oireita voi esiintyä harvoin, mukaan lukien lisämunuaisten vajaatoiminta ja kasvun hidastuminen, jotka todennäköisesti riippuvat annoksesta, altistumisajasta, samanaikaisesta ja aiemmasta steroidihoidosta ja yksilöherkkyydestä.
Valittujen haittavaikutusten kuvaus
Kasvojen ihoärsytystä esimerkkinä yliherkkyysreaktioista on ilmennyt joissakin tapauksissa, joissa käytettiin naamaria sisältävää sumutinta. Ärsytyksen estämiseksi kasvojen iho on pestävä vedellä kasvonaamion käytön jälkeen.
Potilailla, joilla on äskettäin diagnosoitu krooninen obstruktiivinen keuhkosairaus (COPD) ja jotka aloittavat hoidon inhaloitavilla kortikosteroideilla, on suurempi riski saada keuhkokuume. Kuitenkin 8: n yhdistetyn kliinisen tutkimuksen painotettu arviointi, joka tehtiin 4643 keuhkoahtaumatautia sairastavalla ja budesonidilla hoidetulla potilaalla, ja 3643 potilasta, jotka oli satunnaistettu hoitoon ilman inhaloitavia kortikosteroideja, ei osoittanut lisääntynyttä keuhkokuumeen kehittymisen riskiä. Näistä kahdeksasta kliinisestä tutkimuksesta seitsemän ensimmäisen tulokset julkaistiin meta-analyysissä.
Pediatriset potilaat
Kun otetaan huomioon kasvun hidastumisen riski lapsipotilailla, kasvua on seurattava kohdassa 4.4 kuvatulla tavalla.
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeää, koska sen avulla voidaan jatkuvasti seurata lääkkeen hyöty -haitta -suhdetta. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta. "Osoite: www .agenziafarmaco.gov.it/it/Responsabili.
04.9 Yliannostus
Akuutti BUDEXAN -sumutinsuspension yliannostus ei edes suurina annoksina saisi aiheuttaa kliinisiä ongelmia.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: muut antihistamiinit, inhalaattorit, glukokortikoidit.
ATC -koodi: R03BA02
Paikallinen tulehdusta ehkäisevä vaikutus
Glukokortikosteroidien tarkka mekanismi astman hoidossa ei ole täysin ymmärretty. T-soluja, eosinofiilejä ja syöttösoluja vastaan suunnattu tulehdusta ehkäisevä vaikutus sekä tulehdusvälittäjien vapautumisen estäminen ja sytokiinien välittämän immuunivasteen esto ovat luultavasti tärkeitä. Budesonidin luontainen teho, mitattuna affiniteettina glukokortikoidireseptorien vertailut, on noin 15 kertaa suurempi kuin prednisoloni.
Kliinisessä astmapotilailla tehdyssä tutkimuksessa, jossa inhaloitavaa budesonidia verrattiin suun kautta annettavaksi samanlaisilla plasmakonsentraatioilla, osoitettiin "todisteita tilastollisesti merkitsevästä tehosta inhaloituna mutta ei suun kautta otettuna verrattuna lumelääkkeeseen. Siksi tavanomaisten budesonidiannosten terapeuttinen vaikutus , hengitettynä, voi johtua suurelta osin paikallisesta vaikutuksesta hengitysteissä.
Eläimillä ja potilailla tehdyissä provosoivissa tutkimuksissa budesonidilla on osoitettu olevan anafylaktinen ja tulehdusta ehkäisevä vaikutus, mikä ilmenee keuhkoputkien tukkeutumisasteen pienenemisenä välittömässä ja myöhäisessä allergisessa vasteessa.
Hengitysteiden reaktiivisuus:
Hyperreaktiivisilla potilailla budesonidin on osoitettu vähentävän hengitysteiden reaktiivisuutta histamiinille ja metakoliinille.
Vaikutus plasman kortisolipitoisuuksiin:
Terveillä vapaaehtoisilla budesonidilla tehdyt tutkimukset ovat osoittaneet annoksesta riippuvia vaikutuksia plasmaan ja virtsan kortisoliin. ACTH -testi osoitti, että budesonidihoito suositeltuina annoksina vaikutti merkittävästi vähemmän lisämunuaisten toimintaan kuin 10 mg prednisonia.
Pediatriset potilaat
Klinikka - astma
Budesonidin tehoa on arvioitu useissa tutkimuksissa, ja budesonidin on osoitettu olevan tehokas sekä aikuisilla että lapsilla jatkuvan astman ennaltaehkäisevänä hoitona kerran tai kahdesti päivässä. Alla on esimerkkejä edustavista tutkimuksista.
Klinikka - laryngotracheobronchitis
Laryngotracheobronchitis -lapsilla tehdyissä tutkimuksissa budesonidia verrattiin lumelääkkeeseen. Seuraavassa on esimerkkejä edustavista tutkimuksista, joissa arvioidaan budesonidin käyttöä laryngotracheobronchitis -lasten hoitoon.
Teho lapsilla, joilla on lievä tai kohtalainen kurkunpään tulehdus
Satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa suoritettiin 87 lasta (7 kk-9 v), jotka sairaalassa ja joilla oli kliininen diagnoosi laryngotracheobronchitis, sen määrittämiseksi, parantaako budesonidi laryngotracheobronchitis-oirepistettä vai lyhentääkö sairaalassaoloaikaa. Aloitusannosta budesonidia (2 mg) tai lumelääkettä seurasi 1 mg budesonidia tai lumelääkettä 12 tunnin välein.Budesonidi paransi tilastollisesti merkitsevästi laryngotracheobronchitis -pistemäärää 12 ja 24 tunnin ja 2 tunnin kohdalla potilailla, joiden laryngotracheobronchitis -oireyhtymän alkupiste oli yli 3. C "Myös oleskelun kestoa lyhennettiin 33%.
Teho lapsilla, joilla on kohtalainen tai vaikea laryngotracheobronkiitti
Satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa verrattiin budesonidin ja lumelääkkeen tehokkuutta kurkunpään ja keuhkoputkentulehduksen hoidossa 83 imeväisellä ja lapsella (6 kuukauden-8 vuoden ikäiset), jotka oli otettu sairaalaan laryngotrakeobronkiitin vuoksi. Potilaat saivat 2 mg budesonidia tai 12 tuntia enintään 36 tuntia tai sairaalasta lähtöön asti. Laryngotracheobronchitis -oireiden kokonaispistemäärä arvioitiin 0, 2, 6, 12, 24, 36 ja 48 tunnin kuluttua aloitusannoksesta. Kahden tunnin kuluttua sekä budesonidiryhmä että lumelääkeryhmä osoittivat samanlaista parannusta kurkunpään trakeobronkiitin oirepisteissä ilman tilastollisesti merkitseviä eroja ryhmien välillä. Kuuden tunnin kuluttua budesonidiryhmän laryngotrakeobronkiitin oirepisteet paranivat tilastollisesti merkitsevästi lumelääkeryhmään verrattuna, ja tämä parannus lumelääkkeeseen verrattuna oli yhtä ilmeinen 12 ja 24 tunnin kuluttua.
05.2 Farmakokineettiset ominaisuudet
Imeytyminen
Aikuisilla budesonidin systeeminen hyötyosuus suihkusumuttimella sumutettavan suspension annon jälkeen on noin 15% nimellisannoksesta ja 40-70% potilaille annetusta annoksesta. Pieni osa lääkkeen systeemisestä saatavuudesta tulee nauttimalla. Kun 2 mg: n kerta-annos on annettu, maksimipitoisuus plasmassa, joka saavutetaan noin 10-30 minuutin kuluttua sumutuksen aloittamisesta, on 4 nmol / l.
Jakelu
Budesonidin jakautumistilavuus on noin 3 l / kg. Sitoutuminen plasman proteiineihin on keskimäärin 85-90%.
Biotransformaatio
Maksan budesonidi metaboloituu nopeasti suurella prosenttiosuudella (> 90%) metaboliiteiksi, joille on ominaista alhainen glukokortikosteroidiaktiivisuus. Tärkeimmät metaboliitit ovat 6-beeta-hydroksibudesonidi ja 16-alfa-hydroksiprednisoloni, joiden glukokortikosteroidiaktiivisuus on alle 1% budesonidiin verrattuna.
Eliminaatio
Budesonidin metaboliitit erittyvät sellaisenaan tai konjugoituna pääasiassa munuaisten kautta. Muuttumatonta budesonidia ei löydy virtsasta. Terveillä aikuisilla budesonidilla on suuri systeeminen puhdistuma (noin 1,2 l / min) ja laskimonsisäisen annon jälkeen terminaalinen puoliintumisaika on keskimäärin 2–3 tuntia.
Lineaarisuus
Kliinisesti merkityksellisillä annoksilla budesonidin kineettiset parametrit ovat annoksesta riippuvaisia.
Pediatriset potilaat
Budesonidin systeeminen puhdistuma on noin 0,5 l / min 4-6-vuotiailla astmapotilailla. Lasten puhdistuma painokiloa kohti on noin 50% suurempi kuin aikuisilla. Budesonidin terminaalinen puoliintumisaika inhalaation jälkeen on noin 2,3 tuntia astmapotilailla, mikä on suunnilleen sama kuin terveillä aikuisilla.
Sumutettavan suspension annon jälkeen 4-6-vuotiailla astmapotilailla budesonidin systeeminen hyötyosuus suihkusumuttimen (PARI LC Plus ja Jet Pari Master -kompressori) kautta on noin 6% nimellisannoksesta ja 26% annos potilaille. Lasten systeeminen hyötyosuus on noin puolet terveistä aikuisista. 4-6-vuotiailla astmapotilailla 1 mg: n annoksen antamisen jälkeen suurin plasmakonsentraatio, joka saavutetaan noin 20 minuutin kuluttua sumutuksen aloittamisesta, on noin 2,4 nmol / l.
4-6-vuotiailla lapsilla budesonidin altistus (Cmax ja AUC) yhden 1 mg: n annoksen sumuttamisen jälkeen on verrattavissa siihen, mitä havaittiin terveillä aikuisilla, jotka saivat samaa annosta samaa järjestelmää käyttäen.
05.3 Prekliiniset tiedot turvallisuudesta
Akuutin, subakuutin ja kroonisen toksisuuden tutkimusten tulokset osoittavat, että budesonidin systeemiset vaikutukset ovat joko lievempiä tai samankaltaisia kuin muiden glukokortikosteroidien annon jälkeen havaitut vaikutukset, esimerkiksi vähentynyt painonnousu, imusolmukkeiden ja lisämunuaiskudosten surkastuminen.
Budesonidilla, jota arvioitiin kuudella eri testillä, ei havaittu mutageenisia tai klastogeenisiä vaikutuksia.
Aivojen glioomien ilmaantuvuuden lisääntyminen, joka havaittiin urosrotilla tehdyssä karsinogeenisuustutkimuksessa, ei vahvistettu kahdessa myöhemmässä tutkimuksessa, joissa glioomien ilmaantuvuutta havaittiin aktiivisilla lääkkeillä (budesonidi, prednisoloni, triamcinoloniasetaatti) hoidetuissa ryhmissä. samanlainen kuin kontrolliryhmissä.
Urosrotilla tehdyt karsinogeenisuustutkimukset antoivat mahdollisuuden havaita maksamuutoksia (primaariset maksasolukasvaimet), jotka vahvistettiin toisessa tutkimuksessa, joka suoritettiin käsittelemällä eläimiä budesonidilla ja viiteglukokortikosteroideilla. Nämä ilmentymät liittyvät luultavasti glukokortikosteroidien reseptorivaikutuksiin ja edustavat terapeuttiselle luokalle tyypillistä vaikutusta.
Saatavilla oleva kliininen kokemus osoittaa, että ei ole näyttöä siitä, että budesonidi tai muut glukokortikosteroidit aiheuttaisivat aivojen glioomia tai primaarisia maksasolukasvaimia ihmisillä.
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Dinatriumedetaatti; natriumkloridia; polysorbaatti 80; vedetön sitruunahappo; natriumsitraatti; injektionesteisiin käytettävä vesi.
06.2 Yhteensopimattomuus
Yhteensopimattomuuksia ei tunneta.
Katso yhteensopivat tuotteet kohdasta 4.2.
06.3 Voimassaoloaika
3 vuotta.
06.4 Säilytys
Säilytä alle 25 ° C: n lämpötilassa alkuperäispakkauksessa suojataksesi tuotetta valolta.
Alumiinipussin avaamisen jälkeen kerta-annospakkaukset on käytettävä 3 kuukauden kuluessa ja tämän ajan jälkeen jäljellä oleva tuote on hävitettävä.
Kalvopussin avaamisen jälkeen käyttämättömät kerta-annospakkaukset on säilytettävä pussissa valolta suojattuna.
Avattu kerta-annospakkaus on käytettävä 12 tunnin kuluessa. Tämän ajan jälkeen tuotejäämät on poistettava.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Kerta-annospakkaus pienitiheyksisessä polyeteenissä, joka sisältää 2 ml suspensiota.
Jokainen pakkaus sisältää 20 kerta-annospakkausta, jotka on jaettu 5 yksikön liuskoihin alumiinipussissa.
06.6 Käyttö- ja käsittelyohjeet
Katso kohta 4.2
07.0 MYYNTILUVAN HALTIJA
Geneettinen S.p.A., Via Della Monica n. 26, 84083 Castel San Giorgio (SA)
08.0 MYYNTILUVAN NUMERO
BUDEXAN 0,25 mg / ml Sumutettava suspensio -20 kerta -annospakkausta, joissa 2 ml AIC n. 036922019
BUDEXAN 0,5 mg / ml Suspensio sumutettavaksi -20 kerta -annospakkausta, joissa 2 ml AIC n. 036922021
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
Tammikuu 2008