Vaikuttavat aineet: Piroksikaami
FELDENE 20 mg kovat kapselit
FELDENE 20 mg liukoiset tabletit
Feldene -pakkausselosteita on saatavana seuraaville pakkauskokoille: - FELDENE 20 mg kovat kapselit, FELDENE 20 mg liukoiset tabletit
- FELDENE 20 mg / 1 ml injektioneste, liuos lihakseen
- FELDENE 20 mg peräpuikot
Miksi Feldeneä käytetään? Mitä varten se on?
Ennen Feldene -lääkkeen määräämistä lääkäri punnitsee tämän lääkkeen hyödyt ja sivuvaikutusten riskin. Lääkärisi saattaa joutua tarkistamaan sinut säännöllisesti ja kertomaan sinulle, kuinka usein sinut on tarkastettava Feldene -hoidon aikana.
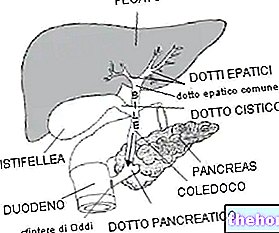
Feldene on tulehdusta ja kipua lievittävä lääke, jota käytetään lievittämään tiettyjä nivelrikon (nivelrikko: rappeuttava nivelsairaus), nivelreuman ja selkärankareuman aiheuttamia oireita, kuten turvotusta, jäykkyyttä ja nivelkipua . Feldene ei paranna niveltulehdusta ja lievittää sinua vain niin kauan kuin jatkat sen käyttöä.
Lääkärisi määrää Feldeneä vain silloin, kun muut ei-steroidiset tulehduskipulääkkeet (NSAID) eivät enää auta lievittämään oireitasi.
Vasta -aiheet Kun Feldeneä ei tule käyttää
ÄLÄ KÄYTÄ FELDENEÄ
- Jos olet allerginen (yliherkkä) vaikuttavalle aineelle tai tämän lääkkeen jollekin muulle aineelle
- Jos sinulla on joskus ollut haavauma tai verenvuoto tai perforaatio mahalaukussa tai suolistossa.
- Jos sinulla on haavauma tai verenvuoto tai perforaatio mahalaukussa tai suolistossa.
- Jos sinulla on tai on ollut aiempia ruoansulatuskanavan häiriöitä (maha- tai suolitulehdus), jotka altistavat verenvuotohäiriöille, kuten haavainen paksusuolitulehdus, Crohnin tauti, ruoansulatuskanavan syöpä, divertikuliitti (paksusuolen tulehtuneet tai tartunnan saaneet taskut / ontelot).
- Jos käytät muita tulehduskipulääkkeitä, mukaan lukien selektiiviset COX-2-estäjät ja asetyylisalisyylihappo (löytyy monista lääkkeistä, joita käytetään kivun lievittämiseen ja kuumeen alentamiseen). Muista, että monia tulehduskipulääkkeitä on saatavana myös ilman reseptiä.
- Jos käytät verenohennuslääkkeitä, kuten varfariinia, verihyytymien estämiseksi.
- Jos sinulla on koskaan ollut vaikea allerginen reaktio piroksikaamille, muille tulehduskipulääkkeille ja muille lääkkeille, erityisesti vakavat ihoreaktiot (riippumatta niiden vakavuudesta), kuten erythema multiforme, exfoliatiivinen dermatiitti (voimakas ihon punoitus ja hilseilevä tai kerrostunut kuorinta), vesiculo-bullous -reaktiot: Stevens-Johnsonin oireyhtymä, jolle on tunnusomaista punainen, syöpynyt, verinen tai kuorittu iho, jossa on rakkuloita, ja nekroottinen epidermolyysi, jolle on tunnusomaista rakkuloiden muodostuminen ja ihon pintakerroksen kuoriminen.
- Jos sinulla on ollut astman, nuhan, nenän polypoosin, angioedeeman tai nokkosihottuman oireita asetyylisalisyylihapon tai muiden tulehduskipulääkkeiden käytön aikana.
- Jos olet raskaana tai epäilet olevasi raskaana.
- Jos imetät.
- Jos olet alle 18 -vuotias.
- Jos sinulla on vaikea maksasairaus.
- Jos sinulla on vaikea munuaissairaus.
- Jos sinulla on kohtalainen tai vaikea sydämen vajaatoiminta.
- Jos sinulla on vaikea verenpaine.
- Jos sinulla on vakavia verisairauksia.
- Jos sinulla on verenvuoto diateesi (taipumus verenvuotoon usein).
Jos jokin näistä tiloista on olemassa, Feldene -valmistetta ei pitäisi määrätä sinulle. Kerro heti lääkärille.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Feldene -valmistetta
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Feldene -valmistetta.
Ole erityisen varovainen Feldene -valmisteen suhteen ja kerro siitä aina lääkärillesi ennen Feldene -valmisteen käyttöä; Kuten kaikki ei-steroidiset tulehduskipulääkkeet, Feldene voi aiheuttaa vakavia maha- ja suolireaktioita, kuten kipua, verenvuotoa ja haavaumia.
Lopeta Feldene -valmisteen käyttö välittömästi ja ota yhteys lääkäriisi, jos sinulla on vatsakipua tai jos sinulla on vatsan tai suolen verenvuodon merkkejä, kuten musta tai verinen uloste tai veren oksentelu.
Lopeta Feldene -valmisteen käyttö välittömästi ja ota yhteys lääkäriisi, jos sinulla on allerginen reaktio, kuten ihottuma, kasvojen turvotus, hengityksen vinkuminen tai hengitysvaikeudet.
Jos olet yli 70 -vuotias, lääkäri saattaa haluta minimoida hoidon keston ja tavata sinut useammin Feldene -hoidon aikana.
Jos olet yli 70 -vuotias tai käytät muita lääkkeitä, kuten kortikosteroideja tai tiettyjä masennuslääkkeitä, joita kutsutaan selektiivisiksi serotoniinin takaisinoton estäjiksi (SSRI -lääkkeiksi) tai asetyylisalisyylihappoa verihyytymien estämiseksi, lääkäri voi määrätä niitä yhdessä Feldenen kanssa vatsaan ja suolistoon.
Älä käytä tätä lääkettä, jos olet yli 80 -vuotias.
Jos sinulla on tai on ollut lääketieteellisiä ongelmia tai allergioita tai jos et ole varma, voitko ottaa Feldene -valmistetta, kerro siitä lääkärillesi ennen tämän lääkkeen käyttöä.
Kerro lääkärillesi, jos käytät muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt. Feldenen kaltaisiin lääkkeisiin voi liittyä sydänkohtauksen (sydäninfarkti) tai aivohalvauksen lisääntynyt riski. Kaikki riskit ovat todennäköisempiä suurilla annoksilla ja pitkillä hoidoilla. Älä ylitä suositeltua annosta tai hoidon kestoa.
Jos sinulla on sydänvaivoja, sinulla on ollut aivohalvaus tai luulet olevasi näiden sairauksien vaarassa (esimerkiksi jos sinulla on korkea verenpaine, diabetes tai korkea kolesteroli tai savu), keskustele hoidostasi lääkärin tai apteekkihenkilökunnan kanssa.
Feldene, kuten muutkin ei-steroidiset tulehduskipulääkkeet, vähentää verihiutaleiden aggregaatiota ja pidentää hyytymisaikaa; tämä mahdollisuus on muistettava suoritettaessa hematologisia testejä ja vaatii valppautta hoidettaessa samanaikaisesti verihiutaleiden aggregaatiota estävillä lääkkeillä.
Varovaisuutta on noudatettava, jos sinulla on aiemmin ollut kohonnut verenpaine ja / tai sydämen vajaatoiminta, koska NSAID -hoidon yhteydessä on raportoitu nesteen kertymistä ja turvotusta.
Erityistä varovaisuutta on noudatettava, jos sinulla on kardiovaskulaarinen vajaatoiminta, valtimoverenpaine, heikentynyt maksan tai munuaisten toiminta, munuaisten hypoperfuusio, nykyiset tai aiemmat verenmuutokset ja jos saat diureettihoitoa.
Jos olet astmaatikko, lääkkeen ja arakidonihapon aineenvaihdunnan välisen vuorovaikutuksen vuoksi voi esiintyä bronkospasmikriisejä ja mahdollisesti sokkia ja muita allergisia ilmiöitä.
Koska NSAID -hoidon aikana on havaittu silmämuutoksia, pitkäaikaishoidon yhteydessä on suositeltavaa suorittaa säännölliset silmälääkärintarkastukset.
Kuten muidenkin samankaltaisen vaikutuksen omaavien aineiden kohdalla, on havaittu atsotemian (veren typpipitoisuuksien) lisääntymistä, joka ei edisty tietyn tason yli annettaessa jatkuvaa annosta ja palaa normaaliarvoihin hoidon lopettamisen jälkeen.
Jos sinulla on diabetes, on suositeltavaa käydä säännöllisesti verikokeissa.
Hengenvaarallisia ihottumia (Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi) on raportoitu Feldene-valmisteen käytön yhteydessä.Näitä esiintyy aluksi pyöreinä punaisina täpliksi tai pyöreiksi laikkuiksi, joihin usein liittyy rakkuloita rungon keskiosassa.
Muita huomioitavia merkkejä ovat haavaumat suussa, kurkussa, nenässä, sukupuolielimissä ja sidekalvotulehdus (punaiset ja turvonnut silmät).
Näihin hengenvaarallisiin ihottumiin liittyy usein flunssan kaltaisia oireita. Ihottuma voi edetä laajojen rakkuloiden tai ihon kuorinnan kehittymiseen
Suurin riski vakavista ihoreaktioista ilmenee ensimmäisten hoitoviikkojen aikana. Jos sinulle on kehittynyt Stevens-Johnsonin oireyhtymä tai toksinen epidermaalinen nekrolyysi Feldene-valmisteen käytön yhteydessä, Feldene-valmistetta ei saa enää käyttää.
Jos sinulle kehittyy ihottuma tai nämä iho -oireet, lopeta Feldene -valmisteen käyttö, ota välittömästi yhteys lääkäriin ja kerro hänelle, että käytät tätä lääkettä.
Jos olet potilas, jolla on geneettisiä polymorfismeja (kuten CYP2C9 * 2- ja CYP2C9 * 3 -polymorfismeja), piroksikaamia on annettava varoen, koska piroksikaamin eliminaatio elimistöstä saattaa vähentyä ja veren piroksikaamipitoisuus voi olla korkea.
Jos suunnittelet raskautta, sinulla on hedelmällisyysongelmia tai tutkit hedelmällisyyttä, keskustele hoidostasi lääkärisi kanssa.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Feldenen vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä. Lääkkeet voivat joskus häiritä toisiaan.Lääkärisi voi rajoittaa Feldenen tai muiden lääkkeiden käyttöä tai sinun on ehkä otettava jokin muu lääke. On erityisen tärkeää ilmoittaa seuraavista tapauksista:
- jos käytät kipua lievittävää aspiriinia tai muita tulehduskipulääkkeitä
- jos käytät kortikosteroideja, lääkkeitä, joita käytetään erilaisten tilojen, kuten allergioiden ja hormonaalisen epätasapainon, hoitoon
- jos käytät verenohennuslääkkeitä, kuten varfariinia verihyytymien estämiseksi
- jos käytät tiettyjä masennuslääkkeitä, joita kutsutaan selektiivisiksi serotoniinin takaisinoton estäjiksi (SSRI)
- jos käytät lääkkeitä, kuten aspiriinia, verihyytymien estämiseksi
- jos käytät diureetteja, ACE: n estäjiä ja angiotensiini II -reseptorin salpaajia
- käytetään korkean verenpaineen ja sydänsairauksien hoitoon
- jos käytät litiumia
- käytetään masennuksen hoitoon
- jos käytät kinoloni -antibakteerisia lääkkeitä, joita käytetään bakteeri -infektioiden hoitoon
- jos käytät kohdunsisäisiä laitteita
Jos sinulla on jokin näistä tiloista, kerro siitä heti lääkärille.
FELDENE RUOKAN, JUOMIEN JA ALKOHOLIN KANSSA
On suositeltavaa olla juomatta alkoholia Feldene -hoidon aikana.
Varoitukset On tärkeää tietää, että:
Raskaus, imetys ja hedelmällisyys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
- Jos olet raskaana tai epäilet olevasi raskaana: kerro lääkärille, koska Feldene on vasta -aiheinen.
- Jos imetät: älä käytä Feldeneä. Kysy neuvoa lääkäriltäsi: saatat joutua lopettamaan imetyksen.
- Hedelmällisyys: Jos suunnittelet raskautta, sinulla on hedelmällisyysongelmia tai tutkit hedelmällisyyttä, kerro siitä lääkärillesi, sillä Feldene ei ehkä sovi sinulle.
Tulehduskipulääkkeiden, kuten Feldenen, käyttö voi viivästyttää tai estää munasarjojen repeämiä, mikä voi johtaa palautuvaan hedelmättömyyteen. Naisilla, joilla on vaikeuksia tulla raskaaksi tai tutkitaan hedelmättömyyttä, on harkittava tulehduskipulääkkeiden, mukaan lukien Feldene, lopettamista.
AJO -AJONEUVOT JA KONEIDEN KÄYTTÖ
Jos tunnet huimausta tai epätavallisen väsynyttä, ole erityisen varovainen ajaessasi tai käyttäessäsi koneita.
Feldene -kovat kapselit ja Feldene -liukoiset tabletit sisältävät laktoosia. Jos lääkäri on kertonut, että sinulla on jokin sokeri -intoleranssi, ota yhteys lääkäriisi ennen tämän lääkevalmisteen ottamista.
Feldene -kovat kapselit ja Feldene -liukoiset tabletit sisältävät alle 1 mmol (23 mg) natriumia annosta kohti, eli ne ovat olennaisesti "natriumittomia".
Annostus ja käyttötapa Feldene -valmisteen käyttö: Annostus
Ota tätä lääkettä juuri siten kuin lääkäri tai apteekki on määrännyt.
Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen. Lääkäri tarkistaa sinut säännöllisesti varmistaaksesi, että käytät optimaalista Feldene -annosta. Lääkärisi säätää hoidon pienimmäksi annokseksi, joka hallitsee parhaiten oireitasi. Älä missään tapauksessa muuta annostasi ilmoittamatta asiasta ensin lääkärillesi.
Aikuiset ja vanhukset:
Feldenen enimmäisvuorokausiannos on 20 milligrammaa kerta -annoksena. Jos olet yli 70 -vuotias, lääkäri voi määrätä pienemmän vuorokausiannoksen ja lyhentää hoidon kestoa.
Lääkärisi voi määrätä Feldeneä yhdessä toisen lääkkeen kanssa, joka suojaa vatsaasi ja suolistasi mahdollisilta sivuvaikutuksilta.
Älä lisää annosta:
Jos sinusta tuntuu, että lääke ei ole kovin tehokas, keskustele aina lääkärisi kanssa.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Feldeneä?
Jos unohdat ottaa Feldeneä:
Ota lääke heti kun muistat. Jos on jo melkein seuraavan annoksen aika, älä ota unohtunutta annosta, vaan ota seuraava annos oikeaan aikaan.
Jos otat enemmän Feldeneä kuin sinun pitäisi:
Oireet: Suurimmat yliannostuksen oireet ovat päänsärky, oksentelu, uneliaisuus, huimaus ja pyörtyminen.
Jos otat vahingossa Feldene -yliannoksen, ilmoita siitä heti lääkärille tai mene lähimpään sairaalaan.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Sivuvaikutukset Mitkä ovat Feldenen sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Lopeta Feldene -valmisteen käyttö välittömästi ja ota yhteys lääkäriisi, jos havaitset:
- vatsakipu tai vatsan tai suoliston puhkeamisen ja verenvuodon merkkejä, kuten musta tai verinen uloste tai veren oksentelu
- ihon ja silmän valkoisen osan keltainen / keltainen väri (keltaisuus);
- maksatulehdus;
- munuaisten toiminnan vakava heikkeneminen (munuaisten vajaatoiminta);
- kaikki allergisen reaktion merkit, kuten ihottuma tai kasvojen, huulten ja kurkun turvotus, joka voi aiheuttaa hengitys- ja nielemisvaikeuksia;
- ihoreaktiot, joille on tunnusomaista rakkulat, ihon punoitus tai kuorinta, haavaumat missä tahansa kehon osassa (esim. iho, suu, nenä, kurkku, sukupuolielimet), mukaan lukien vaikeat (Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi).
Muut mahdolliset haittavaikutukset on lueteltu alla:
Yleisimmät vaikutukset
- Ruoansulatuskanavan haavaumat ja ruoansulatuskanavan verenvuoto
- Pahoinvointi, oksentelu, ripuli, ilmavaivat, ummetus, mahahappo, vatsakipu, haavainen stomatiitti, tulehduksellinen suolistosairaus (koliitti ja Crohnin tauti)
- Nilkkojen, jalkojen ja jalkojen turvotus (nesteen kertyminen)
- Kohonnut verenpaine
- Sydämen vajaatoiminta (hengitysvaikeudet ja väsymys)
Vähemmän yleisiä vaikutuksia
- Sydänkohtaus (sydäninfarkti)
- Aivohalvaus
- Anoreksia
- Väsymys
- Anemia
- Rakkulat, ihon punoitus tai kuorinta (ihottuma) tai haavaumat missä tahansa kehon osassa (esim. Iho, suu, silmät, huulet tai kieli) tai muut allergisten reaktioiden merkit, kuten ihottuma, kasvojen, huulten, kielen turvotus , hengityksen vinkuminen
- Ihon ja silmien keltainen värjäytyminen (keltaisuus)
- Normaalien maksan toiminta -arvojen nousu
- Haimatulehdus
- Akuutti munuaisten vajaatoiminta, verta virtsassa, virtsaamisvaikeuksia
- Ei-proteiinitypen lisääntyminen veressä (lisääntynyt veren ureatyppi)
- Nilkkojen, jalkojen ja jalkojen turvotus (nesteen kertyminen)
- Kohonnut verenpaine (hypertensio)
- Nenäverenvuoto
- Päänsärky
- Uneliaisuus
- Kuurous tai soiminen korvassa
- Huimaus
- Näköhäiriöt
- Huonovointisuus
- Muutokset veressä ja imukudoksessa
- Gastriitti Harvinaiset vaikutukset
- Mustelmien ulkonäkö
- Verensokeriarvojen muutokset (hypoglykemia ja hyperglykemia)
- Hikoilu
- Kehon painon muutos
- Unettomuus
- Masennus
- Ihon turvotus, rakkulat tai kuorinta
- Ihon valoherkkyys
- Kuiva suu
- Eretismi
- Virtsarakon toiminnan muutokset
- Shokki
- Hiustenlähtö
- Kynsien kasvun muutokset
- Tappava hepatiitti
Hyvin harvinaisia vaikutuksia
- Henkeä uhkaavat ihottumat (Stevens-Johnsonin oireyhtymä, toksinen epiedermaalinen nekrolyysi)
Vaikutukset, joiden esiintymistiheys on tuntematon (esiintymistiheyttä ei voida arvioida saatavilla olevien tietojen perusteella)
- Palautuva naisten hedelmättömyys
- Nefroottinen oireyhtymä
- Glomerulonefriitti
- Interstitiaalinen nefriitti
- Munuaisten vajaatoiminta
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. Yhteystiedot alla). lääke
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä ulkopakkauksessa ja etiketissä mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
PAKKAUKSEN SISÄLTÖ JA MUUTA TIETOA
Mitä Feldene sisältää
- Vaikuttava aine on piroksikaami.
Yksi kova kapseli sisältää 20 mg Piroksikaamia; jokainen liukoinen tabletti sisältää 20 mg piroksikaamia.
- Muut aineet ovat:
kovat kapselit: maissitärkkelys, laktoosi, magnesiumstearaatti, natriumlauryylisulfaatti. Sisältävän kapselin muodostaa: liivate, titaanidioksidi (E171).
liukoiset tabletit: laktoosi, mikrokiteinen selluloosa, hydroksipropyyliselluloosa, natriumstearyylifumaraatti.
Lääkevalmisteen kuvaus ja pakkauskoot
FELDENE 20 mg kovat kapselit - kartonki, joka sisältää 30 kapselia PVC- ja raaka -alumiiniläpipainopakkauksissa
FELDENE 20 mg liukoiset tabletit - pahvipakkaus, joka sisältää 30 tablettia PVC- ja raaka -alumiiniläpipainopakkauksissa
Lähdepakkaus: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
FELDENE
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
Jokainen kova kapseli, liukoinen tabletti ja 20 mg peräpuikko sisältää:
Aktiivinen periaate
Piroksikaami 20 mg
Apuaineet, joiden vaikutukset tunnetaan:
Yksi kova kapseli sisältää 233 mg laktoosia ja 0,15 mg natriumlauryylisulfaattia.
Yksi liukoinen tabletti sisältää 375 mg laktoosia ja 5 mg natriumstearyylifumaraattia.
Täydellinen apuaineluettelo, katso kohta 6.1
03.0 LÄÄKEMUOTO
Kovat kapselit
Liukoiset tabletit
Peräpuikot
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Piroksikaami on tarkoitettu nivelrikon, nivelreuman tai selkärankareuman oireenmukaiseen hoitoon.
Turvallisuusprofiilinsa vuoksi piroksikaami ei ole ensisijainen tulehduskipulääke (ks. Kohdat 4.2, 4.3 ja 4.4).
Päätös piroksikaamin määräämisestä tulee perustua yksittäisen potilaan kokonaisriskien arviointiin (ks. Kohdat 4.3 ja 4.4).
04.2 Annostus ja antotapa
Piroksikaamin määräämisen saa aloittaa lääkäri, jolla on kokemusta tulehduksellisia tai rappeuttavia reumasairauksia sairastavien potilaiden diagnosoinnista ja hoidosta.
Suurin suositeltu vuorokausiannos on 20 mg.
Haittavaikutukset voidaan minimoida käyttämällä pienintä tehokasta annosta mahdollisimman lyhyessä hoidon kestossa, joka tarvitaan oireiden hallintaan. Hoidon hyöty ja siedettävyys on arvioitava uudelleen 14 päivän kuluessa. Jos hoidon jatkaminen on tarpeen, jälkimmäiseen on liitettävä usein uudelleenarviointi.
Koska piroksikaamin käyttöön on osoitettu liittyvän lisääntynyt ruoansulatuskanavaan liittyvien komplikaatioiden riski, mahdollinen yhdistelmähoidon tarve ruoansulatuskanavan (esim. Misoprostolin tai protonipumpun estäjien) kanssa on arvioitava huolellisesti, erityisesti iäkkäillä potilailla .
Annostusta ja käyttöaiheita lapsille ei ole vielä varmistettu.
Iäkkäiden potilaiden hoidossa annoksen on oltava huolellisesti lääkäri, jonka on arvioitava edellä mainittujen annosten mahdollinen pienentäminen.
04.3 Vasta -aiheet
• Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
• Aiempi ruoansulatuskanavan haavauma, verenvuoto tai perforaatio.
• Aiemmat ruoansulatuskanavan häiriöt, jotka altistavat verenvuotohäiriöille, kuten haavainen paksusuolitulehdus, Crohnin tauti, ruoansulatuskanavan syöpä tai divertikuliitti.
• Potilaat, joilla on aktiivinen peptinen haava, maha -suolikanavan tulehdukselliset häiriöt tai maha -suolikanavan verenvuoto.
• Potilaat, joilla on gastriitti, dyspepsia, vaikea maksa- ja munuaissairaus, kohtalainen tai vaikea sydämen vajaatoiminta, vaikea verenpaine, vaikeat verisairaudet, verenvuototaipumus.
• Muiden tulehduskipulääkkeiden samanaikainen käyttö, mukaan lukien selektiiviset COX-2-estäjät ja asetyylisalisyylihappo, jotka annetaan kipulääkkeinä.
• Antikoagulanttien samanaikainen käyttö (ks. Kohdat 4.4 ja 4.5).
• Anamneesissa on esiintynyt kaikenlaisia vakavia lääkeallergisia reaktioita, erityisesti ihoreaktioita, kuten erythema multiforme, Stevens-Johnsonin oireyhtymä, nekroottinen epidermolyysi.
• Aiemmat ihoreaktiot (vakavuudesta riippumatta) piroksikaamille, muille tulehduskipulääkkeille ja muille lääkkeille.
• Tiedetty tai epäilty raskaus, imetyksen aikana ja lapsilla (ks. Kohta 4.6).
Ristiinherkkyys on mahdollista asetyylisalisyylihapon tai muiden ei-steroidisten tulehduskipulääkkeiden kanssa. Piroksikaamia ei saa antaa potilaille, joilla asetyylisalisyylihappo tai muut ei-steroidiset tulehduskipulääkkeet aiheuttavat astman, nuhan, nenän polypoosin, angioedeeman ja nokkosihottuman oireita.
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Haittavaikutuksia voidaan minimoida käyttämällä pienintä tehokasta annosta mahdollisimman lyhyen hoidon ajan, joka tarvitaan oireiden hallintaan.
Hoidon kliinistä hyötyä ja siedettävyyttä on arvioitava uudelleen säännöllisesti ja hoito on lopetettava heti, kun ilmenee ensimmäisiä ihoreaktioiden merkkejä tai suuria ruoansulatuskanavan tapahtumia.
Ruoansulatuskanavan (GI) vaikutukset, Ruoansulatuskanavan haavaumien, verenvuodon ja perforaation riski
Tulehduskipulääkkeet, mukaan lukien piroksikaami, voivat aiheuttaa vakavia ruoansulatuskanavan tapahtumia, kuten verenvuotoa, haavaumia ja mahalaukun, ohutsuolen tai paksusuolen perforaatiota, jotka voivat olla hengenvaarallisia. tulehduskipulääkkeiden kanssa.
Sekä lyhyellä että pitkäaikaisella altistumisella tulehduskipulääkkeille on lisääntynyt vakavien ruoansulatuskanavan tapahtumien riski.Havainnointitutkimuksista saadut todisteet viittaavat siihen, että piroksikaamiin voi verrattuna muihin tulehduskipulääkkeisiin liittyä lisääntynyt vakavan ruoansulatuskanavan toksisuuden riski.
Potilaita, joilla on merkittäviä riskitekijöitä vakaville ruoansulatuskanavan tapahtumille, saa hoitaa piroksikaamilla vain huolellisen harkinnan jälkeen (ks. Kohta 4.3 ja kohta alla).
Mahdollista yhdistelmähoidon tarvetta ruoansulatuskanavan estäjien (esim. Misoprostolin tai protonipumpun estäjien) kanssa on harkittava huolellisesti (ks. Kohta 4.2).
Vakavat ruoansulatuskanavan komplikaatiot
Riskiryhmien tunnistaminen
Vakavien ruoansulatuskanavan komplikaatioiden riski kasvaa iän myötä. Yli 70 -vuotiailla on suurempi komplikaatioiden riski. Antamista yli 80 -vuotiaille potilaille tulee välttää.
Potilailla, jotka saavat samanaikaisesti suun kautta otettavia kortikosteroideja, selektiivisiä serotoniinin takaisinoton estäjiä (SSRI), antikoagulantteja, kuten varfariinia tai verihiutaleita estäviä aineita, kuten pieniannoksista asetyylisalisyylihappoa, on suurempi riski vakavista ruoansulatuskanavan komplikaatioista (ks. Alla ja kohta 4.5). Kuten muidenkin tulehduskipulääkkeiden kanssa, piroksikaamin käyttöä yhdessä ruoansulatuskanavan estäjien (esim. Misoprostolin tai protonipumpun estäjien) kanssa tulee harkita näillä riskipotilailla.
Potilaiden ja lääkäreiden tulee kiinnittää huomiota ruoansulatuskanavan haavaumien ja / tai verenvuotojen oireisiin ja oireisiin piroksikaamihoidon aikana. Potilaita tulee pyytää ilmoittamaan kaikista uusista tai epätavallisista vatsan oireista, joita ilmenee hoidon aikana. Jos ruoansulatuskanavan komplikaatiota epäillään hoidon aikana, piroksikaamin käyttö on lopetettava välittömästi ja harkittava kliinistä arviointia ja vaihtoehtoista hoitoa.
Sydän- ja aivoverisuonivaikutukset
Asianmukaista seurantaa ja opastusta tarvitaan potilailla, joilla on aiemmin ollut kohonnut verenpaine ja / tai kongestiivinen sydämen vajaatoiminta, koska NSAID -hoidon yhteydessä on raportoitu nesteen kertymistä ja turvotusta.
Kliiniset tutkimukset ja epidemiologiset tiedot viittaavat siihen, että joidenkin tulehduskipulääkkeiden (etenkin suurina annoksina ja pitkäaikaishoidossa) käyttö voi liittyä jonkin verran suurentuneeseen valtimotromboottisten tapahtumien (esim. Sydäninfarkti tai aivohalvaus) riskiin. poissulkea samanlainen riski piroksikaamille.
Potilaita, joilla on hallitsematon hypertensio, kongestiivinen sydämen vajaatoiminta, todettu iskeeminen sydänsairaus, perifeerinen valtimotauti ja / tai aivoverisuonisairaus, saa hoitaa piroksikaamilla vain huolellisen harkinnan jälkeen. Samanlaisia näkökohtia on harkittava ennen pitkäaikaishoidon aloittamista potilailla, joilla on sydän- ja verisuonitautien riskitekijöitä (esim. Kohonnut verenpaine, hyperlipidemia, diabetes mellitus, tupakointi).
Piroksikaami vähentää verihiutaleiden aggregaatiovoimaa ja pidentää hyytymisaikaa. Piroksikaami voi kuitenkin myös häiritä pieniannoksisen aspiriinin verihiutaleiden vastaista vaikutusta (ks. Kohta 4.5). Nämä ominaisuudet on otettava huomioon suoritettaessa hematologisia testejä ja kun potilasta hoidetaan muilla verihiutaleiden aggregaatiota estävillä aineilla.
Potilaita, joiden munuaisten toiminta on heikentynyt, on seurattava säännöllisesti, koska piroksikaamin aiheuttama prostaglandiinisynteesin esto näillä potilailla voi johtaa munuaisten perfuusion vakavaan heikkenemiseen, mikä voi johtaa akuuttiin munuaisten vajaatoimintaan. hoidon katsotaan olevan vaarassa.
Varovaisuutta on noudatettava myös hoidettaessa potilaita, joilla on maksan vajaatoiminta. Myös näiden osalta on suositeltavaa turvautua kliinisten ja laboratorioparametrien säännölliseen seurantaan, etenkin jos hoito on pitkäaikaista.
Lääkkeen vuorovaikutuksessa arakidonihapon metabolian kanssa astmaatikoilla ja alttiilla henkilöillä voi esiintyä bronkospasmikriisejä ja mahdollisesti sokkia ja muita allergisia ilmiöitä.
Koska silmämuutoksia on havaittu tulehduskipulääkkeiden hoidon aikana, on suositeltavaa suorittaa säännölliset silmälääkkeet pitkäaikaishoidon yhteydessä. On myös suositeltavaa tarkistaa usein diabetespotilaiden glukoositaso ja protrombiiniaika potilailla, jotka saavat samanaikaisesti antikoagulanttihoitoa dikumarolijohdannaisilla.
Maksavaikutukset
Piroksikaami voi aiheuttaa kuolemaan johtavan hepatiitin ja keltaisuuden. Vaikka nämä reaktiot ovat harvinaisia, piroksikaami on lopetettava, jos maksan toimintakokeet pysyvät epänormaaleina tai pahenevat, jos ilmenee maksasairauden mukaisia kliinisiä oireita tai jos ilmenee systeemisiä oireita (esim. Eosinofilia, ihottuma jne.).
Ihon reaktiot
Seuraavia hengenvaarallisia ihoreaktioita on raportoitu Feldenen käytön yhteydessä: Stevens-Johnsonin oireyhtymä (SJS) ja toksinen epidermaalinen nekrolyysi (TEN).
Potilaille on ilmoitettava oireista ja heitä on seurattava tarkasti ihoreaktioiden varalta. Suurin riski SJS: n ja TEN: n kehittymiselle esiintyy hoidon ensimmäisten viikkojen aikana.
Jos SJS: n ja TEN: n oireita ja merkkejä ilmenee (esim. Etenevä ihottuma, johon usein liittyy rakkuloita tai limakalvovaurioita), Feldene -hoito on lopetettava.
Parhaat tulokset SJS: n ja TEN: n hoidossa saadaan varhaisella diagnoosilla ja hoidon välittömällä lopettamisella minkä tahansa epäillyn lääkkeen kanssa.
Jos potilaalle on kehittynyt SJS tai TEN Feldene -hoidon aikana, Feldene -valmistetta ei saa enää käyttää tällä potilaalla.
CYP2C9 -substraattien heikot metaboloijat
Potilaille, joiden tiedetään tai epäillään olevan heikkoja CYP2C9 -metaboloijia aiempien kokemusten tai muiden CYP2C9 -substraattien kokemusten perusteella, piroksikaamia tulee antaa varoen, koska heillä saattaa olla liian korkea plasmataso metabolisen puhdistuman vuoksi (ks. Kohta 5.2).
Käytä oraalisten antikoagulanttien kanssa
Tulehduskipulääkkeiden, mukaan lukien piroksikaamin, samanaikainen käyttö suun kautta otettavien antikoagulanttien kanssa lisää ruoansulatuskanavan ja ei-ruoansulatuskanavan verenvuodon riskiä, ja siksi sitä on vältettävä. Apiksabaani, dabigatraani, rivaroksabaani) Hyytymistä (INR) on seurattava potilailla, jotka käyttävät varfariini- / kumariinityyppisiä antikoagulantteja. (ks. kohdat 4.3 ja 4.5).
Piroksikaamin, kuten kaikkien lääkkeiden, jotka estävät prostaglandiinisynteesiä ja syklo -oksigenaasia, käyttöä ei suositella naisille, jotka aikovat tulla raskaaksi.
Piroksikaamin anto on lopetettava naisilla, joilla on hedelmällisyysongelmia tai joille tehdään hedelmällisyystutkimuksia.
Tärkeää tietoa joistakin ainesosista
Feldene -kovat kapselit ja Feldene -liukoiset tabletit sisältävät laktoosia.
Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, laktaasipuutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää tätä lääkettä.
Feldene -kovat kapselit ja Feldene -liukoiset tabletit sisältävät alle 1 mmol (23 mg) natriumia annosta kohti, eli ne ovat olennaisesti "natriumittomia".
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Asetyylisalisyylihappo tai muut tulehduskipulääkkeet : kuten muidenkin tulehduskipulääkkeiden kanssa, piroksikaamin käyttöä yhdessä asetyylisalisyylihapon tai muiden tulehduskipulääkkeiden kanssa, mukaan lukien muut piroksikaamiformulaatiot, tulee välttää, koska käytettävissä olevat tiedot eivät osoita, että nämä yhdistelmät saisivat paremman parannuksen kuin pelkkä piroksikaami; lisäksi haittavaikutusten mahdollisuus kasvaa (ks. kohta 4.4). Ihmisillä tehdyt tutkimukset ovat osoittaneet, että piroksikaamin ja asetyylisalisyylihapon samanaikainen käyttö pienentää piroksikaamin pitoisuutta plasmassa noin 80% tavanomaisesta arvosta.
Piroksikaami on vuorovaikutuksessa asetyylisalisyylihapon, muiden ei-steroidisten tulehduskipulääkkeiden ja verihiutaleiden aggregaatiota estävien aineiden kanssa (ks. Kohdat 4.3 ja 4.4).
In vitro -tutkimukset ovat osoittaneet, että piroksikaami häiritsee pieniannoksisen aspiriinin verihiutaleiden vastaista vaikutusta ja voi siten häiritä sydän- ja verisuonitautien estohoitona annettavaa aspiriinia.
Kortikosteroidit : lisääntynyt ruoansulatuskanavan haavauman tai verenvuodon riski (ks. kohta 4.4).
Antikoagulantit Tulehduskipulääkkeet, mukaan lukien piroksikaami, voivat tehostaa antikoagulanttien, kuten varfariinin, vaikutuksia. Siksi piroksikaamin käyttöä yhdessä antikoagulanttien, kuten varfariinin, kanssa tulee välttää (ks. Kohdat 4.3 ja 4.4).
Verihiutaleita estävät aineet ja selektiiviset serotoniinin takaisinoton estäjät (SSRI) : lisääntynyt ruoansulatuskanavan verenvuodon riski (ks. kohta 4.4).
Diureetit, ACE: n estäjät, angiotensiini II -antagonistit ja beetasalpaajat: Tulehduskipulääkkeet voivat heikentää diureettien ja muiden verenpainelääkkeiden, mukaan lukien ACE: n estäjät, angiotensiini II -antagonistit ja beetasalpaajat, vaikutusta. Joillakin potilailla, joilla on munuaisten vajaatoiminta (esim. Dehydratoituneet potilaat tai iäkkäät potilaat, joilla on munuaisten vajaatoiminta), ACE: n estäjän tai angiotensiini II -reseptorin salpaajan ja / tai diureetin samanaikainen käyttö syklisysteemiä hapettavaksi estävien aineiden kanssa voi johtaa munuaisten heikkenemiseen entisestään Nämä yhteisvaikutukset on otettava huomioon potilailla, jotka käyttävät piroksikaamia samanaikaisesti ACE: n estäjien tai angiotensiini II -antagonistien ja / tai diureettien kanssa.
Siksi yhdistelmää on käytettävä varoen, erityisesti iäkkäillä potilailla.
Potilaiden tulee olla riittävästi nesteytettyjä ja munuaisten toimintaa on seurattava samanaikaisen hoidon aloittamisen jälkeen.
Jos samanaikaisesti käytetään kaliumia sisältäviä lääkkeitä tai kaliumretentiota aiheuttavia diureetteja, seerumin kaliumpitoisuuden kohoamisen (hyperkalemia) riski on suurempi.
Litium : litiumin ja tulehduskipulääkkeiden samanaikainen käyttö lisää plasman litiumtasoja.
Metotreksaatti : kun metotreksaattia annetaan yhdessä tulehduskipulääkkeiden, mukaan lukien piroksikaami, kanssa, tulehduskipulääkkeet voivat vähentää metotreksaatin eliminaatiota ja lisätä plasman pitoisuuksia. Varovaisuutta suositellaan erityisesti potilaille, jotka käyttävät suuria annoksia metotreksaattia.
Piroksikaami sitoutuu paljon proteiineihin ja syrjäyttää todennäköisesti muita proteiineihin sitoutuneita lääkkeitä. Lääkärien on seurattava potilaita, jotka käyttävät piroksikaamia ja runsaasti proteiineja sitovia lääkkeitä annoksen muuttamiseksi. Simetidiinin antamisen jälkeen piroksikaamin imeytyminen osoittaa lievää nousua, mutta tämän lisääntymisen ei kuitenkaan ole osoitettu olevan kliinisesti merkittävä.
Vältä alkoholin nauttimista.
Piroksikaami voi heikentää kohdunsisäisten laitteiden tehokkuutta.
Ei-steroidisten tulehduskipulääkkeiden käyttöä samanaikaisesti kinolonilääkkeiden kanssa ei suositella.
04.6 Raskaus ja imetys
Piroksikaami on vasta -aiheinen raskauden, vakiintuneen tai epäillyn raskauden ja imetyksen aikana.
Hedelmällisyys
Vaikutusmekanismin perusteella tulehduskipulääkkeiden, mukaan lukien piroksikaami, käyttö voi viivästyttää tai estää munasarjojen follikkelien repeämisen, johon on liittynyt palautuva hedelmättömyys. Harkitse tulehduskipulääkkeiden, mukaan lukien piroksikaamin, lopettamista.
Raskaus
Prostaglandiinisynteesin estäminen voi vaikuttaa haitallisesti raskauteen ja / tai alkion / sikiön kehitykseen.
Epidemiologisten tutkimusten tulokset osoittavat, että keskenmenon ja sydämen epämuodostumien ja mahalaukun riski kasvaa, kun prostaglandiinisynteesin estäjää on käytetty raskauden alkuvaiheessa. Sydämen epämuodostumien absoluuttinen riski kasvoi alle 1 prosentista noin 1,5 prosenttiin. Riskiä on pidetty eläimillä prostaglandiinisynteesin estäjien antamisen on osoitettu aiheuttavan lisääntyneitä menetyksiä ennen ja jälkeen istutuksen sekä alkion ja sikiön kuolleisuutta.
Lisäksi eri epämuodostumien, myös sydän- ja verisuonitautien, esiintyvyyttä on raportoitu eläimillä, joille on annettu prostaglandiinisynteesin estäjiä organogeenisen jakson aikana.
Raskauden kolmannen kolmanneksen aikana kaikki prostaglandiinisynteesin estäjät voivat altistua
sikiö:
• sydän- ja keuhkotoksisuus (valtimokanavan ennenaikainen sulkeminen ja keuhkoverenpainetauti);
• munuaisten vajaatoiminta, joka voi edetä munuaisten vajaatoimintaan oligo-hydroamniosilla;
äiti ja vastasyntynyt raskauden lopussa:
• mahdollinen verenvuodon pidentyminen ja verihiutaleiden vastainen vaikutus, joka voi ilmetä jopa hyvin pienillä annoksilla;
• kohdun supistusten esto, joka johtaa synnytyksen viivästymiseen tai pitkittymiseen.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Piroksikaami voi muuttaa valppautta siten, että se vaarantaa moottoriajoneuvojen ajamisen ja osallistumisen valppautta vaativiin toimintoihin.
04.8 Haittavaikutukset
Ruoansulatuskanava : yleisimmin havaitut haittavaikutukset ovat luonteeltaan ruoansulatuskanavaa. Erityisesti iäkkäillä potilailla voi esiintyä mahahaava, ruoansulatuskanavan perforaatio tai verenvuoto, joskus kuolemaan johtava (ks. Kohta 4.4).
Piroksikaamin annon jälkeen on raportoitu pahoinvointia, oksentelua, ripulia, ilmavaivoja, ummetusta, dyspepsiaa, vatsakipua, melaenaa, veriokseemia, haavaista stomatiittia, koliitin ja Crohnin taudin pahenemista (ks. Kohta 4.4).
Gastriittia on havaittu harvemmin.
Turvotusta, kohonnutta verenpainetta, naisten hedelmällisyyden heikkenemistä ja sydämen vajaatoimintaa on raportoitu tulehduskipulääkkeiden käytön yhteydessä.
Kliiniset tutkimukset ja epidemiologiset tiedot viittaavat siihen, että joidenkin tulehduskipulääkkeiden (etenkin suurina annoksina ja pitkäaikaishoidossa) käyttö voi liittyä jonkin verran suurentuneeseen valtimotromboottisten tapahtumien (esim. Sydäninfarkti tai aivohalvaus) riskiin (ks. Kohta 4.4).
Muut raportoidut haittavaikutukset: ruokahaluttomuus, yliherkkyysilmiöt, kuten ihottuma, päänsärky, huimaus, uneliaisuus, huonovointisuus, tinnitus, kuurous, astenia, muutokset hematologisissa parametreissa, alentunut hemoglobiini ja hematokriitti, anemia.
Kuten muidenkin samankaltaisen vaikutuksen omaavien aineiden kohdalla, atsotemian lisääntymistä on havaittu joillakin potilailla, jotka eivät edisty tietyn tason yli jatkaessaan antamista; ne palaavat normaaliarvoihin hoidon lopettamisen jälkeen.
Kasvojen ja käsien allerginen turvotus, lisääntynyt ihon valoherkkyys, näköhäiriöt, aplastinen anemia, hemolyyttinen anemia, pansytopenia, trombosytopenia, Schoenlein-Henoch-purppura, eosinofilia, kohonneet maksan toimintaindeksit, keltaisuus voi esiintyä harvoin, harvoin kuolemaan johtavaa hepatiittia.
Harvinaisia haimatulehdustapauksia on raportoitu. Joissakin tapauksissa on raportoitu hematuriaa, dysuriaa, akuuttia munuaisten vajaatoimintaa, nesteen kertymistä, joka voi ilmetä turvotuksena erityisesti alaraajojen kaltevilla alueilla tai sydän- ja verenkiertohäiriöitä (hypertensio, dekompensaatio).
Nefroottisen oireyhtymän, glomerulonefriitin, interstitiaalisen nefriitin ja munuaisten vajaatoiminnan tapauksia on raportoitu.
Satunnaisia tapauksia on raportoitu: nenäverenvuoto, suun kuivuminen, erythema multiforme, ihottuma, ihon kuorinta, hikoilu, hypoglykemia, hyperglykemia, kehon painon muutokset, erektio, unettomuus, masennus, virtsarakon toimintahäiriö, sokki ja varoitusoireet, hiustenlähtö, Kynsien kasvu, rakkulaiset reaktiot Vakavia ihon haittavaikutuksia, kuten Stevens-Johnsonin oireyhtymää (SJS) ja toksista epidermaalista nekrolyysiä (TEN), on raportoitu (ks. Kohta 4.4).
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeää, koska se mahdollistaa lääkkeen hyöty -riskisuhteen jatkuvan seurannan.
Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta osoitteessa https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Yliannostus
Oireet: Suurimmat yliannostuksen oireet ovat päänsärky, oksentelu, uneliaisuus, huimaus ja pyörtyminen.
Yliannostustapauksessa oireenmukainen tukihoito on aiheellista.
Vaikka tutkimuksia ei ole toistaiseksi tehty, hemodialyysi ei todennäköisesti ole hyödyllinen piroksikaamin eliminaation helpottamisessa, koska lääkkeelle on ominaista korkea sitoutuminen plasman proteiineihin.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: ei-steroidiset tulehdus- ja reumalääkkeet.
ATC -koodi: M01AC01.
Piroksikaami, joka kuuluu bentsotiatsiinikarboksiamidien-N-heterosyklien ryhmään, on uuden tulehduskipulääkeryhmän, oksikaamien, ensimmäinen yhdiste. Piroksikaamilla on anti-inflammatorinen, analgeettinen ja kuumetta alentava vaikutus, farmakologiset vaikutukset ovat samanlaiset kuin muiden ei-steroidisten tulehduskipulääkkeiden. Eläinkokeet ovat osoittaneet, että piroksikaami vaikuttaa solujen siirtymiseen tulehduskohtiin. Kuten muutkin tulehduskipulääkkeet, piroksikaami häiritsee prostaglandiinisynteesiä estämällä syklo -oksigenaasia. Toisin kuin indometasiini, piroksikaami on palautuva prostaglandiinisynteesin estäjä.Yhdeksässä aktiivisessa nivelreumapotilaassa tehdyssä tutkimuksessa piroksikaamin (20 mg / vrk 15 päivän ajan) havaittiin heikentävän merkittävästi polymorfonukleaaristen solujen toimintaa. (PMN) superoksidianionien tuotanto perifeerisessä veressä ja nivelnesteessä sekä PMN- ja PMN-elastaasin pitoisuus nivelnesteessä PMN-vasteiden modulaatio voi edistää piroksikaamin tulehdusta estävää vaikutusta.
05.2 Farmakokineettiset ominaisuudet
Imeytyminen ja jakautuminen
Piroksikaami imeytyy helposti sekä suun kautta että peräsuolen kautta.Oraalisen annon jälkeen ruoan läsnäolo vähentää vaikuttavan aineen imeytymisnopeutta, mutta ei prosenttiosuutta.
Yhdellä annoksella pitoisuus on vakaa koko päivän.
Jatkuva hoito annoksella 20 mg / vrk yhden vuoden ajan tuottaa veren pitoisuuksia, jotka ovat samankaltaisia kuin ensimmäisen annoksen saavuttamisen jälkeen vakaa tila.
Plasman lääkeainepitoisuudet ovat verrannollisia 10 mg: n ja 20 mg: n annoksille ja saavuttavat yleensä huippunsa 3-5 tunnin kuluessa annosta. Piroksikaamin huippupitoisuudet plasmassa 1,5 - 2 mcg / ml saavutetaan yleensä yhdellä 20 mg: n annoksella, kun taas toistuvien 20 mg: n piroksikaamiannosten jälkeen lääkkeen huippupitoisuudet plasmassa yleensä stabiloituvat tasolle 3-8 mcg / ml. Useimmat potilaat saavuttavat plasman tasot vakaa tila 7-12 päivän kuluessa.
Annostusohjelma, jossa latausannokset ovat 40 mg / vrk kahden ensimmäisen päivän ajan ja sen jälkeen annokset 20 mg / vrk, mahdollistaa vakaa tila heti toisen annoksen jälkeen useimmissa tapauksissa (noin 76%)vakaa tila, käyrän alla oleva alue ja eliminaation puoliintumisaika ovat samankaltaisia kuin 20 mg / vrk -hoidolla saavutetut.
Aineenvaihdunta ja eliminaatio
Piroksikaami metaboloituu suurelta osin elimistössä, ja alle 5% vuorokausiannoksesta erittyy muuttumattomana ulosteeseen ja virtsaan.
Piroksikaamin metabolia välittyy pääasiassa maksassa sytokromi P450 -isoentsyymi CYP 2C9: n kautta. Tärkeä metaboliareitti on sivuketjun pyridiinirenkaan hydroksylaatio, jota seuraa konjugaatio glukuronihapon kanssa ja eliminaatio virtsateitä pitkin. Plasman puoliintumisaika ihmisellä on noin 50 tuntia.
Potilaille, joilla tiedetään tai epäillään olevan CYP2C9: n metabolisen aktiivisuuden heikkeneminen historian / aiemman kokemuksen perusteella muista CYP2C9 -substraateista, on annettava piroksikaamia varoen, koska heillä voi olla liian suuria pitoisuuksia plasmassa heikentyneen metabolisen puhdistuman vuoksi.
Farmakogenetiikka
CYP2C9 -aktiivisuus on vähentynyt yksilöillä, joilla on geneettisiä polymorfismeja, kuten CYP2C9 * 2- ja CYP2C9 * 3 -polymorfismeja. Rajoitetut tiedot kahdesta julkaistusta raportista osoittivat, että koehenkilöt, joilla oli CYP2C9 * 1 / * 2 -heterotsygoottisia genotyyppejä (n = 9), heterotsygoottisia CYP2C9 * 1 / * 3 (n = 9) ja homotsygoottinen CYP2C9 * 3 / * 3 (n = 1) osoittivat systeemisiä piroksikaamipitoisuuksia 1,7, 1,7 ja 5 kertaa korkeammat kuin potilailla, joiden genotyyppi CYP2C9 * 1 / * 1 (n = 17, normaalin metaboloijan genotyyppi) yhden suun kautta annettavan annoksen jälkeen. 1) olivat 1,7 ja 8,8 kertaa korkeammat kuin CYP2C9 * 1 / * 1 -genotyypin potilailla (n = 17). Homotsygoottisen * 3 / * 3 -genotyypin esiintymistiheyden arvioidaan vaihtelevan 0%: sta 5,7%: iin eri etnisissä ryhmissä (ks. Kohta 4.4).
05.3 Prekliiniset tiedot turvallisuudesta
Farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta, genotoksisuutta, karsinogeenisuutta ja lisääntymistoksisuutta koskevien tavanomaisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
Kuten muutkin prostaglandiinisynteesiä estävät aineet, piroksikaami lisää myös dystocian ja synnytyksen jälkeisten eläinten ilmaantuvuutta eläimillä, kun lääke jatkuu tiineyden aikana. raskauden viimeisen kolmanneksen aikana mahalaukun ja pohjukaissuolen toksisuus lisääntyy.
Ei-kliinisissä tutkimuksissa havaittiin joitakin vaikutuksia, kuten maha-suolikanavan vaurioita ja munuaisten papillaarista nekroosia, jotka havaittiin käytetyllä enimmäisannoksella, joka on noin 60 kertaa suurempi kuin ihmisille ilmoitettu annos.
Tämän vuoksi altistumista piroksikaamille pidetään riittävän suurena ihmisten enimmäisaltistusta suurempana, mikä osoittaa näiden vaikutusten vähäistä merkitystä lääkkeen kliinisessä käytössä.
Prekliinisistä tiedoista ei ole muita lisätietoja kuin ne, jotka on jo ilmoitettu muualla tässä valmisteyhteenvedossa (ks. Kohta 4.6).
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
20 mg kovat kapselit: maissitärkkelys, laktoosi, magnesiumstearaatti, natriumlauryylisulfaatti.
Sisältää kapselin gelatiini, titaanidioksidi (E171).
20 mg liukoisia tabletteja: laktoosi, mikrokiteinen selluloosa, hydroksipropyyliselluloosa, natriumstearyylifumaraatti.
20 mg peräpuikot: puolisynteettiset glyseridit, mikrokiteinen vaha, propyyligallaatti.
06.2 Yhteensopimattomuus
Ei oleellinen.
06.3 Voimassaoloaika
20 mg kovat kapselit: 3 vuotta.
20 mg liukoiset tabletit: 3 vuotta.
20 mg peräpuikot: 3 vuotta.
06.4 Säilytys
20 mg kovat kapselit ja 20 mg liukoiset tabletit: Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
20 mg peräpuikot: Säilytä alle 25 ° C: n lämpötilassa.
06.5 Välipakkauksen luonne ja pakkauksen sisältö
FELDENE 20 mg kovat kapselit - 30 kapselia: PVC- ja raaka -alumiiniläpipainopakkaukset
FELDENE 20 mg liukoiset tabletit - 30 tablettia: PVC- ja raaka -alumiiniläpipainopakkaus
FELDENE 20 mg peräpuikot - 10 peräpuikkoa: PVC / PE -läpipainopakkaukset
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet
Käyttämätön lääke ja tästä lääkkeestä peräisin oleva jäte on hävitettävä paikallisten määräysten mukaisesti.
07.0 MYYNTILUVAN HALTIJA
PFIZER ITALIA S.r.l.
Via Isonzo, 71 - 04100 Latina
08.0 MYYNTILUVAN NUMERO
FELDENE 20 mg kovat kapselit - 30 kapselia: n. 024249029
FELDENE 20 mg liukoiset tabletit - 30 tablettia: n. 024249056
FELDENE 20 mg peräpuikot - 10 peräpuikkoa: n. 024249031
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
FELDENE 20 mg kovat kapselit - 30 kapselia: 16. toukokuuta 1983 / 31. toukokuuta 2010
FELDENE 20 mg liukoiset tabletit - 30 tablettia: 20. elokuuta 1985/31. Toukokuuta 2010
FELDENE 20 mg peräpuikot - 10 peräpuikkoa: 26. kesäkuuta 1982 / 31. toukokuuta 2010
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
4. maaliskuuta 2015.