Vaikuttavat aineet: Bimatoprost
LUMIGAN 0,1 mg / ml silmätipat, liuos
Lumigan -pakkausselosteita on saatavana seuraaville pakkauskokoille:- LUMIGAN 0,1 mg / ml silmätipat, liuos
- LUMIGAN 0,3 mg / ml silmätipat, liuos
Miksi Lumigania käytetään? Mitä varten se on?
LUMIGAN on glaukoomalääke. Se kuuluu prostamideiksi kutsuttujen lääkkeiden luokkaan.
LUMIGAN -silmätippoja käytetään kohonneen silmänpaineen alentamiseen. Tätä lääkettä voidaan käyttää yksinään tai yhdessä muiden silmätippojen kanssa, joita kutsutaan beetasalpaajiksi, jotka myös vähentävät silmänpainetta.
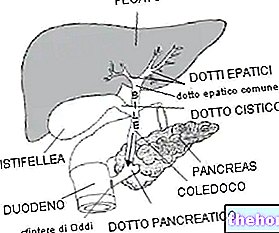
Silmä sisältää kirkasta, vesipohjaista nestettä, joka ravitsee sen sisäosaa. Tämä neste poistuu jatkuvasti silmästä ja uusi neste korvataan poistetulla. Jos nestettä ei puhdisteta riittävän nopeasti, silmän sisällä oleva paine nousee. Tämä lääke lisää erittyvän nesteen määrää ja vähentää siten silmänpainetta. Kohonnut silmänpaine, jos sitä ei lasketa, voi aiheuttaa glaukooma -nimisen sairauden ja voi lopulta aiheuttaa näkövaurioita.
Vasta -aiheet Kun Lumigania ei tule käyttää
Älä käytä LUMIGAN 0,1 mg / ml -valmistetta
- jos olet allerginen (yliherkkä) bimatoprostille tai LUMIGANin jollekin muulle aineelle.
- jos olet joutunut lopettamaan silmätippojen käytön aiemmin säilöntäaineen bentsalkoniumkloridin haittavaikutuksen vuoksi.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Lumigania
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin käytät LUMIGAN 0,1 mg / ml -valmistetta.
Ota yhteys lääkäriisi, jos:
- kärsivät hengitysvaikeuksista
- sinulla on maksa- tai munuaisongelmia
- on leikattu aikaisemmin kaihiin
- kärsivät kuivista silmistä
- sinulla on tai on ollut sarveiskalvon ongelmia (silmän kirkas etuosa)
- käytä piilolinssejä (katso "Tärkeää tietoa LUMIGAN 0,1 mg / ml: n aineosista")
- sinulla on tai on ollut hypotensio tai bradykardia
- sinulla on ollut "virusinfektio tai" silmätulehdus.
LUMIGAN voi aiheuttaa ripsien tummumista ja pidentymistä, se voi myös tummentaa silmäluomia. Ajan myötä myös iiriksen väri voi tummua.Nämä muutokset voivat olla pysyviä ja näkyvämpiä, jos vain yhtä silmiä hoidetaan.
Lapset ja nuoret
LUMIGANia ei ole testattu alle 18 -vuotiailla potilailla, joten sitä ei tule käyttää alle 18 -vuotiailla potilailla.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Lumiganin vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
LUMIGAN voi erittyä rintamaitoon, joten on suositeltavaa olla imettämättä LUMIGAN -hoidon aikana.
Ajaminen ja koneiden käyttö
LUMIGANin antamisen jälkeen voi esiintyä lievää ohimenevää visuaalista sameutta.
Tässä tapauksessa älä aja tai käytä koneita, ennen kuin näkösi on jälleen selvä.
Tärkeää tietoa LUMIGAN 0,1 mg / ml -valmisteen sisältämistä aineista
Älä käytä pisaroita piilolinssien käytön aikana. Silmätippojen antamisen jälkeen odota 15 minuuttia ennen kuin laitat piilolinssit takaisin. LUMIGANin säilöntäaine, nimeltään bentsalkoniumkloridi, voi aiheuttaa silmien ärsytystä ja värjätä pehmeät piilolinssit.
Annostus ja käyttötapa Lumiganin käyttö: Annostus
Käytä tätä lääkettä juuri siten kuin lääkäri tai apteekki on määrännyt. Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
LUMIGANia saa antaa vain silmiin. Suositeltu annos on yksi tippa LUMIGANia kerran päivässä, illalla, kumpaankin hoidettavaan silmään.
Jos käytät LUMIGANia toisen silmälääkkeen kanssa, levitä ensin LUMIGAN -silmätipat ja odota 5 minuuttia ennen toisen silmälääkkeen käyttöä.
Älä käytä sitä useammin kuin kerran päivässä, koska hoidon tehokkuus voi heikentyä.
Käyttöohjeet:
Älä käytä pulloa, jos korkin takin tiiviste ei ole ehjä ennen käyttöä.
- Pese kätesi. Laitat pään taakse ja katsot ylös.
- Vedä alaluomea hitaasti alas muodostaaksesi pienen taskun.
- Käännä pullo ylösalaisin ja paina kevyesti, jotta yksi tippa silmätippoja vapautuu kutakin käsiteltävää silmää kohden.
- Päästä alaspäin ja sulje silmä 30 sekunniksi.
Pyyhi pois kaikki ylimääräinen, joka valuu poskeltasi.
Jos tippa ei pääse silmään, toista toimenpide.
Tulehdusten ja silmävammojen välttämiseksi pullon kärki ei saa koskea silmään tai joutua kosketuksiin muiden pintojen kanssa. Sulje pullo tiiviisti ruiskuttamalla korkki takaisin käytön jälkeen.
Jos unohdat käyttää LUMIGAN 0,1 mg / ml -valmistetta
Jos unohdat käyttää LUMIGANia, tiputa vain yksi tippa heti kun muistat, ja palaa sitten normaaliin annosteluaikaasi. Älä ota kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos lopetat LUMIGAN 0,1 mg / ml -valmisteen käytön
Jotta se toimisi oikein, LUMIGANia on käytettävä joka päivä. Jos lopetat LUMIGANin käytön, silmäsi voi nousta, joten keskustele lääkärisi kanssa ennen tämän hoidon lopettamista.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Lumigania
Jos käytät enemmän LUMIGANia kuin sinun pitäisi, tämä ei todennäköisesti aiheuta vakavia seurauksia. Ota seuraava annos tavalliseen aikaan. Jos tämä huolestuttaa sinua, ota yhteys lääkäriisi tai apteekkiin.
Sivuvaikutukset Mitkä ovat Lumiganin sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa.
Hyvin yleiset haittavaikutukset
Näitä vaikutuksia voi esiintyä yhdellä tai useammalla potilaalla 10: stä.
Vaikutukset silmiin
- Lievä punoitus (jopa 29% ihmisistä)
Yleiset haittavaikutukset
Näitä vaikutuksia voi esiintyä 1–9 potilaalla sadasta.
Vaikutukset silmiin
- Pienet haavaumat silmän pinnalla, tulehduksen kanssa tai ilman
- Ärsytys
- Kutisevat silmät
- Ripsien pidennykset
- Ärsytys, kun tippaa annetaan silmille
- Silmäkipu
Haittavaikutukset iholla
- Punaiset kutiavat silmäluomet
- Silmän ympärillä olevan ihon ruskeantuminen
- Hiusten kasvu silmän ympärillä
Melko harvinaiset haittavaikutukset
Näitä vaikutuksia voi esiintyä 1–9 potilaalla tuhannesta.
Silmän kustannuksella
- Iiriksen värin tummuminen
- Väsyneet silmät
- Silmän pinnan turvotus
- Näön hämärtyminen
- Ripsien menetys
Ihon kustannuksella
- Kuivuus
- Kuorinta silmäluomen reunalla
- Silmäluomen turvotus
- Kutina Vaikuttaa kehoon
- Päänsärky
- Ei voi hyvin
Sivuvaikutukset, joiden esiintymistiheyttä ei tunneta
Silmän kustannuksella
- Makulaarinen turvotus (verkkokalvon turvotus silmän takaosassa, mikä voi johtaa näön huononemiseen)
- Silmäluomien tummuminen
- Syvälle painuneet silmät
- Kuivat silmät Kehon vaikutukset
- Astma
- Astman paheneminen
- Krooniseen obstruktiiviseen keuhkosairauteen (COPD) kutsutun keuhkosairauden paheneminen
- Hengenahdistus
- Allergisen reaktion oireet (turvotus, punasilmäisyys ja ihottuma)
LUMIGAN 0,1 mg / ml: n sivuvaikutusten lisäksi seuraavia haittavaikutuksia on havaittu toisella lääkkeellä, joka sisältää korkeampaa bimatoprostipitoisuutta (0,3 mg / ml):
- Huimaus
- Silmien polttaminen
- Allerginen reaktio silmään
- Tulehtuneet silmäluomet
- Vaikea nähdä teräviä kuvia
- Näön paheneminen
- Silmän pintaa peittävän läpinäkyvän kerroksen turvotus
- Vieraan kehon tunne silmässä
- Herkkyys valolle
- Repiminen
- Tahmeat silmät
- Tummemmat ripset
- Verkkokalvon verenvuoto
- Tulehdus silmän sisällä
- Kystinen makulaedeema (silmän verkkokalvon turvotus, joka johtaa näön huononemiseen)
- Silmäluomien kouristukset
- Silmäluomen kaventuminen, siirtyminen pois silmän pinnasta
- Silmän ympärillä olevan ihon punoitus
- Kohonnut verenpainearvot
- Heikkous
- Maksan toiminta -arvojen nousu verikokeissa
Muita fosfaatteja sisältävien silmätippojen sivuvaikutuksia.
Hyvin harvinaisissa tapauksissa joillakin potilailla, joilla on vakava vaurio silmän etuosan kirkkaassa kerroksessa (sarveiskalvo), on kehittynyt läpinäkymättömiä alueita sarveiskalvoon kalsiumin kertymisen vuoksi hoidon aikana.
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan liitteessä V luetellun kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkkeen turvallisuudesta.
Vanhentuminen ja säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pullon etiketissä ja pakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Hävitä pullo viimeistään 4 viikon kuluttua ensimmäisestä avaamisesta, vaikka siinä olisi vielä tippaa. Tämä välttää infektiot. Muista muistiin kirjoittamalla laatikon ensimmäiseen avaamispäivämäärä.
Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Määräaika "> Muut tiedot
Mitä LUMIGAN 0,1 mg / ml sisältää
- Vaikuttava aine on bimatoprosti. Yksi ml liuosta sisältää 0,1 mg bimatoprostia.
- Muut aineet ovat bentsalkoniumkloridi (säilöntäaine), natriumkloridi, natriumfosfaattiemäsheptahydraatti, sitruunahappomonohydraatti ja puhdistettu vesi. Pieniä määriä suolahappoa tai natriumhydroksidia voidaan lisätä normaalin happamuuden (pH) ylläpitämiseksi.
Kuvaus LUMIGAN 0,1 mg / ml -valmisteen ulkonäöstä ja pakkauksen sisällöstä
LUMIGAN on kirkas, väritön silmätippu, joka toimitetaan pakkauksessa, joka sisältää 1 muovipullon tai 3 muovipulloa, joissa on kierrekorkki.
Jokainen pullo on noin puoliksi täynnä ja sisältää 3 millilitraa liuosta, joka riittää 4 viikon käyttöön.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI -
LUMIGAN 0,1 MG / ML SILMÄTILAT, Liuos
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS -
1 ml liuosta sisältää 0,1 mg bimatoprostia.
Apuaine, jonka vaikutukset tunnetaan:
Yksi ml liuosta sisältää 0,2 mg bentsalkoniumkloridia.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO -
Silmätipat, liuos.
Väritön liuos.
04.0 KLIINISET TIEDOT -
04.1 Käyttöaiheet -
Kohonnut silmänsisäisen paineen alentaminen kroonisen avoimen kulman glaukooman ja silmän verenpaineen hoidossa aikuisilla (monoterapiana tai beetasalpaajien lisähoitona).
04.2 Annostus ja antotapa -
Annostus
Suositeltu annos on yksi tippa sairaaseen silmään kerran päivässä, ja se annetaan illalla.
Pediatriset potilaat
LUMIGANin turvallisuutta ja tehoa 0-18 -vuotiaiden lasten hoidossa ei ole vielä varmistettu.
Potilaat, joilla on maksan ja munuaisten vajaatoiminta:
LUMIGANia ei ole tutkittu potilailla, joilla on munuaisten vajaatoiminta tai kohtalainen tai vaikea maksan vajaatoiminta, joten sitä tulee käyttää varoen näille potilaille. Potilailla, joilla on ollut lievä maksan vajaatoiminta tai alaniiniaminotransferaasi (ALAT), aspartaattiaminotransferaasi (ASAT) ja / tai epänormaali bilirubiini hoidon alussa, bimatoprostin 0,3 mg / ml silmätipat, liuoksella ei ollut haitallisia vaikutuksia maksan toimintaan 24 kuukauden hoidosta.
Antotapa
Jos käytetään useita paikallisia silmälääkkeitä, jokainen lääke on annettava vähintään 5 minuutin välein.
04.3 Vasta -aiheet -
Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
LUMIGAN 0,1 mg / ml on vasta -aiheinen potilaille, joilla on aiemmin esiintynyt epäilty haittavaikutus bentsalkoniumkloridiin, mikä johti hoidon lopettamiseen.
04.4 Varoitukset ja käyttöön liittyvät varotoimet -
Okulaarit
Ennen hoidon aloittamista potilaille on kerrottava mahdollisuudesta ripsien pidentymiseen, silmäluomien tummumiseen ja iiriksen pigmentaation lisääntymiseen, koska nämä reaktiot on havaittu LUMIGAN -hoidon aikana. Jotkut näistä muutoksista voivat olla pysyviä ja voivat aiheuttaa eroja kahden silmän ulkonäössä, kun vain yhtä silmää hoidetaan. Iiriksen pigmentin lisääntyminen on todennäköisesti pysyvää.Pigmentaation muutos johtuu pikemminkin melanosyyttien melaniinipitoisuuden noususta kuin melanosyyttien määrän lisääntymisestä.Iiriksen pigmentin lisääntymisen pitkäaikaisia vaikutuksia ei tunneta. Iiriksen värin muutokset, joita on havaittu bimatoprostin oftalmologisen annon jälkeen, eivät ehkä ole näkyvissä useita kuukausia tai vuosia. Ruskea pigmentaatio oppilaan ympärillä laajenee yleensä samankeskisesti kohti iiriksen kehää ja silmän kaikkia osia. Iiris saa ruskehtavan värin. hoidolla ei ole vaikutusta iiriksen neveliin tai areooloihin. 12 kuukauden iiriksen hyperpigmentaation ilmaantuvuus bimatoprostin 0,1 mg / ml silmätippojen liuoksella oli 0,5%. 12 kuukauden kuluttua bimatoprost 0,3 mg / ml silmätippojen, liuoksen, esiintyvyys oli 1,5% (ks. Kohta 4.8, taulukko) 2) eikä lisääntynyt seuraavien 3 hoitovuoden aikana. Joillakin potilailla on raportoitu periorbitaalisen kudoksen pigmentin palautumista.
Kystinen makulaturvotus on raportoitu melko harvoin (≥ 1/1 000, makulaturvotus (esim. Afaakiset, pseudofaakiset potilaat, joilla on posteriorinen linssikapselin repeämä).
Bimatoprost 0,3 mg / ml silmätippojen liuoksella on harvoin raportoitu spontaanisti aiempien sarveiskalvon tunkeutumisten tai silmäinfektioiden aktivoitumisesta. LUMIGANia tulee käyttää varoen potilailla, joilla on aiemmin ollut merkittäviä virusinfektioita (esim. Herpes simplex) tai uveiitti / iriitti.
LUMIGANia ei ole tutkittu potilailla, joilla on tulehduksellinen silmäsairaus, neovaskulaarinen, tulehduksellinen, kapeakulmainen glaukooma, synnynnäinen glaukooma tai akuutti kulma glaukooma.
Ihon
Hiusten kasvua voi esiintyä alueilla, joilla LUMIGAN -liuos joutuu toistuvasti kosketuksiin ihon pinnan kanssa. Siksi on tärkeää levittää LUMIGANia ohjeiden mukaisesti ja välttää sen kulkeutumista poskelle tai muille ihoalueille.
Hengitys
LUMIGANia ei ole tutkittu potilailla, joilla on heikentynyt hengitystoiminta. Vaikka potilaista, joilla on aiemmin ollut astma tai keuhkoahtaumatauti, on saatavilla vain vähän tietoa, astman pahenemista, hengenahdistusta ja keuhkoahtaumatautia sekä astman tapauksia on raportoitu markkinoille tulon jälkeen. Näiden oireiden esiintymistiheyttä ei tunneta. Potilaita, joilla on keuhkoahtaumatauti, astma tai muiden sairauksien vuoksi heikentynyt hengitystoiminta, tulee hoitaa varoen.
Sydän ja verisuonisto
LUMIGANia ei ole tutkittu potilailla, joilla on yli asteen 1 sydämen lohko tai hallitsematon kongestiivinen sydämen vajaatoiminta. Bimatoprost 0,3 mg / ml silmätippojen liuoksella on raportoitu rajoitettu määrä spontaaneja raportteja bradykardiasta tai hypotensiosta. LUMIGANia tulee käyttää varoen potilailla, joilla on taipumus bradykardiaan tai hypotensioon.
Muita tietoja
Bimatoprost 0,3 mg / ml -tutkimuksissa glaukoomaa tai okulaarista hypertensiota sairastavilla potilailla osoitettiin, että useamman silmän altistuminen useammalle kuin yhdelle bimatoprostiannokselle päivässä voi heikentää silmänpainetta alentavaa vaikutusta (ks. Kohta 4.5) LUMIGANia yhdessä käyttävät potilaat muiden prostaglandiinianalogien kanssa on seurattava silmänpaineen muutosten varalta.
LUMIGAN 0,1 mg / ml sisältää säilöntäaineena bentsalkoniumkloridia (200 ppm), jonka pehmeät piilolinssit voivat imeä. Bentsalkoniumkloridin läsnäolon vuoksi voi esiintyä myös silmien ärsytystä ja pehmeiden piilolinssien värimuutoksia. Piilolinssit on poistettava ennen tiputusta ja asetettava uudelleen 15 minuutin kuluttua annostelusta.
Bentsalkoniumkloridin, jota käytetään yleisesti säilöntäaineena silmälääkkeissä, on raportoitu aiheuttavan täsmällistä keratopatiaa ja / tai toksista haavaista keratopatiaa. Koska LUMIGAN 0,1 mg / ml sisältää 200 ppm bentsalkoniumkloridia (neljä kertaa bimatoprostin 0,3 mg / ml silmätippojen pitoisuus), sitä tulee käyttää varoen potilailla, joilla on kuiva silmä tai joiden sarveiskalvo voi olla heikentynyt, ja potilailla, jotka käyttävät erilaisia silmiä pisarat, jotka sisältävät bentsalkoniumkloridia. Lisäksi näiden potilaiden kliininen seuranta on tarpeen, jos lääkettä käytetään pitkään.
Bakteeri -keratiittitapauksia on raportoitu paikallisten silmälääkkeiden moniannosastioiden käytön yhteydessä. Nämä säiliöt ovat vahingossa saastuneet potilailta, joilla on useimmissa tapauksissa ollut samanaikainen silmäsairaus. Potilaat, joilla on silmän epiteelin pinnan hajoaminen, ovat suuremmassa vaarassa bakteeri -keratiitin saamiseksi.
Kehota potilaita estämään annostelusäiliön kärki joutumasta silmään tai ympäröiviin rakenteisiin, jotta vältetään silmävammat ja liuoksen saastuminen.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset -
Yhteisvaikutustutkimuksia ei ole tehty.
Yhteisvaikutuksia ei ole odotettavissa ihmisillä, koska bimatoprostin 0,3 mg / ml silmätippojen liuoksen silmään antamisen jälkeen bimatoprostin systeemiset pitoisuudet ovat erittäin pienet (alle 0,2 ng / ml). vaikutuksia lääkeaineenvaihdunnasta vastaaviin maksaentsyymeihin ei havaittu.
Kliinisissä tutkimuksissa bimatoprostia 0,3 mg / ml, silmätippoja, liuosta käytettiin samanaikaisesti useiden beetasalpaajien silmälääkkeiden kanssa ilman yhteisvaikutuksia.
LUMIGANia ei ole arvioitu lisä glaukoomalääkityksessä muiden aineiden kuin paikallisten beetasalpaajien kanssa.
Prostaglandiinianalogien (esim. LUMIGAN) silmänpainetta alentava vaikutus voi olla heikompi potilailla, joilla on glaukooma tai silmänpaine, kun niitä käytetään yhdessä muiden prostaglandiinianalogien kanssa (ks. Kohta 4.4).
04.6 Raskaus ja imetys -
Raskaus
Bimatoprostin käytöstä raskaana olevilla naisilla ei ole riittävästi tietoa Eläinkokeet ovat osoittaneet lisääntymistoksisuutta suurilla äidille myrkyllisillä annoksilla (ks. Kohta 5.3).
LUMIGANia ei tule käyttää raskauden aikana paitsi ehdottoman välttämättömissä tapauksissa.
Ruokinta-aika
Ei tiedetä, erittyykö bimatoprosti äidinmaitoon. Eläinkokeet ovat osoittaneet, että bimatoprosti erittyy äidinmaitoon.On päätettävä, lopetetaanko imetys vai lopetetaanko LUMIGAN-hoito ottaen huomioon imetyksen hyödyt lapselle ja hoidon hyödyt naiselle.
Hedelmällisyys
Bimatoprostin vaikutuksista ihmisen hedelmällisyyteen ei ole tietoja.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn -
LUMIGANilla on vähäinen vaikutus ajokykyyn ja koneiden käyttökykyyn. Kuten muidenkin silmälääkkeiden kohdalla, jos tippojen annostelussa ilmenee ohimenevää näön hämärtymistä, potilaan on odotettava ennen ajamista tai koneiden käyttöä.
04.8 Haittavaikutukset -
12 kuukautta kestäneessä vaiheen III kliinisessä tutkimuksessa noin 38% LUMIGAN 0,1 mg / ml silmätippoja, liuosta saaneista potilaista koki haittavaikutuksia. Yleisimmin raportoitu haittavaikutus oli sidekalvon hyperemia (pääasiassa hyvin lievä tai lievä ja luultavasti ei-tulehduksellinen), jota esiintyi 29%: lla potilaista. Kaikki "noin 4% potilaista keskeytti hoidon haittatapahtuman vuoksi 12 kuukauden tutkimus.
Seuraavia haittavaikutuksia on raportoitu kliinisissä tutkimuksissa, joissa on käytetty LUMIGAN 0,1 mg / ml silmätippoja, liuosta tai markkinoille tulon jälkeen. Useimmat niistä olivat lieviä silmään kohdistuvia vaikutuksia, eikä yksikään niistä ollut vakavia.
Hyvin yleinen (≥1 / 10); yleinen (≥ 1/100,
Pöytä 1.
Kliinisissä tutkimuksissa yli 1800 potilasta sai LUMIGAN 0,3 mg / ml -hoitoa. Kun yhdistetään vaiheen III monoterapia ja lisätiedot LUMIGAN 0,3 mg / ml: n kanssa, yleisimpiä haittavaikutuksia ovat:
• ripsien kasvu jopa 45% ensimmäisenä vuonna, uusien tapausten ilmaantuvuus väheni 7%: iin 2 vuoden kuluttua ja 2%: iin 3 vuoden kuluttua
• sidekalvon hyperemia (pääasiassa erittäin lievästä lievään ja luultavasti ei-tulehdukselliseen) jopa 44% ensimmäisen vuoden aikana, ja uusien tapausten ilmaantuvuus väheni 13%: iin 2 vuoden kuluttua ja 12%: iin 3 vuoden kuluttua
• silmän kutina jopa 14%: lla potilaista ensimmäisenä vuonna, ja ilmaantuvuus laskee 3%: iin 2 vuoden kuluttua ja 0%: iin 3 vuoden kuluttua. Alle 9% potilaista joutui lopettamaan hoidon haittavaikutusten vuoksi ensimmäisenä vuonna, ja uusien potilaiden ilmaantuvuus oli 3% hoidon lopettamisesta 2 ja 3 vuoden aikana.
Taulukossa 2 raportoidaan muita haittavaikutuksia, joita havaittiin LUMIGAN 0,3 mg / ml: n käytön yhteydessä. Taulukko sisältää myös haittavaikutuksia, joita ilmeni molempien valmisteiden kanssa, mutta eri esiintymistiheydellä. Useimmat niistä olivat lieviä tai kohtalaisia silmään kohdistuvia vaikutuksia, eikä yksikään niistä ollut vakavia.
Haittavaikutukset ilmoitetaan kussakin yleisyysluokassa vakavuuden mukaan alenevassa järjestyksessä.
Taulukko 2.
Haittavaikutukset, joita on raportoitu fosfaattia sisältävillä silmätipoilla:
Fosfaattia sisältävien silmätippojen käyttöön liittyviä sarveiskalvon kalkkeutumistapauksia on raportoitu hyvin harvoin joillakin potilailla, joilla sarveiskalvo on vakavasti heikentynyt.
Epäillyistä haittavaikutuksista ilmoittaminen
Ilmoittaminen epäillyistä haittavaikutuksista, jotka ilmenevät lääkkeen myyntiluvan myöntämisen jälkeen, on tärkeä, koska se mahdollistaa lääkkeen hyöty -haitta -tasapainon jatkuvan seurannan Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta.
04.9 Yliannostus -
Yliannostustapauksia ei ole raportoitu, ja niitä ei todennäköisesti esiinny silmälääkkeiden käytön yhteydessä.
Yliannostustapauksessa hoidon tulee olla oireenmukaista ja tukevaa. Jos LUMIGANia niellään vahingossa, voi olla hyödyllistä tietää, että: Kahden viikon tutkimuksissa rotilla ja hiirillä havaittiin, että enintään 100 mg / kg / vrk oraalinen anto ei aiheuttanut mitään toksisuutta. Tämä annos (mg / m²) on vähintään 210 kertaa suurempi kuin LUMIGAN 0,1 mg / ml silmätippojen pullon sisältämä annos vahingossa 10 kg painavalle lapselle.
05.0 FARMAKOLOGISET OMINAISUUDET -
05,1 "Farmakodynaamiset ominaisuudet -
Farmakoterapeuttinen ryhmä: silmälääkkeet, prostaglandiinianalogit, ATC -koodi: S01EE03
Toimintamekanismi
Vaikutusmekanismi, jolla bimatoprosti alentaa silmänsisäistä painetta ihmisellä, ilmaistaan lisäämällä sekä trabekulaarisen että uveo-skleraalisen vesihöyryn ulosvirtausta. Silmänsisäisen paineen lasku alkaa noin 4 tuntia ensimmäisen annoksen jälkeen, suurin vaikutus saavutetaan noin 8-12 tunnin kuluessa ja vaikutus kestää vähintään 24 tuntia.
Bimatoprost on voimakas silmän verenpainetta alentava aine. Se on synteettinen prostamidi, joka on rakenteellisesti sukua prostaglandiini F2α: lle (PGF2α), mutta joka ei toimi minkään tunnetun prostaglandiinireseptorin kautta. Bimatoprost jäljittelee valikoivasti äskettäin löydettyjen biosynteettisten aineiden, nimeltään prostamidit, vaikutuksia. Prostamidaalista reseptoria ei kuitenkaan ole vielä rakenteellisesti tunnistettu.
LUMIGAN 0,1 mg / ml -silmätippoja saaneilla aikuisilla tehdyssä 12 kuukautta kestäneessä keskeisessä tutkimuksessa keskimääräiset vuorokautiset silmänpainearvot erosivat kullakin käynnillä 12 kuukauden tutkimusjakson aikana enintään 1,1 mmHg. päivä eikä koskaan ylittänyt 17,7 mmHg.
LUMIGAN 0,1 mg / ml silmätipat sisältävät bentsalkoniumkloridia pitoisuutena 200 ppm.
LUMIGANin käytöstä on rajallista kokemusta potilailla, joilla on pseudoeksfoliatiivinen ja pigmentaalinen kulma-avoin glaukooma ja krooninen suljettu kulma-glaukooma, jossa on patentoitu iridotomia.
Kliinisissä tutkimuksissa ei havaittu kliinisesti merkittäviä vaikutuksia sykkeeseen ja verenpaineeseen.
Pediatriset potilaat
LUMIGANin turvallisuutta ja tehoa 0-18 -vuotiaiden lasten hoidossa ei ole varmistettu.
05,2 "Farmakokineettiset ominaisuudet -
Imeytyminen
In vitro bimatoprosti tunkeutuu hyvin ihmisen sarveiskalvoon ja skleraan. Aikuisten silmään antamisen jälkeen systeeminen altistus bimatoprostille on hyvin vähäinen ilman kertymisilmiöitä ajan myötä. Kun yksi tippa bimatoprostia 0,3 mg / ml on annettu päivittäin molempiin silmiin kahden viikon ajan, veren pitoisuus saavutti huippunsa 10 minuuttia tiputuksen jälkeen ja laski alle havaitsemisrajan (0,025 ng / ml) 1,5 tunnin kuluessa annostelusta. Keskimääräiset Cmax-arvot ja AUC 0-24hrs -arvot olivat samanlaisia päivänä 7 ja 14 ja olivat vastaavasti noin 0,08 ng / ml ja 0,09 ng • h / ml; nämä arvot osoittavat, että bimatoprostin vakaa pitoisuus saavutettiin ensimmäisen silmäviikon aikana.
Jakelu
Bimatoprost jakautuu kohtalaisesti kehon kudoksiin ja systeeminen jakautumistilavuus ihmisillä on vakaan tilan ollessa 0,67 l / kg. Ihmisen veressä bimatoprostia esiintyy pääasiassa plasmassa. Bimatoprostin sitoutuminen plasman proteiineihin on noin 88%.
Biotransformaatio
Silmään annon jälkeen bimatoprosti on tärkein veressä kiertävä aine, kun systeeminen verenkierto saavutetaan. Bimatoprost, joka sitten hapetetaan, N-deetyloidaan ja glukuronidoidaan, muodostaa erilaisia metaboliitteja.
Eliminaatio
Bimatoprosti eliminoituu pääasiassa munuaisten kautta, jopa 67% terveille vapaaehtoisille annetusta laskimonsisäisestä annoksesta erittyi virtsaan, 25% annoksesta erittyi ulosteiden kautta. Eliminaation puoliintumisaika laskimonsisäisen annon jälkeen määritettynä oli noin 45 minuuttia; veren kokonaispuhdistuma oli 1,5 l / h / kg.
Ominaisuudet iäkkäillä potilailla
Kahden bimatoprost 0,3 mg / ml silmätippaliuoksen päivittäisen annoksen jälkeen bimatoprostin keskimääräinen AUC0-24h-arvo 0,0634 ng • h / ml iäkkäillä potilailla (65-vuotiaat tai sitä vanhemmat) oli merkittävästi korkeampi verrattuna arvoon 0,0218 ng • h / ml todettu terveillä nuorilla potilailla. Tämä tulos ei kuitenkaan ole kliinisesti tärkeä, koska systeeminen altistus sekä iäkkäillä että nuorilla henkilöillä pysyi hyvin alhaisena silmään annettuna.Bimatoprostin kertymistä vereen ei havaittu ajan myötä, kun taas turvallisuusprofiili oli sama molemmilla iäkkäillä potilailla ja nuoret potilaat.
05.3 Prekliiniset tiedot turvallisuudesta -
Vaikutuksia ei-kliinisissä tutkimuksissa havaittiin vain altistuksilla, joiden katsottiin selvästi ylittävän ihmisen enimmäisaltistuksen, mikä viittaa vähäiseen kliiniseen merkitykseen.
Apinoilla bimatoprostin päivittäinen antaminen silmiin pitoisuuksilla ≥ 0,3 mg / ml yhden vuoden ajan aiheutti iiriksen pigmentin lisääntymistä ja annoksesta riippuvaisia palautuvia periokulaarisia vaikutuksia, joille on tunnusomaista näkyvä ylä- ja / tai alempi sulku ja halkeamia laajentava silmäluomi. Iiriksen pigmentaation lisääntymisen mekanismi näyttää johtuvan melaniinin tuotannon lisääntyneestä stimulaatiosta melanosyyteissä eikä melanosyyttien määrän lisääntymisestä. Perikulaarisiin vaikutuksiin liittyviä toiminnallisia tai mikroskooppisia muutoksia ei ole havaittu ei tunneta, liittyy löydettyihin periokulaarisiin muutoksiin.
Tutkimussarjassa in vitro Ja in vivo bimatoprosti ei ollut perimää vaurioittava tai karsinogeeninen.
Bimatoprosti ei heikentänyt rotan hedelmällisyyttä annoksilla, jotka olivat enintään 0,6 mg / kg / vrk (vähintään 103 kertaa käytetty ihmisannos) .Alkiot / sikiön kehitystutkimuksissa hiirillä ja rotilla havaittiin abortteja, mutta ei kehitysvaikutuksia jotka olivat vähintään 860 tai 1700 kertaa suurempia kuin ihmisille annetut annokset. Nämä annokset johtivat systeemiseen altistukseen, joka oli vähintään 33 tai 97 kertaa suurempi kuin ihmisille osoitettu. 0,3 mg / kg / vrk (vähintään 41 kertaa ihmisille osoitettu). Jälkeläisten neurokäyttäytymistoiminnot eivät olleet mukana.
06.0 FARMASEUTTISET TIEDOT -
06.1 Apuaineet -
Bentsalkoniumkloridi
Natriumkloridia
Kaksiemäksinen natriumfosfaattiheptahydraatti
Sitruunahappomonohydraatti
Kloorivetyhappo tai natriumhydroksidi (pH: n säätämiseen)
Puhdistettua vettä
06.2 Yhteensopimattomuus "-
Ei oleellinen.
06.3 Voimassaoloaika "-
2 vuotta.
4 viikkoa ensimmäisen avaamisen jälkeen.
06.4 Säilytystä koskevat erityiset varotoimet -
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
06.5 Välipakkauksen luonne ja pakkauksen sisältö -
Maitovalkoiset pienitiheyksiset polyeteenipullot, joissa on kierrettävä polystyreenikorkki.
Jokaisen pullon täyttötilavuus on 3 ml.
Seuraavia pakkauskokoja on saatavana: kartonki, joka sisältää 1 tai 3 pulloa 3 ml liuosta.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet -
Ei erityisiä hävitysohjeita.
07.0 "MYYNTILUVAN HALTIJA" -
Allergan Pharmaceuticals Irlanti
Castlebar Road
Westport
Co.Mayo
Irlanti
08.0 MYYNTILUVAN NUMERO -
EU / 1/02/205 / 003-004
035447022
035447034
09.0 MYYNTILUVAN MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ -
7. tammikuuta 2010
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ -
D.CCE tammikuu 2016