" ensimmäinen osa
Krebs -syklin neljännen vaiheen katalysoiva entsyymi on a-ketoglutaraattidehydrogenaasi; tämä entsyymi on entsyymikompleksi, joka on hyvin samanlainen kuin pyruvaattidehydrogenaasi. Molemmat koostuvat 48-60 proteiinista, joissa tunnistetaan kolme erilaista entsymaattista aktiivisuutta, ja niillä on myös samat entsymaattiset kofaktorit; ovat hyvin samankaltaisia entsyymejä, koska ne vaikuttavat samanlaisiin substraatteihin: sekä pyruvaattiin että l "α-keto glutaraatti, ovat α- ketohapot. Kahden entsymaattisen kompleksin vaikutusmekanismi on sama.
Tiamiinipyrofosfaatin hyökkäys karbonyyliin (C = O)α-ketoglutaraatti, johtaa sen dekarboksylaatioon ja muodostuu karboksihydroksipropyylijohdannainen. Kun siirrytään myöhemmin lipoamidiin, tapahtuu sisäinen redoksiprosessi, josta saadaan lipoamidikarboksijohdannainen tai sukkinyylilipamidi.
Sukkinyylilipamidi reagoi sitten koentsyymi A: n kanssa, jolloin saadaan sukkinyylikoentsyymi A (joka jatkuu krebs -syklissä) ja pelkistetty lipoamidi, joka hapetetaan FAD: n avulla: muodostunut FADH2 hapetetaan uudelleen NAD +: lla ja saadaan NADH. Tässä vaiheessa tapahtui siis toinen hiilen poistaminen hiilipitoisesta luuranosta hiilidioksidin muodossa.
Koentsyymiin A liittyvä asyyliryhmä on aktivoidussa muodossa, eli sillä on korkea energiasisältö: siksi on mahdollista hyödyntää sukkinyylikoentsyymi A: n energiaa.

Krebs -syklin viidennessä vaiheessa sukkinyylikoentsyymi A altistetaan sukkinyylitiokinaasi; sen toimintatavasta on esitetty kaksi hypoteesia: kuvaamme vain yhtä kahdesta, koska se on kaikkein akkreditoitu. Tämän hypoteesin mukaan sukkinyylikoentsyymi A hyökkää entsyymin histidiinin (Hys) typellä: koentsyymi A vapautuu ja välituotteena muodostuu histidiinistä johdettu addukti, eli sukkinyyli-entsyymi (tai sukkinyyli-Hys) ortofosfaatti vaikuttaa tähän välituotteeseen, mikä johtaa sukkinaatin vapautumiseen ja fosfentsyymin muodostumiseen.Fosfoentsyymi, jota hyökkää guanosiinidifosfaatti (GDP), tuottaa guasnosiinitrifosfaattia (GTP) ja entsyymi vapautuu. Energian näkökulmasta GTP = ATP: energiaa tuottava sidos on sama molemmilla lajeilla (se on fosforyyli Β: n ja fosforyyli γ: n välinen anhydridisidos). Joissakin tapauksissa GTP: tä käytetään materiaalina, jolla on korkea energiasisältö, mutta yleensä GTP muuttuu ATP: ksi entsyymin vaikutuksesta nukleosididifosfokinaasi (NDPK); on entsyymi, joka löytyy soluista ja katalysoi seuraavan reaktion:
N1TP + N2DP → N1DP + N2TP
Yleinen NiTP ® -nukleosiditrifosfaatti
Yleinen NiDP ® -nukleosididifosfaatti
Se on palautuva reaktio; meidän tapauksessamme tapahtuu:
GTP + ADP → BKT + ATP
siksi se voi edetä oikealle tai vasemmalle, vaikka reagenssien pitoisuudet olisivat pieniä.
Jos krebs -sykli etenee niin nopeasti, että se johtaa ATP: n tuotantoon, joka on suurempi kuin energiatarve, ADP: tä on niukasti saatavilla, kun taas ATP: tä on paljon: nukleosididifosfokinaasin katalysoima reaktio on, vasemmalle (GTP kerääntyy, jos nukleosididifosfokinaasilla ei ole riittävästi substraattia eli ADP: tä). Siksi GTP on signaali energian saatavuudesta ja hidastaa siksi krebs -sykliä.
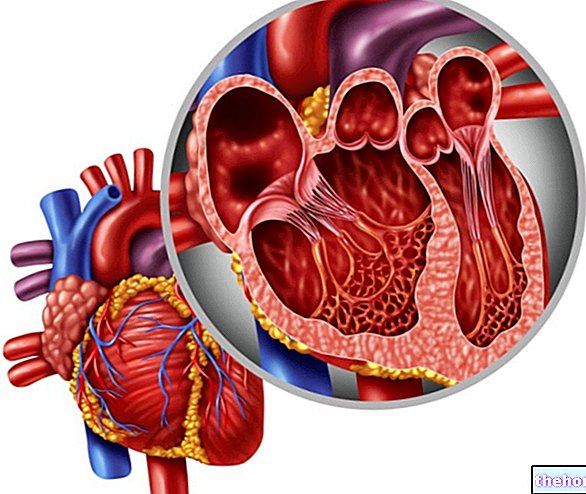
Krebs -syklin kuudes vaihe johtaa fumaraatin muodostumiseen sukkinaattidehydrogenaasi; tämä entsyymi antaa stereospesifisen reaktion, kun tyydyttymätön (se on alkeeni) trans muodostuu aina eli fumaraatti (kun cis -isomeeri on maleaatti). Sukkinaattidehydrogenaasia löytyy mitokondrioiden sisäkalvosta, kun taas kaikki muut krebs -syklin entsyymit ovat hajallaan mitokondrioissa.
Sukkinaattidehydrogenaasilla on FAD kofaktorina; sitä estää oksaloasetaatti (takaisinkytkennän esto), kun sen positiivinen modulaattori (aktivaattori) on sukkinaatti ja fumaraatti. sen aktivaattori. Yritetään ymmärtää miksi, hyppäämällä krebs-syklin viimeiseen vaiheeseen. krebs -sykli vaatii energiaa, joten ainoa mahdollisuus saada oksaloasetaattia potilaalta on, että potilaan pitoisuus on erittäin korkea: malaatti on yksi metaboliiteista, joiden pitoisuus on suurin soluissa. tosiasia, että sitraattisyntaasin vaikutus pitää oksaloasetaattipitoisuuden alhaisena.Sukkinaattidehydrogenaasin katalysoima reaktio on tällöin itsesyöttöreaktio, ja tämä on ainoa tapa saada malaatti muuttumaan oksaloasetaatiksi.
Mitokondriaalimalaatin pitoisuuden on oltava yhteensopiva sytoplasmisen malaatin pitoisuuden kanssa: vain jos mitokondriolalaatin pitoisuus on niin korkea, että se takaa malaatin muuttumisen oksaloasetaatiksi (krebs -syklissä), malaattia voidaan käyttää myös muilla tavoilla (jotka ovat sytoplasmista): sytoplasmassa malaatti voidaan muuttaa oksaloasetaatiksi, josta aspartaattia voidaan saada GOT: n (se on transaminaasi) tai glukoosin vaikutuksesta glukoneogeneesin avulla.
Palaamme Krebs -syklin seitsemänteen vaiheeseen, jota entsyymi katalysoi fumarasi: vettä lisätään stereospesifisellä tavalla L-malaatin valmistamiseksi.
Krebsin syklin viimeisessä vaiheessa, josta olemme jo puhuneet, toiminta malaattidehydrogenaasi. Tämä entsyymi käyttää NAD + -molekyyliä katalyyttiseen toimintaansa.
Olemme siis päättäneet Krebs -syklin eri vaiheiden kuvauksen.
Krebs -sykli on täysin palautuva.
Krebs -syklin nopeuden lisäämiseksi kyseisessä syklissä olevien metaboliittien pitoisuutta voidaan lisätä; yksi strategioista Krebs -syklin nopeuden lisäämiseksi koostuu siitä, että mitokondrioihin tuleva pyruvaatti muutetaan oksaloasetaatiksi (pyruvaattikarboksylaasin vaikutuksesta), eikä sitä muuteta asetyylikoentsyymi A: ksi: tämä lisää oksaloasetaattipitoisuutta on Krebs -syklin metaboliitti ja lisää siten koko syklin nopeutta.
Krebs -syklissä kolme NAD +: a muunnetaan kolmeksi NADH: ksi ja yksi FADH2: ksi ja lisäksi saadaan GTP: n: kanavoimalla krebs -syklistä saatu pelkistysvoima lisää ATP: tä; hengitysketjussa pelkistävä voima siirtyy NADH: sta ja FADH2: sta happiin: tämä siirto johtuu useista entsyymeistä, jotka sijaitsevat mitokondrioiden kalvolla ja jotka omalla toiminnallaan johtavat ATP: n tuotantoon.
Hengitysketjun prosessit ovat eksergonisia prosesseja ja vapautunut energia käytetään ATP: n tuottamiseen; solun tarkoitus on hyödyntää eksergonisia prosesseja ATP: n synteesin aikaansaamiseksi. Jokaista NADH -molekyyliä kohti, joka tulee hengitysketjuun, saadaan 2,5 ATP -molekyyliä ja kullekin FADH2: lle 1,5 ATP -molekyyliä; tämä monimuotoisuus johtuu siitä, että FADH2 tulee hengitysketjuun alemmalla tasolla kuin NADH.
Aerobisen aineenvaihdunnan vähentävällä voimalla saadaan 30-32 ATP: tä (219-233 kcal / mol) noin 33%: n hyötysuhteella (anaerobisen aineenvaihdunnan tehokkuus on noin 2%).