Mikä on Filgrastim Hexal
Filgrastim Hexal on injektio- tai infuusioneste (tiputus laskimoon) esitäytetyssä ruiskussa, joka sisältää vaikuttavaa ainetta filgrastiimia (30 tai 48 miljoonaa yksikköä).
Filgrastim Hexal on biosimilaarinen lääke, mikä tarkoittaa sitä, että se on samanlainen kuin biologinen lääke, joka on jo hyväksytty Euroopan unionissa (EU) ja joka sisältää samaa vaikuttavaa ainetta (kutsutaan myös alkuperäislääkkeeksi). Jos haluat lisätietoja biosimilaarisista lääkkeistä, katso kysymykset ja vastaukset napsauttamalla tätä.
Mihin sitä käytetään
Filgrastim Hexalia käytetään stimuloimaan valkosolujen tuotantoa seuraavissa tilanteissa:
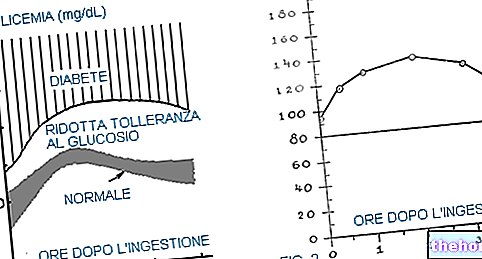
- neutropenian (neutrofiilien alhainen taso, valkosolutyyppi) ja kuumeisen neutropenian (kuumeinen neutropenia) ilmaantuvuuden lyhentämiseksi potilailla, jotka saavat sytotoksista (soluja tuhoavaa) kemoterapiaa (syövän hoito);
- neutropenian keston lyhentäminen potilailla, joita hoidetaan luuytimen solujen tuhoamiseksi ennen luuydinsiirtoa (kuten joillakin leukemiapotilailla), kun heillä on vakavan ja pitkäaikaisen neutropenian riski;
- neutrofiilipitoisuuksien lisääminen ja infektioriskin vähentäminen neutropeniapotilailla, joilla on ollut vakavia ja toistuvia infektioita;
- pysyvän neutropenian hoitoon potilailla, joilla on pitkälle edennyt ihmisen immuunikatovirus (HIV) -infektio, bakteeri -infektioiden riskin vähentämiseksi, kun muut hoidot ovat riittämättömiä.
Filgrastim Hexalia voidaan käyttää myös potilailla, jotka ovat luovuttamassa kantasoluja elinsiirtoa varten näiden solujen vapauttamiseksi luuytimestä.
Lääkettä saa vain reseptillä.
Miten Filgrastim Hexalia käytetään?
Filgrastim Hexal annetaan injektiona ihon alle tai infuusiona laskimoon. Antotapa, annostus ja hoidon kesto riippuvat sen käytön syystä, potilaan painosta ja hoitovasteesta. Filgrastim Hexalia annetaan yleensä erikoistuneessa hoitokeskuksessa, vaikka ihon alle rokotetut potilaat voivat pistää sen itse, jos he ovat asianmukaisesti koulutettuja. Lisätietoja on pakkausselosteessa.
Miten Filgrastim Hexal vaikuttaa?
Filgrastim Hexalin vaikuttava aine, filgrastiimi, on hyvin samanlainen kuin ihmisen proteiini, jota kutsutaan granulosyyttikolonia stimuloivaksi tekijäksi (G-CSF). Filgrastiimia valmistetaan yhdistelmä -DNA -tekniikalla tunnetulla menetelmällä: sen valmistaa bakteeri, joka on siirretty geeniin (DNA), joka tekee siitä kykenevän tuottamaan filgrastiimia. Korvaava aine toimii samalla tavalla kuin luonnollisesti tuotettu G-CSF stimuloimalla luuydintä tuottamaan enemmän valkosoluja.
Miten Filgrastim Hexalia on tutkittu?
Filgrastim Hexalia on tutkittu sen samankaltaisuuden osoittamiseksi vertailuvalmisteen Neupogenin kanssa.
Neljässä tutkimuksessa tarkasteltiin veren neutrofiilitasoja yhteensä 146 terveellä vapaaehtoisella, joille annettiin Filgrastim Hexalia tai Neupogenia. Tutkimuksissa tarkasteltiin eri lääkeannosten kerta -annoksen ja toistuvan annostelun vaikutuksia ihonalaisena injektiona tai laskimonsisäisenä infuusiona. Näiden tutkimusten pääasiallinen mitta oli neutrofiilien määrä ensimmäisten 10 hoitopäivän aikana.
Mitä hyötyä Filgrastim Hexalista on havaittu tutkimuksissa?
Tutkimusten aikana Filgrastim Hexal ja Neupogen lisäsivät neutrofiilien määrää samalla tavalla terveillä vapaaehtoisilla. Tätä pidettiin riittävänä osoittamaan, että Filgrastim Hexalin hyödyt ovat verrattavissa alkuperäislääkkeen hyötyihin.
Mitä riskejä Filgrastim Hexaliin liittyy?
Yleisin Filgrastim Hexalin käytön yhteydessä havaittu sivuvaikutus (yli 1 potilaalla 10: stä) on tuki- ja liikuntaelimistön kipu (kipu lihaksissa ja luissa). Yli 1 potilaalla 10: stä saattaa esiintyä muita haittavaikutuksia sairauden mukaan. Pakkausselosteessa on luettelo kaikista Filgrastim Hexalin ilmoitetuista sivuvaikutuksista.
Filgrastim Hexalia ei saa antaa henkilöille, jotka voivat olla yliherkkiä (allergisia) filgrastiimille tai jollekin muulle aineelle.
Miksi Filgrastim Hexal on hyväksytty?
Lääkevalmistekomitea (CHMP) katsoi, että Filgrastim Hexal on EU: n lainsäädännön vaatimusten perusteella osoittanut samanlaisia laatu-, turvallisuus- ja tehokkuusominaisuuksia kuin Neupogen. Siksi CHMP on sitä mieltä, että Komitea suositteli myyntiluvan myöntämistä Filgrastim Hexalille Neupogenista.
Muita tietoja Filgrastim Hexalista:
Euroopan komissio myönsi 6. helmikuuta 2009 Hexal AG: lle Filgrastim Hexalin myyntiluvan, joka on voimassa koko Euroopan unionin alueella.
Katso Filgrastim Hexalin EPAR -julkaisun täydellinen versio napsauttamalla tätä.
Tämän yhteenvedon viimeisin päivitys: 12-2008
Tällä sivulla julkaistut tiedot Filgrastim Hexalista voivat olla vanhentuneita tai puutteellisia. Jos haluat käyttää näitä tietoja oikein, katso Vastuuvapauslauseke ja hyödyllisiä tietoja -sivu.