Vaikuttavat aineet: Valaciclovir
Valtrex 250 mg kalvopäällysteiset tabletit
Valtrex 500 mg kalvopäällysteiset tabletit
Valtrex 1000 mg kalvopäällysteiset tabletit
Miksi Valtrexia käytetään? Mitä varten se on?
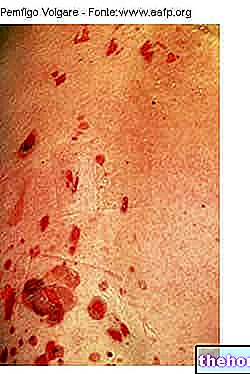
Valtrex kuuluu viruslääkkeiden ryhmään. Se toimii tappamalla tai pysäyttämällä herpes simplex (HSV) -, varicella zoster (VZV) - ja sytomegalovirus (CMV) -nimisten virusten kasvun.
Valtrexia voidaan käyttää:
- vyöruusun hoito (aikuisilla)
- ihon ja sukupuolielinten herpesinfektioiden hoitoon (aikuisilla ja yli 12 -vuotiailla nuorilla) .Sitä käytetään myös estämään näiden infektioiden uusiutuminen.
- huuliherpeksen hoitoon (aikuisilla ja yli 12 -vuotiailla nuorilla)
- ehkäistä CMV -infektioita elinsiirron jälkeen (aikuisilla ja yli 12 -vuotiailla nuorilla)
- hoitaa ja ehkäistä HSV -silmäinfektioita, jotka toistuvat jatkuvasti (aikuisilla ja yli 12 -vuotiailla nuorilla).
Vasta -aiheet Milloin Valtrexia ei tule käyttää
Älä ota Valtrexia
- Jos olet allerginen valasikloviirille tai asikloviirille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa 6).
- Älä ota Valtrexia, jos yllä oleva koskee sinua. Jos olet epävarma, keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Valtrexia.
Käyttöön liittyvät varotoimet Mitä sinun on tiedettävä, ennen kuin otat Valtrexia
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Valtrexia, jos:
- sinulla on munuaisongelmia
- sinulla on maksavaivoja
- on yli 65 -vuotias
- hänen immuunijärjestelmänsä on heikko
Jos et ole varma, koskeeko yllä oleva sinua, keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Valtrexia.
Estää sukupuolielinten herpesin tartunnan muille ihmisille
Jos käytät Valtrexia sukupuolielinten herpesin hoitoon tai ehkäisyyn tai jos sinulla on ollut sukupuolielinten herpes aiemmin, sinulla on oltava suojattu sukupuoli, mukaan lukien kondomien käyttö. Tämä on tärkeää, jotta estetään tartunnan siirtyminen muille ihmisille. Sinun ei pitäisi harrastaa seksiä, jos sinulla on kipua tai rakkuloita sukupuolielimissäsi.
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Valtrexin vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät tai olet äskettäin käyttänyt muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt ja yrttilääkkeitä.
Kerro lääkärille tai apteekkihenkilökunnalle, jos käytät muita munuaisiin vaikuttavia lääkkeitä. Näitä ovat: aminoglykosidit, platinapohjaiset yhdisteet, joditut varjoaineet, metotreksaatti, pentamidiini, foskarnetti, syklosporiini, takrolimuusi, simetidiini ja probenesidi.
Kerro aina lääkärillesi tai apteekkihenkilökunnalle kaikista muista lääkkeistä, kun käytät Valtrexia vyöruusun hoitoon tai elinsiirron jälkeen.
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Valtrexin käyttöä ei yleensä suositella raskauden aikana.Jos olet raskaana tai epäilet olevasi raskaana tai jos suunnittelet raskautta, älä ota Valtrex -valmistetta keskustelematta lääkärisi kanssa.Lääkärisi arvioi hyödyt sinulle ja vauvalle aiheutuva riski ottaa Valtrex raskauden tai imetyksen aikana.
Ajaminen ja koneiden käyttö
Valtrex voi aiheuttaa haittavaikutuksia, jotka vaikuttavat ajokykyyn. Älä aja tai käytä koneita, ellet ole varma, että tämä ei vaikuta sinuun.
Annos, menetelmä ja antotapa Valtrexin käyttö: Annostus
Ota tätä lääkettä juuri sen verran kuin lääkäri on määrännyt. Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Tarvittava annos riippuu siitä, miksi lääkäri on määrännyt sinulle Valtrex -valmistetta. Lääkäri keskustelee tästä kanssasi.
"Herpes zosterin (St. Anthony's fire)" hoito
- Tavanomainen annos on 1000 mg (yksi 1000 mg tabletti tai kaksi 500 mg tablettia) kolme kertaa päivässä.
- Sinun on otettava Valtrex seitsemän päivän ajan.
Kylmäherpeksen hoito
- Suositeltu annos on 2000 mg (kaksi 1000 mg tablettia tai neljä 500 mg tablettia) kahdesti vuorokaudessa.
- Toinen annos tulee ottaa 12 tuntia (aikaisintaan 6 tuntia) ensimmäisen annoksen jälkeen
- Sinun tulee ottaa Valtrex vain yhden päivän ajan (kaksi annosta).
Ihon ja sukupuolielinten herpesin HSV -infektioiden hoito
- Suositeltu annos on 500 mg (yksi 500 mg tabletti tai kaksi 250 mg tablettia) kahdesti vuorokaudessa.
- Ensimmäisen infektion yhteydessä sinun tulee ottaa Valtrexia viisi päivää tai enintään kymmenen päivää, jos lääkäri suosittelee sitä. Toistuvien infektioiden hoidon kesto on yleensä 3-5 päivää.
Estää HSV -infektioiden uusiutumisen niiden saamisen jälkeen
- Suositeltu annos on yksi 500 mg: n tabletti kerran vuorokaudessa.
- Jotkut ihmiset, joilla on usein toistuvia infektioita, pitävät hyödyllisenä ottaa yksi 250 mg: n tabletti kahdesti päivässä.
- Sinun on otettava Valtrex, kunnes lääkäri kehottaa sinua lopettamaan.
CMV (Cytomegalovirus) -infektion estämiseksi
- Suositeltu annos on 2000 mg (kaksi 1000 mg tablettia tai neljä 500 mg tablettia) neljä kertaa päivässä.
- Ota jokainen annos noin 6 tunnin välein.
- Normaalisti aloitat Valtrexin käytön mahdollisimman pian leikkauksen jälkeen.
- Sinun on otettava Valtrex noin 90 päivän ajan leikkauksen jälkeen, kunnes lääkäri kehottaa sinua lopettamaan.
Lääkäri voi muuttaa Valtrex -annosta, jos:
- on yli 65 -vuotias
- on heikko immuunijärjestelmä
- sinulla on munuaisongelmia.
Kerro lääkärillesi ennen Valtrexin ottamista, jos jokin yllä luetelluista tilanteista koskee sinua.
Lääkkeen ottaminen
- Ota tämä lääke suun kautta.
- Niele tabletit kokonaisina veden kanssa.
- Ota Valtrex samaan aikaan joka päivä.
- Ota Valtrex lääkärin tai apteekkihenkilökunnan ohjeiden mukaan.
Yli 65 -vuotiaat tai munuaisongelmat
Valtrex -hoidon aikana on erittäin tärkeää juoda vettä säännöllisesti koko päivän. Tämä auttaa vähentämään ei -toivottuja vaikutuksia, jotka voivat vaikuttaa munuaisiin tai hermostoon. Lääkäri seuraa sinua huolellisesti näiden vaikutusten merkkien varalta. Hermoston haittavaikutuksia voivat olla sekavuus tai levottomuus, epätavallinen uneliaisuus tai tunnottomuus.
Yliannostus Mitä tehdä, jos olet ottanut liikaa Valtrexia
Jos otat enemmän Valtrexia kuin sinun pitäisi
Valtrex ei yleensä ole haitallinen, ellet ota liikaa ja useita päiviä. Jos otat liian monta tablettia, saatat tuntea pahoinvointia, oksentelua, munuaisongelmia, hämmennystä, levottomuutta tai huonovointisuutta, nähdä asioita, joita ei ole, tai menettää tajuntasi. Kerro lääkärille tai apteekkihenkilökunnalle, jos olet ottanut liikaa Valtrexia. Ota lääkepakkaus mukaasi.
Jos unohdat ottaa Valtrexia
- Jos unohdat ottaa Valtrexia, ota se heti kun muistat. Jos kuitenkin on melkein seuraavan annoksen aika, jätä unohtunut annos väliin.
- Älä ota kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Sivuvaikutukset Mitkä ovat Valtrexin sivuvaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Seuraavia haittavaikutuksia voi esiintyä tämän lääkkeen kanssa:
Ehdot, joihin sinun on kiinnitettävä huomiota
- vaikeat allergiset reaktiot (anafylaksia). Nämä ovat harvinaisia Valtrexia käyttävillä ihmisillä. Oireiden nopea kehitys, mukaan lukien:
- punoitus, kutiava ihottuma
- huulten, kasvojen, kaulan ja kurkun turvotus, joka aiheuttaa hengitysvaikeuksia (angioedeema)
- äkillinen verenpaineen lasku, joka johtaa romahtamiseen.
Jos sinulla on allerginen reaktio, lopeta Valtrex -valmisteen käyttö ja ota heti yhteys lääkäriisi.
Hyvin yleinen (voi esiintyä useammalla kuin yhdellä henkilöllä 10: stä):
- päänsärky
Yleiset (voi esiintyä enintään 1 käyttäjällä 10: stä):
- pahoinvointi
- huimaus
- Hän vetäytyi
- ripuli
- ihoreaktio auringonvalolle altistumisen jälkeen (valoherkkyys)
- ihottuma
- kutittaa
Melko harvinaiset (voi esiintyä enintään 1 käyttäjällä 100: sta):
- hämmennyksen tila
- nähdä tai kuulla asioita, joita ei ole olemassa (hallusinaatiot)
- vakavan tunnottomuuden tila
- vapinaa
- levottomuuden tila
Nämä hermoston sivuvaikutukset ilmenevät yleensä ihmisillä, joilla on munuaisongelmia, vanhuksilla tai elinsiirtopotilailla, jotka ottavat suuria annoksia, vähintään 8 grammaa, Valtrexia päivässä. Nämä vaikutukset yleensä paranevat, kun Valtrex -hoito lopetetaan tai sitä käytetään.
Muut harvinaiset haittavaikutukset:
- hengenahdistus (hengenahdistus)
- vatsavaivat
- ihottuma, joskus kutina, nokkosihottuma
- alaselän kipu (munuaiskipu)
- veri virtsassa (hematuria)
Melko harvinaiset haittavaikutukset, jotka voivat näkyä verikokeissa:
- vähentynyt valkosolujen määrä (leukopenia)
- verihiutaleiden määrän väheneminen, jotka ovat hyytymiseen tarvittavia soluja (trombosytopenia)
- maksan tuottamien aineiden lisääntyminen.
Harvinaiset (voi esiintyä enintään 1 käyttäjällä 1000: sta):
- epävakaus kävelyssä ja koordinaation puute (ataksia)
- sanat, jotka puhutaan hitaasti ja virheellisesti (dysartria)
- kouristukset
- heikentynyt aivotoiminta (enkefalopatia)
- tajunnan menetys (kooma)
- sekava tai häiriintynyt ajattelu (delirium)
Nämä hermoston sivuvaikutukset ilmenevät yleensä ihmisillä, joilla on munuaisongelmia, vanhuksilla tai elinsiirtopotilailla, jotka ottavat suuria annoksia, 8 grammaa tai enemmän, Valtrexia päivässä.Nämä vaikutukset yleensä paranevat, kun Valtrex -hoito lopetetaan tai otetaan.
Muut harvinaiset haittavaikutukset
- munuaisongelmat, joissa virtsaa on vähän tai ei lainkaan.
Sivuvaikutusten ilmoittaminen
Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen, mukaan lukien mahdolliset haittavaikutukset, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan ilmoittamalla ilmoitusjärjestelmän kautta osoitteessa https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkkeen turvallisuudesta.
Vanhentuminen ja säilyttäminen
- Ei lasten ulottuville eikä näkyville.
- Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivä (EXP) viittaa kuukauden viimeiseen päivään.
- Säilytä alle 30 ° C: n lämpötilassa.
- Älä heitä lääkkeitä viemäriin tai talousjätteisiin. Kysy apteekista, kuinka heittää pois lääkkeet, joita et enää käytä. Tämä auttaa suojelemaan ympäristöä.
Koostumus ja lääkemuoto
Mitä Valtrex sisältää
- Vaikuttava aine on valatsikloviiri. Yksi tabletti sisältää 250 mg, 500 mg tai 1000 mg valasikloviiria (valatsikloviirihydrokloridina).
Muut aineet ovat:
Tabletin ydin
Mikrokiteinen selluloosa
Krospovidoni
Povidoni
Magnesiumstearaatti
Vedetön kolloidinen piidioksidi
Pinnoite
Hypromelloosi
Titaanidioksidi
Makrogoli 400
Polysorbaatti 80 (vain 500 mg ja 1000 mg tabletit)
Karnaubavaha
Lääkevalmisteen kuvaus ja pakkaus
Valtrex -tabletit ovat polyvinyylikloridi / alumiini -läpipainopakkauksissa.
Valtrex 250 mg tabletit toimitetaan pakkauksissa, jotka sisältävät 20 tai 60 kalvopäällysteistä tablettia. Ne ovat valkoisia ja niiden toisella puolella on merkintä "GX CE7".
Valtrex 500 mg tabletit toimitetaan pakkauksissa, jotka sisältävät 10, 24, 30, 42, 90 tai 112 kalvopäällysteistä tablettia. Ne ovat valkoisia ja niiden toisella puolella on merkintä "GX CF1".
Valtrex 1000 mg tabletit toimitetaan pakkauksissa, jotka sisältävät 21 kalvopäällysteistä tablettia. Ne ovat valkoisia ja niiden toisella puolella on merkintä "GX CF2".
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI
ZELITREX -TABLETIT, PÄÄLLYTTYNYT KALVOLLA
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
Yksi tabletti sisältää valatsikloviirihydrokloridia, joka vastaa 250 mg valasikloviiria.
Yksi tabletti sisältää valatsikloviirihydrokloridia, joka vastaa 500 mg valasikloviiria.
Yksi tabletti sisältää valatsikloviirihydrokloridia, joka vastaa 1000 mg valasikloviiria.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO
Kalvopäällysteinen tabletti
250 mg tabletti
Valkoinen, pitkänomainen, kaksoiskupera tabletti, jonka ydin on valkoinen tai tummanvalkoinen ja jossa on toisella puolella merkintä "GX CE7".
500 mg tabletti
Valkoinen, pitkänomainen, kaksoiskupera tabletti, jonka ydin on valkoinen tai tummanvalkoinen ja jossa on toisella puolella merkintä "GX CF 1".
1000 mg tabletti
Valkoinen, pitkänomainen, kaksoiskupera tabletti, jonka ydin on valkoinen tai tummanvalkoinen ja jossa on jakouurre molemmilla puolilla ja jonka toisella puolella on merkintä "GX CF2".
04.0 KLIINISET TIEDOT
04.1 Käyttöaiheet
Varicella zoster -viruksen (VZV) infektiot - herpes zoster
Valtrex on tarkoitettu herpes zosterin ja silmätaudin hoitoon aikuisille, joilla on immuunivaste (ks. Kohta 4.4).
Valtrex on tarkoitettu herpes zosterin hoitoon aikuispotilaille, joilla on lievä tai kohtalainen immunosuppressio (ks. Kohta 4.4).
Herpes simplex -viruksen (HSV) infektiot
Valtrex on tarkoitettu
• ihon ja limakalvojen HSV -infektioiden hoitoon ja tukahduttamiseen, mukaan lukien
- ensimmäisen sukupuolielinten herpes -episodin hoito immuunipuutteisilla aikuisilla ja nuorilla sekä immuunipuutteisilla aikuisilla
- toistuvien sukupuolielinten herpesinfektioiden hoito immuunipuutteisilla aikuisilla ja nuorilla ja immuunipuutteisilla aikuisilla
- toistuvan sukupuolielinten herpesin tukahduttaminen immuunikompetentteilla aikuisilla ja nuorilla ja immuunipuutteisilla aikuisilla
• toistuvien HSV -silmäinfektioiden hoitoon ja estämiseen (ks. Kohta 4.4).
Kliinisiä tutkimuksia ei ole tehty HSV-tartunnan saaneilla potilailla, joiden immuunivajavuus johtuu muista syistä kuin HIV-infektiosta (ks. Kohta 5.1).
Sytomegalovirusinfektiot (CMV)
Valtrex on tarkoitettu aikuisten ja nuorten CMV -infektion ja sairauden ennaltaehkäisyyn kiinteän elinsiirron jälkeen (ks. Kohta 4.4).
04.2 Annostus ja antotapa
Varicella zoster -viruksen (VZV) infektiot - herpes zoster ja oftalmical zoster
Potilaita tulee neuvoa aloittamaan hoito mahdollisimman pian herpes zoster -diagnoosin jälkeen. Ei ole tietoa hoidosta, joka on aloitettu yli 72 tuntia zoster -ihottuman puhkeamisen jälkeen.
Immunokompetentit aikuiset
Immunokompetenttien potilaiden annos on 1000 mg kolme kertaa päivässä seitsemän päivän ajan (päivittäinen kokonaisannos 3000 mg). Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella (ks. Munuaisten vajaatoiminta alla).
Immuunipuutteiset aikuiset
Immuunipuutteisten potilaiden annos on 1000 mg kolme kertaa päivässä vähintään seitsemän päivän ajan (kokonaisvuorokausiannos 3000 mg) ja 2 päivän ajan leesioiden kuorinnan jälkeen.
Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella (ks. Munuaisten vajaatoiminta alla).
Immuunipuutteisilla potilailla viruslääkehoitoa suositellaan potilaille, jotka esiintyvät viikon kuluessa rakkuloiden muodostumisesta tai milloin tahansa ennen vaurioiden muodostumista.
Herpes simplex -viruksen (HSV) infektioiden hoito aikuisilla ja nuorilla (≥ 12 vuotta)
Immunokompetentit aikuiset ja nuoret (≥ 12 -vuotiaat)
Valtrex -annos on 500 mg kahdesti vuorokaudessa (päivittäinen kokonaisannos 1000 mg). Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella (ks. Munuaisten vajaatoiminta alla).
Toistuvissa jaksoissa hoidon tulee kestää kolme tai neljä päivää. Alkuvaiheissa, jotka voivat olla vakavampia, hoitoa on ehkä pidennettävä kymmeneen päivään. Hoito tulee aloittaa mahdollisimman pian. Toistuvissa herpes simplex -tapauksissa hoito on suositeltavaa suorittaa prodromaalivaiheessa tai heti ensimmäisten merkkien tai oireiden ilmaantuessa.Valtrex voi estää leesioiden kehittymisen, kun se otetaan toistuvan HSV -infektion ensimmäisten merkkien ja oireiden yhteydessä.
Kylmäherpes
Kylmäherpeksen hoitoon valasikloviiri 2000 mg kahdesti vuorokaudessa yhden päivän ajan on tehokas hoito aikuisille ja nuorille.Toinen annos tulee ottaa noin 12 tuntia (aikaisintaan 6 tuntia) ensimmäisen annoksen jälkeen. Sitä on pienennettävä kreatiniinipuhdistuman perusteella ( ks. alla munuaisten vajaatoiminta).
Tätä annostusohjelmaa käytettäessä hoito ei saisi ylittää yhtä päivää, koska siitä ei ole osoitettu olevan "kliinistä lisähyötyä. Hoito on aloitettava ensimmäisistä huuliherpesoireista (esim. Pistely, kutina tai polttaminen)."
Immuunipuutteiset aikuiset
HSV: n hoidossa aikuisilla, joilla on immuunivaste, annos on 1000 mg kahdesti vuorokaudessa vähintään 5 päivän ajan potilaan kliinisen tilan ja immunologisen tilan vakavuuden arvioinnin jälkeen. Annostus on aloitettava mahdollisimman pian. Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella (ks. alla munuaisten vajaatoiminta). Maksimaalisen kliinisen hyödyn saavuttamiseksi hoito on aloitettava 48 tunnin kuluessa. Leesioiden kehittymistä on seurattava tarkasti.
Toistuvien herpes simplex -virus (HSI) -infektioiden tukahduttaminen aikuisilla ja nuorilla (≥ 12 vuotta)
Immunokompetentit aikuiset ja nuoret (≥ 12 -vuotiaat)
Annos on 500 mg Valtrexia kerran vuorokaudessa. Jotkut potilaat, joilla uusiutumisjaksoja esiintyy hyvin usein (≥ 10 / vuosi ilman hoitoa), voivat hyötyä enemmän päivittäisestä 500 mg: n annoksesta, joka on jaettu kahteen annokseen (250 mg kahdesti vuorokaudessa). Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella. (ks. munuaisten vajaatoiminta alla) Hoito on arvioitava uudelleen 6-12 kuukauden hoidon jälkeen.
Immuunipuutteiset aikuiset
Annos on 500 mg Valtrexia kahdesti vuorokaudessa. Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella (ks. Munuaisten vajaatoiminta alla). Hoito on arvioitava uudelleen 6-12 kuukauden hoidon jälkeen.
Sytomegalovirus (CMI) -infektion ja -sairauden ehkäisy aikuisilla ja nuorilla (≥ 12 vuotta)
Valtrex -annos on 2000 mg neljä kertaa päivässä, ja se aloitetaan mahdollisimman pian elinsiirron jälkeen. Tätä annosta on pienennettävä kreatiniinipuhdistuman perusteella (ks. Munuaisten vajaatoiminta alla).
Hoidon kesto on tyypillisesti 90 päivää, mutta sitä on ehkä pidennettävä suuririskisillä potilailla.
Erityisryhmät
Lapset
Valtrexin tehoa alle 12 -vuotiailla lapsilla ei ole arvioitu.
Eläkeläiset
Iäkkäillä potilailla on otettava huomioon munuaisten vajaatoiminnan mahdollisuus ja annosta on muutettava vastaavasti (ks. Alla oleva munuaisten vajaatoiminta). Riittävä nesteytys on pidettävä yllä.
Munuaisten vajaatoiminta
Varovaisuutta on noudatettava annettaessa Valtrexia potilaille, joilla on munuaisten vajaatoiminta. Riittävä nesteytys on säilytettävä.Valtrex -annosta on pienennettävä potilailla, joilla on munuaisten vajaatoiminta, kuten taulukossa 1 on esitetty.
Ajoittaista hemodialyysihoitoa saavilla potilailla Valtrex -annos on annettava hemodialyysin jälkeen.Kreatiniinipuhdistumaa on seurattava usein, erityisesti silloin, kun munuaisten toiminta muuttuu nopeasti, esimerkiksi heti munuaisensiirron tai sen juurtumisen jälkeen.Valtrex -annosta on muutettava vastaavasti.
Maksan vajaatoiminta
Aikuisilla potilailla tehdyt tutkimukset, joissa käytettiin 1000 mg valasikloviiriannosta, osoittavat, että annosta ei tarvitse muuttaa potilailla, joilla on lievä tai kohtalainen kirroosi (maksan synteesitoiminto säilyy). Farmakokineettiset tiedot aikuispotilaista, joilla on pitkälle edennyt kirroosi (heikentynyt maksan synteesitoiminta ja näyttöä)
systeeminen shuntti) eivät osoita tarvetta muuttaa annosta; suurempia annoksia (4000 mg tai enemmän päivässä), ks. kohta 4.4.
Taulukko 1: ANNOSTUSSÄÄDÖT "MUNNEY INSUFFICIENY"
a Potilaille, jotka saavat jaksottaista hemodialyysiä, annos on annettava dialyysin jälkeen dialyysipäivinä.
b HSV: n tukahduttamiseksi immuunikompetentteilla henkilöillä, joilla on ollut uusiutumisia vuodessa ≥10, parempia tuloksia voidaan saada 250 mg: lla kahdesti vuorokaudessa.
04.3 Vasta -aiheet
Yliherkkyys valasikloviirille tai asikloviirille tai apuaineille (ks. Kohta 6.1).
04.4 Varoitukset ja käyttöön liittyvät varotoimet
Nesteytyksen tila
On huolehdittava siitä, että potilaat, joilla on nestehukka, erityisesti vanhukset, saavat riittävästi nestettä.
Käyttö munuaisten vajaatoimintaa sairastaville potilaille ja iäkkäille potilaille
Asikloviiri eliminoituu munuaispuhdistuman kautta, joten valatsikloviiriannosta on pienennettävä potilailla, joilla on munuaisten vajaatoiminta (ks. Kohta 4.2). Iäkkäillä potilailla on todennäköisesti munuaisten vajaatoiminta, joten annoksen pienentämisen tarvetta on harkittava tässä potilasryhmässä. Sekä iäkkäillä potilailla että potilailla, joilla on munuaisten vajaatoiminta, on suurempi riski saada neurologisia sivuvaikutuksia, ja heitä tulee seurata huolellisesti näiden vaikutusten varalta. Raportoiduissa raporteissa nämä reaktiot olivat yleensä palautuvia hoidon lopettamisen jälkeen (ks. Kohta 4.8).
Suurempien valatsikloviiriannosten käyttö maksan vajaatoiminnassa ja maksansiirrossa
Ei ole olemassa tietoja suurempien valatsikloviiriannosten (4000 mg tai enemmän päivässä) käytöstä maksasairautta sairastavilla potilailla. 4000 mg näille potilaille.
Käytä vyöruusun hoitoon
Kliinistä vastetta on seurattava tarkasti erityisesti immuunipuutteisilla potilailla. IV -viruslääkehoitoa tulee harkita, jos vaste suun kautta annettavaan hoitoon katsotaan riittämättömäksi.
Potilaita, joilla on monimutkainen herpes zoster, esimerkiksi viskeraalinen osallisuus, levinnyt vyöruusu, motorinen neuropatia, aivotulehdus ja aivoverenkierron komplikaatiot, tulee hoitaa laskimonsisäisellä antiviraalisella hoidolla.
Lisäksi potilaita, joilla on heikentynyt immuunivaste, joilla on silmäsairaus tai joilla on suuri taudin leviämisen ja sisäelinten osallisuuden riski, tulee hoitaa laskimonsisäisellä viruslääkityksellä.
Sukupuolielinten herpesin siirto
Potilaita tulee neuvoa välttämään yhdyntää oireiden ilmaantuessa, vaikka viruslääkitys olisi aloitettu. Antiviraalisella aineella tapahtuvan tukahduttavan hoidon aikana virusten leviämisen taajuus vähenee merkittävästi. Tartuntariski on kuitenkin edelleen mahdollinen. Siksi valasikloviirihoidon lisäksi potilaille suositellaan suojattua yhdyntää.
Käyttö HSV -silmäinfektioissa
Näiden potilaiden kliinistä vastetta on seurattava tarkasti. IV -viruslääkehoitoa tulee harkita, jos vaste suun kautta annettavaan hoitoon katsotaan riittämättömäksi.
Käyttö CMV -infektioissa
Tiedot valatsikloviirin tehosta elinsiirtopotilailla (≥ 200), joilla on suuri CMV-taudin riski (esim. CMV-positiivinen luovuttaja / CMV-negatiivinen vastaanottaja tai induktiivisen hoidon käyttö tymosyyttiglobuliinilla) osoittavat, että valatsikloviiria tulee käyttää vain näissä potilaille, kun siedettävyysongelmat estävät valgansikloviirin tai gansikloviirin käytön.
CMV -ennaltaehkäisyyn tarvittava suuri valasikloviiriannos voi johtaa haittavaikutusten, mukaan lukien keskushermoston poikkeavuuksien, esiintymistiheyteen useammin kuin muilla käyttöaiheilla annetuilla pienemmillä annoksilla (ks. Kohta 4.8). toiminta ja annos säädetty asianmukaisesti (ks. kohta 4.2).
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Valasikloviirin ja munuaistoksisten lääkevalmisteiden samanaikaisessa käytössä on noudatettava varovaisuutta, erityisesti potilailla, joiden munuaisten toiminta on heikentynyt ja joiden munuaisten toimintaa on seurattava säännöllisesti. Tämä koskee aminoglykosidien, platinapohjaisten yhdisteiden, jodattujen varjoaineiden, metotreksaatin, pentamidiinin, foskarnetin, syklosporiinin ja trakolimuusin samanaikaista antamista.
Asikloviiri eliminoituu muuttumattomana pääasiassa virtsaan aktiivisen munuaistiehyen erityksen kautta. Kun 1000 mg valasikloviiria on annettu, simetidiini ja probenesidi pienentävät asikloviirin munuaispuhdistumaa ja lisäävät asikloviirin AUC -arvoa noin 25% ja 45% estämällä asikloviirin aktiivista munuaisteneritystä. Simetidiini ja probenesidi yhdessä valatsikloviirin kanssa lisäävät asikloviirin AUC -arvoa noin 65%. Muut samanaikaisesti annetut lääkkeet (mukaan lukien esim. Tenofoviiri), jotka kilpailevat aktiivisen tubulaarisen erityksen kanssa tai estävät sitä, voivat lisätä asikloviiripitoisuuksia tällä mekanismilla. Vastaavasti valatsikloviirin antaminen voi lisätä muiden samanaikaisesti annettavien aineiden pitoisuudet plasmassa.
Potilaat, jotka altistuvat suuremmille asikloviiriannoksille valasikloviirista (esim. Zoster -hoitoon tai CMV -ennaltaehkäisyyn), ovat varovaisia, kun niitä annetaan samanaikaisesti lääkkeiden kanssa, jotka estävät aktiivista munuaistiehyen eritystä.
Asikloviirin ja siirtopotilaiden immunosuppressiivisen aineen, mykofenolaattimofetiilin, inaktiivisen metaboliitin, plasman AUC -arvojen nousua on havaittu, kun lääkevalmisteita annetaan samanaikaisesti. Valasikloviirin ja mykofenolaattimofetiilin samanaikaisen käytön yhteydessä terveillä vapaaehtoisilla ei havaittu muutoksia huippupitoisuuksissa tai AUC -arvossa Tämän yhdistelmän käytöstä on vain vähän kliinistä kokemusta.
04.6 Raskaus ja imetys
Raskaus
Valasikloviirin käytöstä on vain vähän tietoja ja raskaana olevista rekistereistä (joissa on dokumentoitu raskauden lopputulos naisilla, jotka ovat altistuneet valatsikloviirille tai asikloviirille suun kautta tai suun kautta). 111 ja 1246 (29 ja 756 altistuneet raskauden ensimmäisen kolmanneksen aikana) ja "markkinoille tulon jälkeiset kokemukset" eivät viitanneet epämuodostumiin tai sikiö- / vastasyntyneen myrkyllisyyteen. . Valasikloviiria tulee käyttää raskauden aikana vain, jos hoidosta saatava hyöty on suurempi kuin mahdollinen riski.
Ruokinta-aika
Asikloviiri, valatsikloviirin tärkein metaboliitti, erittyy äidinmaitoon. Valasikloviirin terapeuttisilla annoksilla ei kuitenkaan odoteta olevan vaikutusta imetettäviin vastasyntyneisiin / imeväisiin, koska imeväisen nauttima annos on alle 2% vastasyntyneen herpesin hoitoon annetusta suonensisäisen asikloviirin terapeuttisesta annoksesta (ks. Kohta 5.2) Valatsikloviiria tulee käyttää varoen imetyksen aikana ja vain jos se on kliinisesti osoitettu.
Hedelmällisyys
Valatsikloviiri ei vaikuta suun kautta hoidettujen rottien hedelmällisyyteen. Kiveksen atrofiaa ja aspermatogeneesiä havaittiin rotilla ja koirilla suurilla parenteraalisen asikloviirin annoksilla. Valasikloviirilla ei ole tehty hedelmällisyystutkimuksia ihmisillä, mutta muutoksia siittiöiden lukumäärässä, liikkuvuudessa ja morfologiassa ei ole raportoitu 20 potilaalla 6 kuukauden päivittäisen 400 mg - 1000 mg asikloviirihoidon jälkeen.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn
Tutkimuksia ajokyvystä ja koneiden käyttökyvystä ei ole tehty.
Potilaan kliininen tila ja Valtrexin haittavaikutusprofiili on otettava huomioon arvioitaessa potilaan kykyä ajaa ja käyttää koneita. Muita haitallisia vaikutuksia näihin toimintoihin ei voida ennakoida vaikuttavan aineen farmakologian perusteella.
04.8 Haittavaikutukset
Yleisimmät haittavaikutukset, joita kliinisissä tutkimuksissa Valtrexilla hoidetuilla potilailla raportoitiin vähintään yhdessä käyttöaiheessa, olivat päänsärky ja pahoinvointi.Vakavampia haittavaikutuksia, kuten tromboottinen trombosytopeeninen purppura / hemolyyttinen ureeminen oireyhtymä, akuutti munuaisten vajaatoiminta ja neurologiset häiriöt, kuvataan yksityiskohtaisemmin. valmisteyhteenvedon muissa osissa.
Sivuvaikutukset on lueteltu alla elinjärjestelmän ja esiintymistiheyden mukaan. Seuraavia yleisyysluokkia käytetään haittavaikutusten luokittelemiseen:
Kliinisistä tutkimuksista saatuja tietoja käytettiin haittavaikutusten esiintymistiheyden määrittämiseen, jos tutkimuksissa todettiin olevan yhteys valatsikloviirin kanssa.
Haittavaikutusten osalta, jotka on tunnistettu markkinoille tulon jälkeen, mutta joita ei ole havaittu kliinisissä tutkimuksissa, arviointipisteen konservatiivisempaa arvoa ("kolmen sääntö") käytettiin haittavaikutusten esiintymistiheyden määrittämiseen. Markkinoille tulon jälkeen havaittujen ja kliinisissä tutkimuksissa havaittujen haittavaikutusten valasikloviiriin liittyvien haittavaikutusten osalta haittavaikutusten yleisyysluokkien määrittämisessä käytettiin tutkimuksessa raportoitua esiintyvyyttä. tutkimukset, jotka kattavat useita käyttöaiheita (herpes zosterin hoito, sukupuolielinten herpesin hoito / tukahduttaminen ja huuliherpes).
Tiedot kliinisistä tutkimuksista
Hermosto
Hyvin yleinen: päänsärky
Ruoansulatuselimistö
Yleinen: pahoinvointi
Julkaise markkinointitiedot
Veren ja imukudoksen häiriöt
Melko harvinaiset: leukopenia, trombosytopenia
Leukopeniaa on raportoitu useimmissa tapauksissa immuunipuutteisilla potilailla.
Immuunijärjestelmän häiriöt
Harvinainen: anafylaksia
Psyykkiset häiriöt ja hermoston patologiat
Yleinen: huimaus
Melko harvinainen: sekavuus, hallusinaatiot, tajunnan huononeminen, vapina,
levottomuus
Harvinainen: ataksia, dysartria, kouristukset, enkefalopatia, kooma, psykoottiset oireet, delirium.
Neurologiset häiriöt, joskus vakavat, voivat liittyä enkefalopatiaan ja niihin voivat liittyä sekavuus, levottomuus, kouristukset, aistiharhat, kooma.Nämä tapahtumat ovat yleensä palautuvia ja niitä havaitaan yleensä potilailla, joilla on munuaisten vajaatoiminta tai muita altistavia tekijöitä (ks. Kohta 4.4). potilailla, jotka saivat suuria Valtrex -annoksia (8000 mg päivässä) CMV -ennaltaehkäisyyn, neurologisia reaktioita esiintyi useammin verrattuna muihin käyttöaiheisiin käytettyihin pienempiin annoksiin.
Hengityselimet, rintakehä ja välikarsina
Melko harvinainen: hengenahdistus
Ruoansulatuselimistö
Yleiset: oksentelu, ripuli
Melko harvinainen: vatsavaivat
Maksa ja sappi
Melko harvinaiset: palautuvat muutokset maksan toimintakokeissa (esim. Bilirubiini, entsyymit)
maksasairaus)
Iho ja ihonalainen kudos
Yleinen: ihottuma, mukaan lukien valoherkkyys, kutina
Melko harvinainen: nokkosihottuma
Harvinainen: angioedeema
Munuaiset ja virtsatiet
Melko harvinainen: munuaiskipu, hematuria (liittyy usein muihin munuaistapahtumiin)
Harvinainen: munuaisten vajaatoiminta, akuutti munuaisten vajaatoiminta (erityisesti
iäkkäille potilaille tai potilaille, joilla on munuaisten vajaatoiminta ja jotka saavat suositeltuja annoksia suurempia annoksia).
Munuaiskipu voi liittyä munuaisten vajaatoimintaan.
Asykloviirikiteiden saostumista munuaisiin on myös raportoitu. Riittävä nesteen saanti on varmistettava hoidon aikana (ks. Kohta 4.4).
Lisätietoja erityisistä potilasryhmistä
Vaikeasti immuunipuutteisilla aikuispotilailla, etenkin potilailla, joilla on pitkälle edennyt HIV -tauti ja jotka saavat kliinisissä tutkimuksissa suuria annoksia (8000 mg päivässä) valatsikloviiria pitkiä aikoja, on raportoitu munuaisten vajaatoimintaa, mikroangiopaattista hemolyyttistä anemiaa ja trombosytopeniaa (joskus siihen liittyvää). Näitä havaintoja on havaittu myös potilailla, joita ei ole hoidettu valasikloviirilla ja joilla on sama perussairaus tai samanaikainen sairaus.
04.9 Yliannostus
Oireet ja merkit
Akuuttia munuaisten vajaatoimintaa ja neurologisia oireita, kuten sekavuutta, aistiharhoja, levottomuutta, tajunnan heikkenemistä ja koomaa on raportoitu potilailla, jotka ovat saaneet valatsikloviirin yliannoksen. Pahoinvointia ja oksentelua on myös raportoitu. Varovaisuutta on noudatettava tahattoman yliannostuksen estämiseksi. Monet näistä raportoiduista tapauksista koskivat iäkkäitä potilaita ja munuaisten vajaatoimintaa sairastavia potilaita, jotka olivat saaneet toistuvia yliannostuksia asianmukaisen annoksen pienentämisen puutteen vuoksi.
Hoito
Potilaita on tarkkailtava huolellisesti toksisuuden merkkien varalta. Hemodialyysi edistää merkittävästi asykloviirin poistumista verestä, ja siksi sitä voidaan pitää vaihtoehtona oireisen yliannostuksen sattuessa.
05.0 FARMAKOLOGISET OMINAISUUDET
05.1 Farmakodynaamiset ominaisuudet
Farmakoterapeuttinen ryhmä: Nukleosidit ja nukleotidit, pois lukien käänteiskopioijaentsyymin estäjät. ATC -koodi: J05AB 11.
Toimintamekanismi
Valasikloviiri, viruslääke, on asikloviirin esteri L-valiinin kanssa. Asikloviiri on puriinin (guaniinin) nukleosidianalogi.
Valatsikloviiri muuttuu ihmisissä nopeasti ja lähes kokonaan asikloviiriksi ja valiiniksi, luultavasti valatsikloviirihydrolaasina tunnetulla entsyymillä.
Asykloviiri on spesifinen herpesvirusten estäjä, jolla on aktiivisuutta, in vitro, Herpes simplex -viruksia (HSV) tyyppejä 1 ja 2, Varicella zoster -virusta (VZV), sytomegalovirusta (CMV), Epstein-Barr -virusta (EBV) ja ihmisen herpesvirusluokkaa 6 (HHV-6) vastaan). Asykloviiri, joka on fosforyloitu aktiivisessa trifosfaattimuodossaan, estää herpeettisten virusten DNA -synteesiä.
Fosforylaation ensimmäinen vaihe edellyttää tietyn virusentsyymin aktiivisuutta. HSV-, VZV- ja EBV-virusten tapauksessa tämä entsyymi on viruksen tymidiinikinaasi (TK), jota esiintyy vain viruksella infektoiduissa soluissa. Selektiivisyys ylläpidetään ainakin osittain fosfotransferaasigeenin UL97 välittämän fosforylaation avulla. Asykloviirin tarve aktivoida spesifisellä virusentsyymillä selittää suurelta osin sen selektiivisyyden.
Fosforylaatioprosessi (asykloviirimonofosfaatista trifosfaatiksi) saadaan päätökseen solukinaasien avulla. Asykloviiritrifosfaatti estää kilpailevasti viruksen DNA-polymeraasia ja tämän nukleosidianalogin liittäminen virus-DNA: han aiheuttaa jälkimmäisen ketjun venymisprosessin keskeytymisen, mistä seuraa DNA-synteesin ja viruksen replikaation estyminen.
Farmakodynaamiset vaikutukset
Resistenssi asykloviirille johtuu yleensä tymidiinikinaasin fenotyyppisestä puutteesta, mikä johtaa virukseen, joka on epäedullisessa asemassa luonnollisessa isännässä. Vähentynyt herkkyys asikloviirille on kuvattu johtuen minimaalisista muutoksista viruksen tymidiinikinaasissa tai viruksen DNA -polymeraasissa, ja näiden varianttifenotyyppien virulenssi on samanlainen kuin villiviruksen.
Asikloviirihoitoa tai ennaltaehkäisyä saavien potilaiden HSV: n ja VZV: n kliinisten isolaattien seuranta paljasti, että virusherkkyyden heikkeneminen asikloviirille on erittäin harvinaista immuunikompetentteilla isännöillä ja sitä havaitaan vain harvoin potilailla, joilla on vakava immuunivaste, kuten esim. elin- tai luuydinsiirto, potilaat, jotka saavat kemoterapiaa pahanlaatuisten kasvainten hoitoon, ja potilaat, joilla on ihmisen immuunikatovirus (HIV).
Kliiniset tutkimukset
Varicella Zoster -virusinfektio
Valtrex nopeuttaa kivun paranemista: lyhentää vyöruusuun liittyvän kivun kestoa ja vyöruusuun liittyvien kipujen määrää, mukaan lukien akuutti neuralgia, ja yli 50-vuotiailla potilailla postherpeettistä neuralgiaa. Valtrex vähentää silmäsairauksien riskiä silmän vyöruususta.
Laskimonsisäistä hoitoa pidetään yleensä standardina zosterin hoidossa immuunipuutteisilla potilailla. Kuitenkin rajalliset tiedot viittaavat valatsikloviirin kliiniseen hyötyyn VZV -infektion (herpes zoster) hoidossa joillakin immuunipuutteisilla potilailla, mukaan lukien potilaat, joilla on kiinteä elinsyöpä, HIV, autoimmuunisairaudet, lymfooma, leukemia ja kantasolusiirrot.
Herpes simplex -virusinfektio
Valatsikloviiri HSV -silmäinfektioiden hoitoon tulee antaa sovellettavien hoito -ohjeiden mukaisesti.
Valasikloviirilla on tehty tutkimuksia sukupuolielinten herpesin hoitoon ja tukahduttamiseen potilailla, joilla on samanaikainen HIV / HSV -infektio ja joiden keskimääräinen CD4 -luku on yli 100 solua / mm3. Valatsikloviiri 500 mg kahdesti vuorokaudessa oli suurempi kuin 1000 mg kerran vuorokaudessa oireiden aiheuttamien uusiutumisten vaimentaminen Valaciclovir 1000 mg kahdesti vuorokaudessa uusiutumisten hoitoon, herpesjakson keston aikana, oli verrattavissa 200 mg: aan suun kautta annettavaa asikloviiria viisi kertaa päivässä.
Valatsikloviirin teho muiden HSV -ihoinfektioiden hoitoon on dokumentoitu. Valatsikloviirin on osoitettu olevan tehokas hoidettaessa huuliherpesä, kemoterapiasta tai sädehoidosta johtuvaa mukosiittia, HSV: n uudelleenaktivointia kasvojen pinnoittamisesta, herpes gladiatorumista. Asikloviirin historiallisen kokemuksen perusteella näyttää siltä, että valatsikloviiri on yhtä tehokas kuin asikloviiri erythema multiforme, ekseema herpeticum ja herpeettinen paronychia hoidossa.
Valatsikloviirin on osoitettu vähentävän sukupuolielinten herpesin tartuntariskiä aikuisilla, joilla on immuunivaste, kun sitä käytetään tukahduttavana hoitona ja yhdistettynä suojattuun yhdyntään. tai ei HSV-2-infektiota. Tulokset osoittivat merkitsevän vähenemisen tartuntariskissä: 75% (oireinen HSV-2-hankinta), 50% (HSV-2-serokonversio) ja 48% (täydellinen HSV-2-hankinta) valasikloviirilla lumelääkkeeseen verrattuna. Valasikloviiri vähensi merkitsevästi erittymistä 73%: lla lumelääkkeeseen verrattuna virusten leviämistä käsittelevään alatutkimukseen osallistuneista henkilöistä (ks. Lisätietoja 4.4 leviämisen vähentämisestä).
Sytomegalovirusinfektio (ks. kohta 4.4)
CMV -profylaksia valatsikloviirilla potilailla, joille on tehty elinsiirto (munuaiset, sydän), vähentää akuutin elinsiirteen hyljinnän, opportunististen infektioiden ja muiden herpeettisten infektioiden (HSV, VZV) esiintymistä. hoito potilailla, joilla on kiinteä elinsiirto.
05,2 "Farmakokineettiset ominaisuudet
Imeytyminen
Valatsikloviiri on asikloviirin aihiolääke. Valasikloviirin asikloviirin hyötyosuus on noin 3,3–5,5 kertaa suurempi kuin historiallisesti oraalisen asikloviirin kohdalla. Oraalisen annon jälkeen valatsikloviiri imeytyy hyvin ja nopeasti ja muuttuu lähes kokonaan asikloviiriksi ja valiiniksi. Tätä konversiota välittää todennäköisesti ihmisen maksasta eristetty entsyymi, joka tunnetaan nimellä valacikloviirihydrolaasi. Asikloviirin hyötyosuus 1000 mg: n valasikloviiriannoksesta on 54%, eikä ruoka vähennä sitä. Valatsikloviirin farmakokinetiikka ei ole annoksesta riippuvainen. Imeytymisnopeus ja -aste vähenevät annoksen kasvaessa, jolloin Cmax -arvo kasvaa suhteellisesti vähemmän alle terapeuttisen annosalueen ja alentunut hyötyosuus yli 500 mg: n annoksilla. Alla on esitetty asikloviirin farmakokineettisten parametrien (PK) ennusteet yksittäisten 250-2000 mg: n valatsikloviiriannosten jälkeen terveillä vapaaehtoisilla, joilla on normaali munuaisten toiminta.
Cmax = huippupitoisuus; Tmax = huippukonsentraation aika; AUC = aika-pitoisuuskäyrän alla oleva alue. Cmax- ja AUC -arvot osoittavat keskiarvon ± keskihajonnan. Tmax -arvot osoittavat mediaanin ja aikavälin.
Muuttumattoman valasikloviirin huippupitoisuudet plasmassa ovat vain 4% asikloviiripitoisuuksista, ne saavutetaan 30-100 minuutin kuluttua mediaanista annoksen jälkeen ja ne ovat määritysrajalla tai sen alapuolella 3 tuntia annoksen jälkeen. Valatsikloviirin ja asikloviirin farmakokineettiset profiilit ovat samanlainen sekä kerta- että toistuvien annosten jälkeen. Herpes zoster ja herpes simplex ja HIV -infektio eivät muuta merkittävästi valacikloviirin ja asikloviirin farmakokinetiikkaa suun kautta annetun valacikloviirin jälkeen verrattuna terveisiin aikuisiin. Siirtopotilailla, jotka saivat valasikloviiria 2000 mg 4 kertaa päivässä, asikloviirin huippupitoisuudet ovat samanlaisia tai suurempia kuin Aikuiset oletetut päivittäiset AUC -arvot ovat merkittävästi korkeammat.
Jakelu
Valasikloviirin sitoutuminen plasman proteiineihin on hyvin vähäistä (15%).
Plasman CSF / AUC-suhteen määrittämä aivo-selkäydinnesteen (CSF) läpäisy on riippumaton munuaisten toiminnasta ja se oli noin 25% asikloviirin ja metaboliitin 8-OH-ACV ja noin 2,5% metaboliitin CMMG suhteen.
Biotransformaatio
Oraalisen annon jälkeen valatsikloviiri muuttuu asikloviiriksi L-valiini ensimmäisestä suolikanavasta ja / tai maksan aineenvaihdunnasta. Asikloviiri muuttuu pieneksi määräksi metaboliitteja
9 (karboksimetoksi) metyyliguaniini (CMMG) alkoholista ja aldehydidehydrogenaasista, 8-hydroksiasikloviirissa (8-OH-ACV) aldehydioksidaasista. Noin 88% plasman kokonaisaltistuksesta johtuu asikloviirista, 11% CMMG: stä ja 1%-8-OH-ACV.Sytokromi P450 ei metaboloi valatsikloviiria eikä asikloviiria.
Eliminaatio
Valatsikloviiri eliminoituu pääasiassa virtsaan asikloviirina (yli 80% saannosta) ja asikloviirin CMMG: n metaboliitina (noin 14% saannosta). Metaboliitti 8-OH-ACV on havaittavissa vain pieninä määrinä virtsassa (asikloviirin eliminaation puoliintumisaika plasmassa sekä yksittäisten että toistuvien valatsikloviiriannosten jälkeen on noin 3 tuntia.
Erityisryhmät
Munuaisten vajaatoiminta
Asikloviirin eliminaatio liittyy munuaisten toimintaan ja asikloviirialtistus kasvaa
munuaisten vajaatoiminnan lisääntymisen myötä. Potilailla, joilla on loppuvaiheen munuaissairaus, asikloviirin keskimääräinen eliminaation puoliintumisaika valacikloviirin annon jälkeen on noin 14 tuntia verrattuna normaaliin munuaistoimintaan noin 3 tuntiin (ks. Kohta 4.2).
Altistumista asikloviirille ja sen metaboliiteille CMMG ja 8-OH-ACV plasmassa ja aivo-selkäydinnesteessä arvioitiin vakaa tila valasikloviirin toistuvan annon jälkeen 6 potilaalla, joiden munuaistoiminta oli normaali (keskimääräinen kreatiniinipuhdistuma 111 ml / min, vaihteluväli 91-144 ml / min), joita hoidettiin 2000 mg: lla 6 tunnin välein ja kolmella potilaalla, joilla oli vaikea munuaisten vajaatoiminta (puhdistuman keskimääräinen kreatiniiniarvo 26 ml / min, vaihteluväli 17-31 ml / min), jota hoidettiin 1500 mg: lla 12 tunnin välein. Plasmassa ja aivo-selkäydinnesteessä asikloviirin ja metaboliittien CMMG ja 8-OH-ACV pitoisuudet olivat keskimäärin 2, 4 ja 5-6 kertaa suurempia vaikeassa munuaisten vajaatoiminnassa kuin normaalissa munuaisten toiminnassa.
Maksan vajaatoiminta
Farmakokineettiset tiedot osoittavat, että maksan vajaatoiminta vähentää valatsikloviirin muutosnopeutta asikloviiriksi, mutta ei täydellistä muuntumista.
Raskaana olevat naiset
Valasikloviirin ja asikloviirin farmakokineettinen tutkimus, joka tehtiin raskauden loppuvaiheessa, osoittaa, että raskaus ei vaikuta valatsikloviirin farmakokinetiikkaan.
Siirrä rintamaitoon
500 mg: n suun kautta annetun valatsikloviiriannoksen jälkeen asikloviirin huippupitoisuudet Cmax rintamaidossa olivat 0,5 - 2,3 kertaa vastaavat äidin seerumin asikloviiripitoisuudet. Asikloviirin keskimääräinen pitoisuus rintamaidossa oli 2,24 mcg / ml (9,95 mikromolia / l). Kun äidin annos on 500 mg valatsikloviiria kahdesti vuorokaudessa, tämä taso saattaa altistaa rintaruokitun lapsen päivittäiselle oraaliselle asikloviiriannokselle noin 0,6 1 mg / kg / vrk. Asikloviirin eliminaation puoliintumisaika rintamaidosta oli samanlainen kuin seerumista Muuttumatonta valatsikloviiria ei havaittu äidin seerumista, rintamaidosta tai imeväisten virtsasta.
05.3 Prekliiniset tiedot turvallisuudesta
Ei-kliiniset tiedot osoittavat, että tavanomaiset tutkimukset eivät viittaa erityiseen vaaraan ihmisille turvallisuus farmakologia, toistuvan annoksen toksisuus, genotoksisuus ja karsinogeenisuus.
Valatsikloviiri ei vaikuta oraalisesti hoidettujen uros- tai naarasrottien hedelmällisyyteen.
Valatsikloviiri ei ollut teratogeeninen rotilla tai kaneilla. Valatsikloviiri metaboloituu lähes kokonaan asikloviiriksi. Asikloviirin antaminen ihon alle kansainvälisesti hyväksytyissä testeissä ei aiheuttanut teratogeenisia vaikutuksia rotilla ja kaneilla. Jatkotutkimuksissa rotilla havaittiin sikiön poikkeavuuksia ja äidin toksisuutta ihon alle annettuna, mikä johti asikloviiripitoisuuksiin plasmassa 100 μg / ml (yli 10 kertaa suurempi kuin yksittäinen 2000 mg: n valatsikloviiriannos ihmisillä, joilla on normaali munuaisten toiminta).
06.0 FARMASEUTTISET TIEDOT
06.1 Apuaineet
Tabletin ydin
Mikrokiteinen selluloosa
Krospovidoni
Povidoni
Magnesiumstearaatti
Kolloidinen piidioksidi
Pinnoite
Hypromelloosi
Titaanidioksidi
Makrogoli
Polysorbaatti 80 (vain 500 mg ja 1000 mg tabletit)
Karnaubavaha
06.2 Yhteensopimattomuus
Ei oleellinen.
06.3 Voimassaoloaika
250 mg tabletit, 1000 mg tabletit
Kaksi vuotta
500 mg tabletit
Kolme vuotta
06.4 Säilytys
Säilytä alle 30 ° C: n lämpötilassa
06.5 Välipakkauksen luonne ja pakkauksen sisältö
Polyvinyylikloridi / alumiini -läpipainopakkaukset.
250 mg tabletit
Pakkaus sisältää 20 tai 60 tablettia
500 mg tabletit
Pakkauskoot: 10, 24, 30, 42, 90 tai 112 tablettia
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
1000 mg tabletit
Pakkaus sisältää 21 tablettia
06.6 Käyttö- ja käsittelyohjeet
Ei erityisiä ohjeita.
07.0 MYYNTILUVAN HALTIJA
GlaxoSmithKline S.p.A. - Via A.Fleming, 2 - Verona.
08.0 MYYNTILUVAN NUMERO
ZELITREX 250 mg Kalvopäällysteiset tabletit - 60 tablettia A.I.C .: 029503048
ZELITREX 500 mg Kalvopäällysteiset tabletit - 42 tablettia A.I.C .: 029503012
ZELITREX 500 mg Kalvopäällysteiset tabletit - 10 tablettia A.I.C .: 029503036
ZELITREX 1000 mg Kalvopäällysteiset tabletit - 21 tablettia A.I.C .: 029503024
09.0 MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ
42 tablettia 500 mg - 21 tablettia 1000 mg: 19. tammikuuta 1998 / marraskuu 2002
60 tablettia 250 mg -10 tablettia 500 mg: 9. toukokuuta 2002 / marraskuu 2002
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
23. syyskuuta 2011