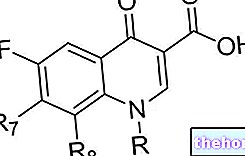
kalsiumia ja epäorgaanisia happoja, kuten esimerkiksi typpihappoa, suolahappoa tai rikkihappoa. Alla on kemiallinen reaktio, joka sisältää tämän viimeisen hapon käytön:
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
Lämpöprosessi puolestaan käsittää fosforihappoanhydridin saamisen alkuainefosforista alkaen. Kun anhydridi on muodostunut, se on hydratoitava, kunnes saadaan ortofosforihappoa, kuten seuraavassa reaktiossa esitetään:
P2O5 + 3 H2O → 2 H3PO4
Tämä jälkimmäinen prosessi johtaa yleensä puhtaampaan ortofosforihappoon kuin märkäprosessi.
ympäristön kannalta, se näyttää valkoisena kiinteänä aineena, joka sulaa noin 42 ° C: n lämpötilassa.
Kuitenkin fosforihappoa markkinoidaan yleensä tiivistetyn 85% vesiliuoksen muodossa. Se on väritön, hajuton ja haihtumaton liuos, mutta syövyttävä ja koostumukseltaan melko tiheä, lähes "siirappimainen".
Sen lisäksi, että ortofosforihappo liukenee veteen, se liukenee myös etanoliin.
kapselien, siltojen, viilujen, täytteiden jne. sementtimateriaalien tarttumisen edistämiseksi. Tässä yhteydessä ortofosforihappoa käytetään yleensä 37% liuoksissa.









.jpg)