Vaikuttavat aineet: Valsartaani, hydroklooritiatsidi
Combisartan 80 mg / 12,5 mg kalvopäällysteiset tabletit
Combisartan 160 mg / 12,5 mg kalvopäällysteiset tabletit
Combisartan 160 mg / 25 mg kalvopäällysteiset tabletit
Combisartan 320 mg / 12,5 mg kalvopäällysteiset tabletit
Combisartan 320 mg / 25 mg kalvopäällysteiset tabletit
Käyttöaiheet Miksi Combisartania käytetään? Mitä varten se on?
Kalvopäällysteiset Combisartan-tabletit sisältävät kahta vaikuttavaa ainetta, nimeltään valsartaani ja hydroklooritiatsidi. Molemmat aineet auttavat hallitsemaan korkeaa verenpainetta (kohonnutta verenpainetta).
- Valsartaani kuuluu lääkeryhmään, joka tunnetaan nimellä "angiotensiini II -reseptorin salpaajat", jotka auttavat hallitsemaan korkeaa verenpainetta. Valsartaani estää angiotensiini II: n vaikutuksen. Seurauksena on, että verisuonet rentoutuvat ja verenpaine laskee.
- Hydroklooritiatsidi kuuluu tiatsididiureettien lääkeryhmään.
- Hydroklooritiatsidi lisää eliminoituneen virtsan määrää ja alentaa näin verenpainetta.
Combisartaania käytetään korkean verenpaineen hoitoon, kun verenpainetta ei saada riittävästi hallintaan yhdellä lääkkeellä.
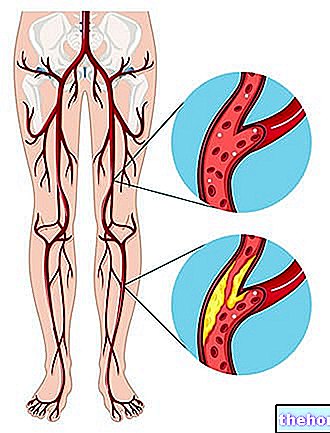
Kun verenpaine on korkea, sydämen ja valtimoiden työmäärä kasvaa. Jos sitä ei käsitellä, se voi vahingoittaa aivojen, sydämen ja munuaisten verisuonia ja johtaa aivohalvaukseen, sydämen vajaatoimintaan tai munuaisten vajaatoimintaan. Korkea verenpaine lisää sydänkohtauksen riskiä. Verenpaineen palauttaminen normaaliksi vähentää näiden sairauksien kehittymisen riskiä.
Vasta -aiheet Milloin Combisartania ei tule käyttää
Älä ota Combisartania
- jos olet allerginen (yliherkkä) valsartaanille, hydroklooritiatsidille, sulfonamidijohdannaisille (hydroklooritiatsidille kemiallisesti samankaltaiset aineet) tai Combisartan -valmisteen jollekin muulle aineelle (lueteltu kohdassa 6)
- jos olet yli 3 kuukautta raskaana (on myös parempi välttää Combisartan Accord -valmistetta raskauden alkuvaiheessa - katso kohta Raskaus)
- jos sinulla on vakavia maksavaivoja, maksan pienten sappikanavien tuhoutuminen (sappikirroosi), joka johtaa sapen kertymiseen maksaan (kolestaasi)
- jos sinulla on vakavia munuaisongelmia
- jos et voi virtsata (anuria)
- jos sinua hoidetaan keinotekoisella munuaisella
- jos veren kalium- tai natriumpitoisuus on normaalia alhaisempi tai jos veren kalsiumpitoisuus on normaalia korkeampi hoidosta huolimatta
- jos sinulla on kihti
- jos sinulla on diabetes tai munuaisten vajaatoiminta ja sinua hoidetaan verenpainetta alentavalla lääkkeellä, joka sisältää aliskireenia.
Jos jokin näistä koskee sinua, älä ota tätä lääkettä ja ota yhteys lääkäriisi.
Käyttöä koskevat varotoimet Mitä sinun on tiedettävä, ennen kuin otat Combisartan Orion -tabletteja
Ole erityisen varovainen Combisartanin suhteen
- jos käytät kaliumia säästäviä lääkkeitä, kaliumlisiä, kaliumia sisältäviä suolan korvikkeita tai muita veren kaliumpitoisuutta lisääviä lääkkeitä, kuten hepariinia.Lääkärisi saattaa joutua tarkistamaan veren kaliumpitoisuus säännöllisin väliajoin.
- jos veren kaliumpitoisuus on alhainen
- jos sinulla on ripuli tai voimakas oksentelu
- jos käytät suuria annoksia nesteitä poistavia lääkkeitä (diureetteja)
- jos sinulla on vakavia sydänvaivoja
- jos sinulla on sydämen vajaatoiminta tai sinulla on ollut sydänkohtaus. Noudata huolellisesti lääkärin ohjeita hoidon aloitusannoksesta. Lääkäri tarkistaa myös munuaistesi toiminnan.
- jos kärsit munuaisvaltimon kaventumisesta
- jos olet äskettäin saanut uuden munuaisen
- jos sinulla on hyperaldosteronismi, sairaus, jossa lisämunuaiset tuottavat liikaa aldosteronihormonia. Jos tämä koskee sinua, Combisartan -valmisteen käyttöä ei suositella
- jos sinulla on maksa- tai munuaissairaus
- jos sinulla on joskus ollut kielen ja kasvojen turvotusta angioedeemaksi kutsutun allergisen reaktion aikana, kun käytät muita lääkkeitä (mukaan lukien ACE: n estäjät), kerro siitä lääkärillesi. Jos näitä oireita ilmenee Combisartan Accord -hoidon aikana, lopeta Combisartan Accord -valmisteen käyttö välittömästi äläkä ota sitä uudelleen. Katso kohta 4, "Mahdolliset haittavaikutukset"
- jos sinulla on kuumetta, ihottumaa ja nivelkipua, jotka voivat olla merkkejä systeemisestä lupus erythematosuksesta (SLE, ns. autoimmuunisairaus)
- jos sinulla on diabetes, kihti, korkea kolesteroli- tai triglyseridipitoisuus veressä
- jos sinulla on ollut allergisia reaktioita muiden saman luokan verenpainetta alentavien lääkkeiden (angiotensiini II -reseptorin salpaajat) käyttöön tai jos sinulla on allergia tai astma.
- jos sinulla on heikentynyt näkö tai silmäkipu. Nämä voivat olla oireita "kohonneesta silmänpaineesta ja voivat ilmetä muutamasta tunnista viikkoon Combisartan Accord -valmisteen ottamisen jälkeen. Jos sitä ei hoideta, se voi johtaa pysyvään näön menetykseen. Jos olet aiemmin ollut allerginen penisilliineille tai sulfonamideille. kehittää tätä häiriötä
- se voi aiheuttaa ihon herkkyyden auringolle
- jos käytät jotakin seuraavista korkean verenpaineen hoitoon käytettävistä lääkkeistä: - "ACE: n estäjä" (esimerkiksi enalapriili, lisinopriili, ramipriili), erityisesti jos sinulla on diabetekseen liittyviä munuaisongelmia. - aliskireeni
- jos saat ACE: n estäjää yhdessä muiden sydämen vajaatoiminnan hoitoon käytettävien lääkkeiden kanssa, jotka tunnetaan mineralokortikoidireseptorin salpaajina (esim. spironolaktoni, eplerenoni) tai beetasalpaajina (esim. metoprololi).
Lääkärisi voi tarkistaa munuaistesi toiminnan, verenpaineen ja elektrolyyttien (esimerkiksi kaliumin) määrän veressäsi säännöllisin väliajoin.
Katso myös tiedot kohdasta "Älä ota Combisartania".
Jos jokin näistä koskee sinua, ota yhteys lääkäriisi.
Combisartaania ei suositella lapsille ja nuorille (alle 18 -vuotiaille).
Kerro lääkärillesi, jos epäilet olevasi raskaana (tai jos sinulla on mahdollisuus tulla raskaaksi). Combisartaania ei suositella raskauden alkuvaiheessa eikä sitä saa käyttää, jos olet yli 3 kuukautta raskaana, koska se voi aiheuttaa vakavaa haittaa lapsellesi, jos sitä käytetään tässä vaiheessa (ks. Kohta Raskaus).
Yhteisvaikutukset Mitkä lääkkeet tai elintarvikkeet voivat muuttaa Combisartan Orion -valmisteen vaikutusta
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt.
Hoidon vaikutukseen voi vaikuttaa, jos Combisartan Krka -tabletteja käytetään yhdessä tiettyjen muiden lääkkeiden kanssa.
Voi olla tarpeen muuttaa annosta, ryhtyä muihin varotoimiin tai joissakin tapauksissa lopettaa jonkin lääkkeen käyttö. Tämä koskee erityisesti seuraavia lääkkeitä:
- litium, lääke, jota käytetään tietyntyyppisten psyykkisten häiriöiden hoitoon
- lääkkeitä tai aineita, jotka voivat lisätä veren kaliumpitoisuutta. Näitä ovat kaliumlisät tai kaliumia sisältävät suolan korvikkeet, kaliumia säästävät lääkkeet ja hepariini
- lääkkeet, jotka voivat vähentää veren kaliumpitoisuutta, kuten diureetit (lääkkeet, jotka lisäävät nesteiden poistumista), kortikosteroidit, laksatiivit, karboksoloni, amfoterisiini tai penisilliini G.
- jotkin antibiootit (rifampisiiniryhmä), elinsiirron hyljintää vastaan käytettävä lääke (syklosporiini) ja antiretroviraalinen lääke, jota käytetään HIV / AIDS -infektioiden hoitoon (ritonaviiri). Nämä lääkkeet voivat lisätä Combisartan Orion -valmisteen vaikutusta
- lääkkeet, jotka voivat aiheuttaa kääntyvien kärkien takykardiaa (epäsäännöllinen syke), kuten rytmihäiriölääkkeet (sydänsairauksien lääkkeet) ja jotkin psykoosilääkkeet.
- lääkkeet, jotka voivat vähentää veren natriumpitoisuutta, kuten masennuslääkkeet, psykoosilääkkeet, epilepsialääkkeet
- kihdin hoitoon käytettävät lääkkeet, kuten allopurinoli, probenesidi, sulfiinipyratsoni
- terapeuttinen D -vitamiini ja kalsiumlisät,
- diabeteslääkkeet (suun kautta, kuten metformiini tai insuliinit)
- muut verenpainetta alentavat lääkkeet, mukaan lukien metyylidopa, ACE: n estäjät (kuten enalapriili, lisinopriili jne.) tai aliskireeni (katso myös tiedot kohdista "Älä käytä Combisartania" ja "Ole erityisen varovainen Combisartanin suhteen").
- verenpainetta nostavat lääkkeet, kuten norepinefriini ja adrenaliini
- digoksiini tai muut digitalisglykosidit (sydänongelmien hoitoon käytettävät lääkkeet)
- lääkkeet, jotka voivat nostaa verensokeria, kuten diatsoksidi tai beetasalpaajat
- sytotoksiset lääkkeet (käytetään syövän hoitoon), kuten metotreksaatti tai syklofosfamidi
- kipulääkkeet, kuten ei-steroidiset tulehduskipulääkkeet (NSAID), mukaan lukien selektiiviset syklo-oksigenaasi-2-estäjät (Cox-2) ja asetyylisalisyylihappo> 3 g
- lihaksia rentouttavia lääkkeitä, kuten tubokurariini
- antikolinergiset lääkkeet,
- amantadiini (lääke, jota käytetään Parkinsonin taudin hoitoon ja myös tiettyjen virusten aiheuttamien sairauksien hoitoon tai ehkäisyyn)
- kolestyramiini ja kolestipoli (lääkkeitä, joita käytetään pääasiassa veren korkean lipidipitoisuuden hoitoon)
- siklosporiini, lääke, jota käytetään elinsiirroissa elinten hyljinnän estämiseksi
- alkoholi, unilääkkeet ja anestesia-aineet (lääkkeet, joilla on huumaavaa tai kipua lievittävää vaikutusta ja joita käytetään esimerkiksi leikkauksen aikana)
- jodipitoiset varjoaineet (käytetään radiologisiin tutkimuksiin)
Combisartanin ottaminen ruoan ja juoman kanssa
Combisartaani voidaan ottaa ruoan kanssa tai ilman. Vältä alkoholin käyttöä, ellet ole ensin keskustellut lääkärisi kanssa. Alkoholi voi edelleen alentaa verenpainetta ja / tai lisätä huimauksen tai pyörtymisen riskiä.
Varoitukset On tärkeää tietää, että:
Raskaus ja imetys
Kysy lääkäriltäsi tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
- Sinun on kerrottava lääkärillesi, jos epäilet olevasi raskaana (tai jos sinulla on mahdollisuus tulla raskaaksi) .Lääkärisi yleensä neuvoo sinua lopettamaan Combisartan Accord -valmisteen käytön ennen raskautta tai heti kun tiedät olevasi raskaana ja Kombisartaania ei suositella raskauden alkuvaiheessa eikä sitä saa käyttää, jos olet yli 3 kuukautta raskaana, koska se voi aiheuttaa vakavaa haittaa lapselle, jos sitä käytetään kolmannen raskauskuukauden jälkeen.
- Kerro lääkärillesi, jos imetät tai aiot imettää Combisartania ei suositella imettäville naisille.
Ajaminen ja koneiden käyttö
Ennen kuin ajat autoa, käytät koneita tai suoritat muita keskittymistä vaativia toimintoja, sinun on tiedettävä reaktiosi Combisartan -valmisteen kanssa. Kuten monet muut korkean verenpaineen hoitoon käytettävät lääkkeet, Combisartan Accord voi harvinaisissa tapauksissa aiheuttaa huimausta ja vaikuttaa keskittymiskykyyn.
Niille, jotka harjoittavat urheilutoimintaa: lääkkeen käyttö ilman terapeuttista tarvetta on dopingia ja voi joka tapauksessa määrittää positiivisen dopingtestin.
Annos, antotapa ja antamisaika Miten Combisartaania käytetään: Annostus
Ota Combisartania aina juuri sen verran kuin lääkäri on määrännyt. Tämä auttaa sinua saamaan parempia tuloksia ja vähentämään sivuvaikutusten riskiä.Jos olet epävarma, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Ne, joilla on korkea verenpaine, eivät useinkaan huomaa merkkejä tästä ongelmasta, ja monet tuntevat olonsa normaaliksi. Tästä syystä on erittäin tärkeää, että pidät säännöllisiä tapaamisia lääkärisi kanssa, vaikka olosi olisikin hyvä.
Lääkärisi kertoo sinulle tarkasti, kuinka monta Combisartan -tablettia sinun tulee ottaa. Hoitovasteesi perusteella lääkäri voi ehdottaa suurempaa tai pienempää annosta.
- Tavanomainen Combisartan -annos on yksi tabletti päivässä.
- Älä muuta annostasi tai lopeta tablettien käyttöä keskustelematta ensin lääkärisi kanssa.
- Tämä lääke on otettava samaan aikaan joka päivä, yleensä aamulla.
- Voit ottaa Combisartan ratiopharmin ruoan kanssa tai ilman.
- Niele tabletti vesilasillisen kanssa.
Jos unohdat ottaa Combisartan Orion -tabletteja
Jos unohdat ottaa annoksen, ota se heti kun muistat sen. Jos kuitenkin on melkein seuraavan annoksen aika, jätä unohtunut annos väliin.
Älä ota kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos lopetat Combisartanin käytön
Combisartan -hoidon lopettaminen voi aiheuttaa korkean verenpaineen pahenemista.
Älä lopeta lääkkeen käyttöä, ellei lääkäri niin kehota.
Jos sinulla on kysymyksiä tämän tuotteen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Yliannostus Mitä tehdä, jos olet ottanut yliannoksen Combisartan Orion -tabletteja
Vaikean huimauksen ja / tai pyörtymisen sattuessa on parasta maata ja ottaa välittömästi yhteys lääkäriisi.
Jos olet vahingossa ottanut liian monta tablettia, ota yhteys lääkäriisi, apteekkiin tai sairaalaan.
Sivuvaikutukset Mitkä ovat Combisartaanin sivuvaikutukset
Kuten kaikki lääkkeet, Combisartan voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Näitä haittavaikutuksia voi esiintyä tietyillä esiintymistiheyksillä, jotka määritellään seuraavasti:
- hyvin yleinen: esiintyy useammalla kuin yhdellä käyttäjällä 10: stä
- yleinen: esiintyy 1--10 käyttäjällä 100: sta
- melko harvinainen: esiintyy 1--10 käyttäjällä 1000: sta
- harvinainen: esiintyy 1--10 käyttäjällä 10000: sta
- hyvin harvinainen: esiintyy alle yhdellä käyttäjällä 10000: sta
- tuntematon: esiintymistiheyttä ei voida arvioida saatavilla olevien tietojen perusteella.
Jotkut haittavaikutukset voivat olla vakavia ja vaatia välitöntä lääkärinhoitoa.
Ota heti yhteys lääkäriisi, jos sinulla on angioedeeman oireita, kuten:
- kasvojen, kielen tai nielun turvotus
- nielemisvaikeudet
- nokkosihottuma ja hengitysvaikeudet
Jos sinulla ilmenee jokin näistä oireista, lopeta Combisartan Orion -tablettien käyttö ja ota välittömästi yhteys lääkäriisi (ks. Myös kohta 2 "Ole erityisen varovainen Combisartan -valmisteen suhteen").
Muita haittavaikutuksia ovat:
Melko harvinainen
- yskä
- alhainen paine
- pyörrytystä
- nestehukka (oireita kuten jano, suun ja kielen kuivuminen, harvinainen virtsa, tumma virtsa, kuiva iho)
- lihaskipu
- väsymys
- pistely tai tunnottomuus
- näön hämärtyminen
- ääniä korvissa (esim. soittoäänet, vilinä)
Erittäin harvinainen
- huimaus
- ripuli
- nivelkipu
Ei tunnettu
- hengitysvaikeudet
- havaittavissa oleva virtsamäärän lasku
- alhainen veren natriumpitoisuus (joka voi aiheuttaa väsymystä, sekavuutta, lihasten nykimistä ja / tai kouristuksia vaikeissa tapauksissa)
- alhainen veren kaliumpitoisuus (joskus lihasheikkoutta, lihaskouristuksia, epänormaalia sydämen rytmiä)
- alhainen valkosolujen määrä (oireita kuten kuume, ihoinfektiot, infektioiden aiheuttama kurkkukipu tai suun haavaumat, heikkous)
- kohonnut bilirubiinipitoisuus veressä (mikä voi vaikeissa tapauksissa aiheuttaa ihon ja silmien keltaisuutta)
- veren ureatypen ja kreatiniinipitoisuuden nousu (mikä voi viitata munuaisten vajaatoimintaan)
- kohonnut virtsahappopitoisuus veressä (mikä voi vaikeissa tapauksissa aiheuttaa kihtiä)
- pyörtyminen (pyörtyminen)
Seuraavia haittavaikutuksia on raportoitu pelkästään valsartaania tai hydroklooritiatsidia sisältävien lääkkeiden yhteydessä:
Valsartaani
Melko harvinainen
- pyörrytyksen tunne
- vatsakipu
Ei tunnettu
- ihon rakkulat (rakkulaisen ihottuman merkki)
- ihottuma, johon liittyy kutinaa tai ilman kutinaa, sekä joitakin seuraavista oireista: kuume, nivelkipu, lihaskipu, imusolmukkeiden turvotus ja / tai flunssan kaltaiset oireet
- ihottuma, puna-violetit täplät, kuume, kutina (verisuonitulehduksen oireet)
- alhainen verihiutaleiden määrä veressä (joskus epätavallista verenvuotoa tai mustelmia)
- kohonnut veren kaliumpitoisuus (joskus lihaskouristuksia, epänormaalia sydämen rytmiä)
- allergiset reaktiot (oireina kuten ihottuma, kutina, nokkosihottuma, hengitys- tai nielemisvaikeudet, huimaus)
- turvotus pääasiassa kasvoissa ja kurkussa, ihottuma, kutina
- maksan toiminta -arvojen nousu
- hemoglobiiniarvojen lasku ja punasolujen prosenttiosuus veressä (mikä voi vaikeissa tapauksissa johtaa anemiaan)
- munuaisten vajaatoiminta
- alhainen veren natriumpitoisuus (joka voi aiheuttaa väsymystä, sekavuutta, lihasten nykimistä ja / tai kouristuksia vaikeissa tapauksissa)
Hydroklooritiatsidi
Erittäin yleinen
- alhainen veren kaliumpitoisuus
- veren rasva -arvojen nousu
yleinen
- alhainen veren natriumpitoisuus
- veren alhainen magnesiumpitoisuus
- korkea virtsahappopitoisuus veressä
- kutiava ihottuma tai muu ihottuma
- vähentynyt ruokahalu
- lievä pahoinvointi ja oksentelu
- huimaus, pyörtyminen pystyasennossa
- kyvyttömyys saavuttaa tai ylläpitää erektiota
Harvinainen
- ihon turvotus ja rakkulat (johtuen "lisääntyneestä auringon herkkyydestä")
- korkea kalsiumpitoisuus veressä
- korkea verensokeri
- sokeria virtsassa
- diabeteksen metabolisen tilan paheneminen
- ummetus, ripuli, vatsavaivat tai suolet, maksavaivat, joita voi esiintyä ihon tai silmien keltaisuudessa
- epäsäännöllinen syke
- päänsärky
- univaikeudet
- suru (masennus)
- alhainen verihiutaleiden määrä (joskus verenvuotoa tai mustelmia ihon alla)
- huimaus
- pistely tai tunnottomuus
- näköhäiriöt
Erittäin harvinainen
- verisuonitulehdus, johon liittyy oireita, kuten ihottuma, purppuranpunaiset täplät, kuume (vaskuliitti)
- ihottuma, kutina, nokkosihottuma, hengitys- tai nielemisvaikeudet, huimaus (yliherkkyysreaktiot)
- vaikeat iho -oireet, jotka aiheuttavat ihottumaa, ihon punoitusta, rakkuloita huulilla, silmissä tai suussa, ihon hilseilyä, kuumetta (toksinen epidermaalinen nekrolyysi)
- kasvojen ihottuma, nivelkipu, lihassairaudet, kuume (lupus erythematosus)
- voimakas ylävatsakipu (haimatulehdus)
- hengitysvaikeudet, joihin liittyy kuumetta, yskää, hengityksen vinkumista, hengenahdistusta (hengitysvaikeuksia, mukaan lukien keuhkokuume ja keuhkopöhö)
- kuume, kurkkukipu, usein esiintyvät infektiot (agranulosytoosi)
- vaalea iho, väsymys, hengenahdistus, tumma virtsa (hemolyyttinen anemia)
- infektioiden aiheuttama kuume, kurkkukipu tai suun haavaumat (leukopenia)
- sekavuus, väsymys, lihasten vapina tai kouristus, hengenahdistus (hypokloreeminen alkaloosi)
Ei tunnettu
- väsymys, mustelmat ja usein esiintyvät infektiot (aplastinen anemia)
- virtsamäärän voimakas väheneminen (mahdollinen merkki munuaissairaudesta tai munuaisten vajaatoiminnasta)
- heikentynyt näkö tai silmän kipu korkean silmänpaineen vuoksi (mahdollinen merkki akuutista kapeakulmaisesta glaukoomasta)
- ihottuma, ihon punoitus, rakkuloita huulilla, silmissä tai suussa, ihon kuorinta, kuume (mahdollisia oireita erythema multiforme)
- lihaskouristus
- kuume (kuume)
- heikkous (astenia)
Jos havaitset sellaisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa, kerro niistä lääkärille tai apteekkihenkilökunnalle.
Vanhentuminen ja säilyttäminen
- Pidä Combisartan poissa lasten ulottuvilta ja näkyviltä.
- Älä käytä Combisartania etiketissä mainitun viimeisen käyttöpäivämäärän jälkeen.
- Säilytä alle 30 ° C. Säilytä alkuperäispakkauksessa.Herkkä kosteudelle.
- Älä käytä Combisartania, jos huomaat pakkauksen olevan vaurioitunut tai siinä on merkkejä väärentämisestä.
- Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy apteekista, kuinka heittää pois käyttämättömät lääkkeet. Tämä auttaa suojelemaan ympäristöä.
Määräaika "> Muut tiedot
Mitä Combisartan sisältää
- Vaikuttavat aineet ovat valsartaani ja hydroklooritiatsidi. Yksi kalvopäällysteinen tabletti sisältää 80 mg, 160 mg tai 320 mg valsartaania ja 12,5 mg tai 25 mg hydroklooritiatsidia.
- Tabletin ydin sisältää mikrokiteistä selluloosaa, krospovidonia, vedetöntä kolloidista piidioksidia, magnesiumstearaattia.
- Tabletin päällyste sisältää hypromelloosia, makrogolia 8000 (vain 80 mg / 12,5 mg ja 160 mg / 12,5 mg), makrogolia 4000 (vain 160 mg / 25 mg, 320 mg / 12,5 mg ja 320 mg / 25) mg), talkkia, punaista rautaoksidi (E172, paitsi 320 mg / 25 mg), keltainen rautaoksidi (E172, vain 80 mg / 12,5 mg, 160 mg / 12,5 mg ja 320 mg / 12,5 mg) mg), musta rautaoksidi (E172, vain 160 mg) / 25 mg ja 320 mg / 12,5 mg), titaanidioksidi (E171).
Kuvaus Combisartan -valmisteen ulkonäöstä ja pakkauksen sisällöstä
- Combisartan 80 mg / 12,5 mg kalvopäällysteiset tabletit ovat vaalean oranssia, soikeita, ja niiden toisella puolella on merkintä "HGH" ja toisella puolella "CG" tai "HGH".
- Combisartan 160 mg / 12,5 mg kalvopäällysteiset tabletit ovat tummanpunaisia, soikeita, ja niiden toisella puolella on merkintä "HHH" ja toisella puolella "CG" tai "HHH".
- Combisartan 160 mg / 25 mg kalvopäällysteiset tabletit ovat ruskeita, soikeita, ja niiden toisella puolella on merkintä "HXH" ja toisella puolella "NVR" tai "HXH".
- Combisartan 320 mg / 12,5 mg kalvopäällysteiset tabletit ovat vaaleanpunaisia, soikeita, viistettyjä reunoja, joissa on kaiverrus "NVR" toisella puolella ja "HIL" toisella puolella tai "HIL" vain toisella puolella.
- Combisartan 320 mg / 25 mg kalvopäällysteiset tabletit ovat keltaisia, soikeita, toisella puolella on merkintä "CTI" ja toisella puolella "NVR" tai toisella puolella "CTI".
Combisartan 80 mg / 12,5 mg tabletteja on saatavana kalenteriläpipainopakkauksissa 14 tai 28 tabletin pakkauksissa.
Combisartan 160 mg / 12,5 mg, 160 mg / 25 mg, 320 mg / 12,5 mg ja 320 mg / 25 mg tabletteja on saatavana kalenteriläpipainopakkauksissa, 7 pakkauksessa (vain 320 mg / 12,5 mg ja 320 mg / 25 mg), 14, 28, 56, 98 tai 280 tablettia.
Saatavana on myös jaettavissa olevia kerta -annospakkauksia, joissa on 56x1 (vain 320 mg / 12,5 ja 320 mg / 25 mg), 98x1 (paitsi 80 mg / 12,5) tai 280x1 (vain 320 mg / 12,5 ja 320 mg / 25 mg) tabletit. .
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Alkuperäinen pakkausseloste: AIFA (Italian lääkevirasto). Sisältö julkaistu tammikuussa 2016. Esitetyt tiedot eivät välttämättä ole ajan tasalla.
Jotta saat käyttöösi uusimman version, on suositeltavaa käyttää AIFA: n (Italian Medicines Agency) verkkosivustoa. Vastuuvapauslauseke ja hyödyllistä tietoa.
01.0 LÄÄKEVALMISTEEN NIMI -
COMBISARTAN 160 MG / 12,5 MG TABLETTI, PÄÄLLYTETTY KALVOLLA
02.0 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS -
Yksi tabletti sisältää 160 mg valsartaania ja 12,5 mg hydroklooritiatsidia.
Täydellinen apuaineluettelo, katso kohta 6.1.
03.0 LÄÄKEMUOTO -
Kalvopäällysteinen tabletti.
Tummanpunainen, soikea tabletti, johon on kaiverrettu kirjaimet "HHH" ja "CG" toiselle puolelle tai kaiverrettu kirjaimilla "HHH" vain toiselle puolelle.
04.0 KLIINISET TIEDOT -
04.1 Käyttöaiheet -
Essentiaalisen valtimon verenpaineen hoito aikuisilla.
Combisartaani on kiinteä yhdistelmä, joka on tarkoitettu potilaille, joiden verenpainetta ei saada riittävästi hallintaan valsartaanin tai hydroklooritiatsidin monoterapialla.
04.2 Annostus ja antotapa -
Annostus
Suositeltu annos Combisartan 160 mg / 12,5 mg on yksi kalvopäällysteinen tabletti kerran vuorokaudessa. Annoksen titrausta yksittäisten komponenttien kanssa suositellaan. Kussakin tapauksessa yksittäiset komponentit on titrattava seuraavaan annokseen hypotension ja muiden haittatapahtumien riskin pienentämiseksi.
Jos kliinisesti on tarkoituksenmukaista, potilailla, joiden verenpainetta ei saada riittävästi hallintaan valsartaani- tai hydroklooritiatsidi -monoterapialla, voidaan harkita suoraa siirtymistä monoterapiasta kiinteään yhdistelmään edellyttäen, että noudatetaan yksittäisten komponenttien suositeltua annoksen titrausjärjestystä.
Kliininen vaste Combisartaanille on arvioitava hoidon aloittamisen jälkeen, ja jos verenpaine pysyy hallinnassa, jommankumman komponentin annosta voidaan nostaa enintään 320 mg / 25 mg: n Combisartan -annokseen.
Verenpainetta alentava vaikutus ilmenee olennaisesti kahden viikon kuluessa.
Suurin osa potilaista saavuttaa suurimman vaikutuksen 4 viikon kuluessa, mutta joillekin potilaille saattaa olla tarpeen 4-8 viikon hoito, joka on otettava huomioon annosta titrattaessa.
Antotapa
Combisartaani voidaan ottaa ruoan kanssa tai ilman, ja se tulee antaa veden kanssa.
Erityisryhmät
Munuaisvaurio
Annosta ei tarvitse muuttaa potilailla, joilla on lievä tai kohtalainen munuaisten vajaatoiminta (glomerulusten suodatusnopeus ≥ 30 ml / min). Hydroklooritiatsidikomponentin vuoksi Combisartan Sandoz on vasta -aiheinen potilaille, joilla on vaikea munuaisten vajaatoiminta (glomerulusten suodatusnopeuden anuria (ks. Kohdat 4.3, 4.4 ja 5.2).
Maksan vajaatoiminta
Potilailla, joilla on lievä tai kohtalainen maksan vajaatoiminta ilman kolestaasia, valsartaaniannos ei saa ylittää 80 mg (ks. Kohta 4.4). Hydroklooritiatsidin annosta ei tarvitse muuttaa potilailla, joilla on lievä tai kohtalainen maksan vajaatoiminta. Valsartaanikomponentin vuoksi Combisartaani on vasta -aiheinen potilaille, joilla on vaikea maksan vajaatoiminta tai sappikirroosi ja kolestaasi (ks. Kohdat 4.3, 4.4 ja 5.2).
Eläkeläiset
Iäkkäiden potilaiden annosta ei tarvitse muuttaa.
Pediatriset potilaat
Kombisartaania ei suositella käytettäväksi alle 18 -vuotiaille lapsille, koska tiedot turvallisuudesta ja tehosta puuttuvat.
04.3 Vasta -aiheet -
• Yliherkkyys valsartaanille, hydroklooritiatsidille, muille sulfonamidijohdannaisia sisältäville lääkkeille tai apuaineille.
• Raskauden toinen ja kolmas kolmannes (ks. Kohdat 4.4 ja 4.6).
• Vaikea maksan vajaatoiminta, sappikirroosi ja kolestaasi.
• Vaikea munuaisvaurio (kreatiniinipuhdistuma
• Tulenkestävä hypokalemia, hyponatremia, hyperkalsemia ja oireinen hyperurikemia.
• Combisartaanin ja aliskireenia sisältävien lääkkeiden samanaikainen käyttö on vasta-aiheista potilailla, joilla on diabetes mellitus tai munuaisten vajaatoiminta (glomerulusten suodatusnopeus GFR)
04.4 Varoitukset ja käyttöön liittyvät varotoimet -
Muutokset seerumin elektrolyytteissä
Valsartaani
Kaliumlisien, kaliumia säästävien diureettien, kaliumia sisältävien suolan korvikkeiden tai muiden kaliumpitoisuutta nostavien aineiden (hepariini jne.) Samanaikaista käyttöä ei suositella. Veren kaliumpitoisuuksia on seurattava asianmukaisesti.
Hydroklooritiatsidi
Hypokalemiaa on raportoitu tiatsididiureettien, myös hydroklooritiatsidihoidon aikana.Seerumin kaliumpitoisuuden säännöllistä seurantaa suositellaan.
Tiatsididiureettien, mukaan lukien hydroklooritiatsidi, hoitoon on liittynyt hyponatremiaa ja hypokloreemista alkaloosia.Tiatsidit, mukaan lukien hydroklooritiatsidi, lisäävät magnesiumin erittymistä virtsaan ja siksi voi ilmetä hypomagnesemiaa.Tiatsididiureetit voivat vähentää tätä ja aiheuttaa hyperkalsemiaa.
Kuten kaikilla diureettihoitoa saavilla potilailla, seerumin elektrolyyttien määrä on seurattava säännöllisin väliajoin.
Natrium- ja / tai tilavuuspotilaat
Tiatsididiureetteja, mukaan lukien hydroklooritiatsidi, käyttäviä potilaita on tarkkailtava neste- tai elektrolyyttitasapainon kliinisten oireiden varalta.
Potilailla, joilla on suuri natrium- ja / tai tilavuushäiriö, kuten suuret diureettiannokset, voi harvinaisissa tapauksissa ilmetä oireista hypotensiota Combisartan -hoidon aloittamisen jälkeen. .
Potilaat, joilla on vaikea krooninen sydämen vajaatoiminta tai muut reniini-angiotensiini-aldosteronijärjestelmää stimuloivat tilat
Potilailla, joiden munuaisten toiminta voi olla riippuvainen reniini-angiotensiini-aldosteronijärjestelmän aktiivisuudesta (esim. Potilaat, joilla on vaikea kongestiivinen sydämen vajaatoiminta), angiotensiiniä konvertoivan entsyymin estäjien hoitoon on liittynyt oliguriaa ja / tai etenevää atsotemiaa ja harvinaisissa tapauksissa , akuutti munuaisten vajaatoiminta ja / tai kuolema Sydämen vajaatoimintaa tai sydäninfarktia sairastavien potilaiden arviointiin on aina sisällyttävä munuaisten toiminnan tutkimus. Kombisartaanin käyttöä vaikeaa kroonista sydämen vajaatoimintaa sairastaville potilaille ei ole varmistettu, joten ei voida sulkea pois sitä mahdollisuutta, että reniini-angiotensiini-aldosteronijärjestelmän esteen vuoksi Combisartaanin käyttö voi myös liittyä munuaisten vajaatoimintaan. Kombisartaania ei tule käyttää näille potilaille.
Munuaisvaltimon ahtauma
Kombisartaania ei pidä käyttää verenpainelääkkeenä potilailla, joilla on yksipuolinen tai kahdenvälinen munuaisvaltimon ahtauma tai yksittäisen munuaisvaltimon ahtauma, koska BUN ja seerumin kreatiniini voivat nousta näillä potilailla.
Ensisijainen hyperaldosteronismi
Potilaita, joilla on primaarinen aldosteronismi, ei tule hoitaa Combisartan Accordilla, koska heidän reniini-angiotensiinijärjestelmänsä ei ole aktiivinen.
Aortta- ja mitraaliläpän ahtauma, obstruktiivinen hypertrofinen kardiomyopatia
Kuten kaikki muutkin verisuonia laajentavat aineet, erityistä varovaisuutta on noudatettava potilailla, jotka kärsivät aortan tai mitraalisen stenoosista tai obstruktiivisesta hypertrofisesta kardiomyopatiasta.
Munuaisten vajaatoiminta
Annosta ei tarvitse muuttaa potilailla, joilla on munuaisten vajaatoiminta ja kreatiniinipuhdistuma ≥ 30 ml / min (ks. Kohta 4.2). Seerumin kalium-, kreatiniini- ja virtsahappopitoisuuksien säännöllistä seurantaa suositellaan, kun Combisartania käytetään munuaisten vajaatoimintaa sairastaville potilaille.
Munuaissiirto
Tähän mennessä ei ole kokemusta Combisartanin turvallisesta käytöstä potilaille, joille on äskettäin tehty munuaisensiirto.
Maksan vajaatoiminta
Potilailla, joilla on lievä tai kohtalainen maksan vajaatoiminta ilman kolestaasia, Combisartaania tulee käyttää varoen (ks. Kohdat 4.2 ja 5.2). Tiatsididiureetteja tulee käyttää varoen potilailla, joilla on maksan vajaatoiminta tai etenevä maksasairaus, koska pienet muutokset nesteen ja elektrolyyttitasapainossa voivat aiheuttaa maksakooman.
Aiemmat angioedeeman jaksot
Valsartaania saaneilla potilailla on raportoitu angioedeemaa, johon liittyy kurkunpään ja kurkunpään suurentuminen, joka johtaa hengitysteiden tukkeutumiseen ja / tai kasvojen, huulten, nielun ja / tai kielen turpoamiseen; joillakin näistä potilaista oli aiemmin esiintynyt angioedeemaa muiden lääkkeiden, myös ACE: n estäjien, kanssa. Potilaille, joille kehittyy angioedeema, Combisartan -hoito on lopetettava välittömästi eikä sitä saa aloittaa uudelleen (ks. Kohta 4.8).
Systeeminen lupus erythematosus
Tiatsididiureettien, mukaan lukien hydroklooritiatsidi, on osoitettu pahentavan tai aktivoivan systeemistä lupus erythematosusta.
Muut aineenvaihduntahäiriöt
Tiatsididiureetit, mukaan lukien hydroklooritiatsidi, voivat heikentää glukoosinsietoa ja nostaa seerumin kolesteroli-, triglyseridi- ja virtsahappotasoja.
Tiatsidit voivat vähentää kalsiumin erittymistä virtsaan ja aiheuttaa lievää ja ajoittaista seerumin kalsiumpitoisuuden nousua, jos ei tunneta kalsiumin aineenvaihduntahäiriöitä. Merkittävä hyperkalsemia voi olla todiste taustalla olevasta hyperparatyreoosista. Ennen lisäkilpirauhasen toimintakokeiden suorittamista. Tiatsidihoito on lopetettava.
Valoherkkyys
Valoherkkyysreaktioita on raportoitu tiatsididiureettihoidon aikana (ks. Kohta 4.8). Jos valoherkkyysreaktioita ilmenee, hoito on suositeltavaa lopettaa. Jos diureetin antoa jatketaan tarpeellisena, on suositeltavaa suojata auringolle tai keinotekoisille UVA -säteille altistuneet osat.
Raskaus
Angiotensiini II -reseptorin salpaajahoitoa (AIIRA) ei saa aloittaa raskauden aikana. Raskautta suunnitteleville potilaille on käytettävä vaihtoehtoista verenpainelääkitystä, jonka turvallisuusprofiili on osoitettu raskauden aikana, ellei AIIRA -hoidon jatkamista pidetä välttämättömänä. Kun raskaus todetaan, AIIRA -hoito on lopetettava välittömästi ja tarvittaessa aloitettava vaihtoehtoinen hoito (ks. Kohdat 4.3 ja 4.6).
Yleistä
Erityistä varovaisuutta on noudatettava potilailla, joilla on aiemmin ollut yliherkkyysreaktioita muille angiotensiini II -reseptorin salpaajille.Yliherkkyysreaktiot hydroklooritiatsidille ovat todennäköisempiä allergikoille ja astmalle.
Akuutti sulkukulma-glaukooma
Hydroklooritiatsidiin, sulfonamidiin, on liittynyt omituinen reaktio, joka on johtanut vakavaan ohimenevään likinäköisyyteen ja akuuttiin kapeakulmaiseen glaukoomaan.Oireita ovat akuutti heikentynyt näöntarkkuus tai silmäkipu ja ilmaantuvat yleensä muutamassa tunnissa-viikossa hoidon aloittamisen jälkeen. hoitamaton, akuutti sulkukulma-glaukooma voi aiheuttaa pysyvän näköhäviön.
Ensisijainen hoito on "lopettaa hydroklooritiatsidin antaminen mahdollisimman nopeasti. Nopea lääketieteellinen tai kirurginen interventio voi olla tarpeen, jos silmänpaine pysyy hallinnassa. Akuutin kapeakulmaglaukooman kehittymisen riskitekijöitä voivat olla allergiat sulfonamidille tai penisilliinille.
Reniini-angiotensiini-aldosteronijärjestelmän (RAAS) kaksinkertainen saarto
On näyttöä siitä, että ACE: n estäjien, angiotensiini II -reseptorin salpaajien tai aliskireenin samanaikainen käyttö lisää hypotension, hyperkalemian ja heikentyneen munuaisten toiminnan riskiä (mukaan lukien akuutti munuaisten vajaatoiminta). Siksi RAAS: n kaksoissalpaa ACE: n estäjien, angiotensiini II -reseptorin salpaajien tai aliskireenin yhteiskäytön kautta ei suositella (ks. Kohdat 4.5 ja 5.1).
Jos kaksoissalpahoitoa pidetään ehdottoman välttämättömänä, se tulee tehdä vain erikoislääkärin valvonnassa ja tarkasti ja usein seuraamalla munuaisten toimintaa, elektrolyyttejä ja verenpainetta.
ACE: n estäjiä ja angiotensiini II -reseptorin salpaajia ei tule käyttää samanaikaisesti potilailla, joilla on diabeettinen nefropatia.
04.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset -
Yhteisvaikutukset, jotka liittyvät sekä valsartaaniin että hydroklooritiatsidiin
Yhteiskäyttöä ei suositella
Litium
Seerumin pitoisuuksien palautumista ja litiumin toksisuutta on raportoitu palautuvasti, kun litiumia annettiin samanaikaisesti ACE: n estäjien, angiotensiini II -reseptorin salpaajien tai tiatsidien kanssa, mukaan lukien hydroklooritiatsidi. Koska tiatsidit vähentävät litiumin munuaispuhdistumaa, litiummyrkyllisyyden riski voi oletettavasti edelleen kasvaa Combisartan Accord -hoidon aikana.Jos yhdistelmän käyttö osoittautuu tarpeelliseksi, seerumin litiumpitoisuuksien tarkka seuranta on suositeltavaa.
Samanaikainen käyttö vaatii varovaisuutta
Muut verenpainelääkkeet
Kombisartaani voi tehostaa muiden verenpainetta alentavia aineita (esim. Guanetidiini, metyylidopa, vasodilataattorit, ACE: n estäjät, angiotensiinireseptorin salpaajat, beetasalpaajat, kalsiumkanavan salpaajat ja reniinin estäjät).
Painemiinit (esim. adrenaliini, noradrenaliini)
Puristusamiinien vasteen heikkeneminen on mahdollista. Tämän vaikutuksen kliininen merkitys on epävarma eikä riitä estämään niiden käyttöä.
Ei-steroidiset tulehduskipulääkkeet (NSAID), mukaan lukien selektiiviset COX-2-estäjät, asetyylisalisyylihappo (> 3 g / vrk) ja ei-selektiiviset tulehduskipulääkkeet
Samanaikaisesti annetut tulehduskipulääkkeet voivat heikentää sekä angiotensiini II -antagonistien että hydroklooritiatsidin verenpainetta alentavaa vaikutusta. Siksi hoidon alussa on suositeltavaa tarkistaa munuaisten toiminta ja potilaan riittävä nesteytys.
Valsartaaniin liittyvät yhteisvaikutukset
Reniini-angiotensiini-aldosteronijärjestelmän (RAAS) kaksoisesto ARB: llä, ACEI: llä tai aliskireenilla
Kliinisistä tutkimuksista saadut tiedot ovat osoittaneet, että reniini-angiotensiini-aldosteronijärjestelmän (RAAS) kaksoissulku ACE: n estäjien, angiotensiini II -reseptorin salpaajien tai aliskireenin yhdistelmällä lisää haittavaikutusten esiintyvyyttä, kuten hypotensio, hyperkalemia ja vähentynyt munuaisten toiminta (mukaan lukien akuutti munuaisten vajaatoiminta) verrattuna yksittäisen RAAS -järjestelmään vaikuttavan aineen käyttöön (ks. kohdat 4.3, 4.4 ja 5.1).
Yhteiskäyttöä ei suositella
Kaliumia säästävät diureetit, kaliumlisät, kaliumia sisältävät ruokasuolan korvikkeet ja muut kaliumpitoisuutta nostavat aineet.
Jos valsartaanin ja kaliumpitoisuutta muuttavan lääkkeen yhdistelmän käyttö on välttämätöntä, on suositeltavaa seurata plasman kaliumpitoisuuksia.
Kuljettimet
Tiedot in vitro osoittavat, että valsartaani on maksan sisäänottokuljettajien OATP1B1 / OATP1B3 ja maksan ulosvirtauskuljettajan MRP2 substraatti. Tämän havainnon kliinistä merkitystä ei tunneta. Takaisinoton kuljettajan estäjien (esim. Rifampisiini, syklosporiini) tai ulosvirtauskuljettajan (esim. Ritonaviiri) samanaikainen käyttö voi lisätä systeemistä valsartaanialtistusta. Erityistä varovaisuutta on noudatettava aloitettaessa tai lopetettaessa samanaikainen hoito näillä lääkkeillä.
Ei vuorovaikutusta
Valsartaania koskevissa yhteisvaikutustutkimuksissa ei havaittu kliinisesti merkityksellisiä yhteisvaikutuksia valsartaanin tai minkään seuraavien lääkevalmisteiden kanssa: simetidiini, varfariini, furosemidi, digoksiini, atenololi, indometasiini, hydroklooritiatsidi, amlodipiini, glibenklamidi. Digoksiini ja indometasiini voivat olla vuorovaikutuksessa Combisartaanin hydroklooritiatsidikomponentin kanssa (ks. Hydroklooritiatsidiin liittyvät yhteisvaikutukset).
Hydroklooritiatsidiin liittyvät yhteisvaikutukset
Samanaikainen käyttö vaatii varovaisuutta
Seerumin kaliumpitoisuuteen vaikuttavat lääkkeet.
Hydroklooritiatsidin hypokaleminen vaikutus voi lisääntyä, jos sitä käytetään samanaikaisesti kaliureettisten diureettien, kortikosteroidien, laksatiivien, ACTH: n, amfoterisiinin, karbenoksolonin, penisilliini G: n, salisyylihapon ja sen johdannaisten kanssa.
Jos näitä lääkkeitä määrätään valsartaani-hydroklooritiatsidiyhdistelmän kanssa, plasman kaliumpitoisuuden seurantaa suositellaan (ks. Kohta 4.4).
Lääkkeet, jotka voivat aiheuttaa kääntyvien kärkien takykardiaa
Hypokalemian riskin vuoksi hydroklooritiatsidia on annettava varoen, kun sitä käytetään yhdessä sellaisten lääkevalmisteiden kanssa, jotka voivat aiheuttaa kääntyvien kärkien takykardiaa, erityisesti luokan Ia ja luokan III rytmihäiriölääkkeiden ja joidenkin psykoosilääkkeiden kanssa.
Seerumin natriumpitoisuuteen vaikuttavat lääkkeet
Diureettien hyponatremista vaikutusta voi tehostaa antamalla samanaikaisesti tiettyjä lääkkeitä, kuten masennuslääkkeitä, psykoosilääkkeitä, epilepsialääkkeitä jne. Näiden lääkkeiden pitkäaikaisessa käytössä on noudatettava varovaisuutta.
Digitalis -glykosidit
Tiatsidien aiheuttama hypokalemia tai hypomagnesemia voi ilmetä haittavaikutuksina, mikä suosii digitalis-indusoitujen sydämen rytmihäiriöiden ilmaantumista (ks. Kohta 4.4).
Kalsiumin ja D -vitamiinin suolat
Tiatsididiureettien, mukaan lukien hydroklooritiatsidi, antaminen D -vitamiinin tai kalsiumsuolojen kanssa voi voimistaa seerumin kalsiumpitoisuuden nousua. Tiatsididiureettien ja kalsiumsuolojen samanaikainen käyttö voi aiheuttaa hyperkalsemiaa potilailla, jotka ovat alttiita hyperkalsemialle (esim. Hyperparatyreoosi, kasvaimet tai D -vitamiinin välittämät tilat) lisäämällä kalsiumin tubulaarista imeytymistä.
Diabeteslääkkeet (insuliini ja suun kautta otettavat diabeteslääkkeet)
Tiatsididiureetit voivat heikentää glukoosinsietoa. Diabeteslääkkeiden annosta on ehkä muutettava.
Metformiinia tulee käyttää varoen, koska hydroklooritiatsidiin liittyvä mahdollinen munuaisten vajaatoiminta aiheuttaa maitohappoasidoosin riskin.
Beetasalpaajat ja diatsoksidi
Tiatsididiureettien, mukaan lukien hydroklooritiatsidi, ja beetasalpaajien samanaikainen käyttö voi lisätä hyperglykemian riskiä. Tiatsididiureetit, mukaan lukien hydroklooritiatsidi, voivat tehostaa diatsoksidin hyperglykeemistä vaikutusta.
Lääkkeet, joita käytetään kihdin hoitoon (probenesidi, sulfinpyratsoni ja allopurinoli)
Urikosuristen lääkevalmisteiden annosta on ehkä muutettava, koska hydroklooritiatsidi voi nostaa seerumin virtsahappopitoisuutta. Probenesidin tai sulfinpyratsonin annosta voidaan joutua suurentamaan. Tiatsididiureettien, mukaan lukien hydroklooritiatsidi, samanaikainen käyttö voi lisätä annosta. allopurinolille.
Antikolinergit ja muut mahalaukun liikkuvuuteen vaikuttavat lääkkeet
Antikolinergiset lääkkeet (esim. Atropiini, biperideeni) voivat lisätä tiatsidityyppisten diureettien hyötyosuutta, mikä johtuu ilmeisesti ruoansulatuskanavan liikkuvuuden ja mahalaukun tyhjenemisnopeuden vähenemisestä.Sitä vastoin oletetaan, että prokineettiset lääkkeet, kuten sisapridi, voivat vähentää tiatsididiureettien hyötyosuutta.
Amantadina
Tiatsidit, mukaan lukien hydroklooritiatsidi, voivat lisätä amantadiinin aiheuttamien haittavaikutusten riskiä.
Ioninvaihtohartsit
Kolestyramiini tai kolestipoli heikentää tiatsididiureettien, mukaan lukien hydroklooritiatsidi, imeytymistä. Tämä voi johtaa tiatsididiureettien subterapeuttisiin vaikutuksiin. Kuitenkin jakamalla hydroklooritiatsidin ja hartsin annos siten, että hydroklooritiatsidi annetaan vähintään 4 tuntia ennen tai 4-6 tuntia hartsien antamisen jälkeen, vuorovaikutus voidaan mahdollisesti minimoida.
Sytotoksiset aineet
Tiatsidit, mukaan lukien hydroklooritiatsidi, voivat vähentää sytotoksisten lääkkeiden (esim. Syklofosfamidi, metotreksaatti) erittymistä munuaisten kautta ja parantaa niiden myelosuppressiivisia vaikutuksia.
Ei-depolarisoivat luurankolihakset (esim. tubokurariini)
Tiatsidit, mukaan lukien hydroklooritiatsidi, tehostavat luustolihasrelaksanttien, kuten kurareijohdannaisten, toimintaa.
Syklosporiini
Siklosporiinin samanaikainen käyttö voi lisätä hyperurikemian ja kihti-tyyppisten komplikaatioiden riskiä.
Alkoholi, barbituraatit ja huumeet
Tiatsididiureettien samanaikainen käyttö muiden aineiden kanssa, joilla on myös verenpainetta alentava vaikutus (esim. Aineet, jotka vähentävät sympaattista keskushermoston toimintaa tai joilla on suora verisuonia laajentava vaikutus), voi voimistaa ortostaattista hypotensiota.
Metyylidopa
Metyylidopan ja hydroklooritiatsidin samanaikaisen käytön yhteydessä on raportoitu yksittäisiä hemolyyttistä anemiaa.
Jodiväriaine
Diureettien aiheuttaman dehydraation tapauksessa akuutin munuaisten vajaatoiminnan riski kasvaa erityisesti suurilla jodituotteiden annoksilla. Potilaat on nesteytettävä ennen antoa.
04.6 Raskaus ja imetys -
Raskaus
Valsartaani
Angiotensiini II -reseptorin salpaajien (AIIRA) käyttöä ei suositella raskauden ensimmäisen kolmanneksen aikana (ks. Kohta 4.4). AIIRA -lääkkeiden käyttö on vasta -aiheista raskauden toisen ja kolmannen kolmanneksen aikana (ks. Kohdat 4.3 ja 4.4).
Epidemiologiset todisteet teratogeenisuuden riskistä ACE: n estäjille altistumisen jälkeen raskauden ensimmäisen kolmanneksen aikana eivät ole olleet vakuuttavia; pientä riskin kasvua ei kuitenkaan voida sulkea pois. Vaikka kontrolloituja epidemiologisia tietoja angiotensiini II -reseptorin salpaajien (AIIRA) käyttöön liittyvistä riskeistä ei ole saatavilla, samanlainen riski voi esiintyä myös tämän lääkeryhmän osalta. raskauden aikana, ellei AIIRA -hoidon jatkamista pidetä välttämättömänä. Kun raskaus todetaan, AIIRA -hoito on lopetettava välittömästi ja tarvittaessa aloitettava vaihtoehtoinen hoito.
Altistuksen AIIRA -lääkkeille toisen ja kolmannen raskauskolmanneksen aikana tiedetään aiheuttavan sikiötoksisuutta (heikentynyt munuaisten toiminta, oligohydramnioni, kallon luutumisen hidastuminen) ja vastasyntyneen toksisuutta (munuaisten vajaatoiminta, hypotensio, hyperkalemia) ihmisillä (ks. Myös kohta 5.3).
Jos altistuminen AIIRA -lääkkeille on tapahtunut raskauden toisesta kolmanneksesta lähtien, suositellaan munuaisten toiminnan ja kallon ultraäänitutkimusta.
Vastasyntyneitä, joiden äidit ovat ottaneet AIIRA -lääkkeitä, on seurattava tarkoin hypotension varalta (ks. Kohdat 4.3 ja 4.4).
Hydroklooritiatsidi
Kokemus hydroklooritiatsidin käytöstä raskauden aikana, erityisesti ensimmäisen kolmanneksen aikana, on rajallinen. Eläinkokeet eivät ole riittäviä. Hydroklooritiatsidi läpäisee istukan. Hydroklooritiatsidin farmakologisen vaikutusmekanismin perusteella sen käyttö raskauden toisen ja kolmannen kolmanneksen aikana voi heikentää sikiön ja istukan perfuusiota ja aiheuttaa sikiö- ja vastasyntyneen vaikutuksia, kuten keltaisuutta, elektrolyyttihäiriöitä ja trombosytopeniaa.
Ruokinta-aika
Valsartaanin käytöstä imetyksen aikana ei ole tietoja. Hydroklooritiatsidi erittyy äidinmaitoon, joten Combisartan Krka -valmisteen käyttöä imetyksen aikana ei suositella. Vaihtoehtoisia hoitoja, joiden turvallisuusprofiili on osoittautunut suositeltaviksi käytettäväksi imetyksen aikana, etenkin jos imetät vastasyntyneitä ja imeväisiä.
04.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn -
Tutkimuksia Combisartanin vaikutuksesta ajokykyyn ja koneiden käyttökykyyn ei ole tehty. Ajettaessa tai käytettäessä koneita on otettava huomioon ajoittain esiintyvä huimaus tai väsymys.
04.8 Haittavaikutukset -
Kliinisissä tutkimuksissa raportoidut haittavaikutukset ja laboratoriotulokset, joita esiintyi useammin valsartaanin ja hydroklooritiatsidin kuin lumelääkkeen yhteydessä, ja yksittäiset raportit markkinoille tulon jälkeen on esitetty elinjärjestelmäluokittain. Haittavaikutuksia, jotka tiedetään kullekin yksittäiselle aineosalle yksin, mutta joita ei ole havaittu kliinisissä tutkimuksissa, voi esiintyä myös valsartaani / hydroklooritiatsidihoidon aikana.
Haittavaikutukset on luokiteltu esiintymistiheyden mukaan, alkaen yleisimmistä, käyttämällä seuraavaa käytäntöä: hyvin yleinen (≥1 / 10); yleinen (≥ 1/100,
Haittavaikutukset ilmoitetaan kussakin yleisyysluokassa vakavuuden mukaan alenevassa järjestyksessä.
Taulukko 1. Valsartaanin / hydroklooritiatsidin haittavaikutusten esiintymistiheys
Lisätietoja yksittäisistä komponenteista
Jokaisesta yksittäisestä aineosasta jo raportoidut haittavaikutukset voivat myös olla Combisartanin mahdollisia haittavaikutuksia, vaikka niitä ei havaittu kliinisissä tutkimuksissa tai markkinoille tulon jälkeen.
Taulukko 2. Valsartaanin haittavaikutusten esiintymistiheys
Taulukko 3. Hydroklooritiatsidin haittavaikutusten esiintymistiheys
Hydroklooritiatsidia on määrätty laajalti monien vuosien ajan, usein suuremmilla annoksilla kuin Combisartanin kanssa annetut annokset Seuraavia haittavaikutuksia on raportoitu potilailla, joita on hoidettu monoterapiana tiatsididiureetteilla, mukaan lukien hydroklooritiatsidi.
04.9 Yliannostus -
Oireet
Valsartaanin yliannostus voi johtaa huomattavaan hypotensioon, joka voi johtaa tajunnan laskuun, verenkierron romahtamiseen ja / tai sokkiin. Hydroklooritiatsidin yliannostuksen jälkeen voi ilmetä myös seuraavia oireita: pahoinvointi, uneliaisuus, hypovolemia, elektrolyyttihäiriöt, jotka liittyvät sydämen rytmihäiriöihin ja lihaskouristuksiin.
Hoito
Terapeuttiset toimenpiteet riippuvat nielemisajasta ja oireiden tyypistä ja vakavuudesta ja antavat etusijalle verenkierron normalisoitumisen.
Jos hypotensio ilmenee, potilas on asetettava selällään ja suolaliuos on annettava nopeasti.
Valsartaania ei voida poistaa hemodialyysillä, koska se sitoutuu voimakkaasti plasman proteiineihin, kun taas hydroklooritiatsidi voidaan poistaa dialyysillä.
05.0 FARMAKOLOGISET OMINAISUUDET -
05,1 "Farmakodynaamiset ominaisuudet -
Farmakoterapeuttinen ryhmä: Angiotensiini II -antagonistit yhdessä diureettien, valsartaanin ja diureettien kanssa ATC -koodi: C09D A03.
Valsartaani / hydroklooritiatsidi
Kaksoissokkoutetussa, satunnaistetussa, aktiivisesti kontrolloidussa tutkimuksessa potilailla, joiden hoitotasapaino oli riittämätön 12,5 mg: lla hydroklooritiatsidia, todettiin merkittävästi suurempaa systolisen / diastolisen verenpaineen laskua valsartaani / hydroklooritiatsidi 160 / 12,5 mg -yhdistelmällä (12,4 / 7,5 mmHg) verrattuna hydroklooritiatsidille 25 mg (5,6 / 2,1 mmHg). Lisäksi merkittävästi suurempi osa potilaista vastasi (verenpaine
Kaksoissokkoutetussa, satunnaistetussa, aktiivisesti kontrolloidussa tutkimuksessa potilailla, joiden hoitotasapaino oli riittämätön 160 mg valsartaanilla, todettiin merkittävästi suurempaa systolisen / diastolisen verenpaineen laskua 160/25 mg (14,6 / 11,9 mmHg) -valsartaani / hydroklooritiatsidi-yhdistelmällä ja valsartaani / hydroklooritiatsidi 160 / 12,5 mg (12,4 / 10,4 mmHg) verrattuna valsartaaniin 160 mg (8,7 / 8,8 mmHg).
Ero verenpaineen alenemisessa 160/25 mg: n ja 160 / 12,5 mg: n annosten välillä saavutti myös tilastollisen merkityksen. Lisäksi merkittävästi suurempi prosenttiosuus potilaista vastasi (diastolinen verenpaine
Monitekijäisessä, satunnaistetussa, kaksoissokkotutkimuksessa, jossa verrattiin valsartaani / hydroklooritiatsidiyhdistelmien eri annoksia verrattuna vastaaviin komponentteihin, havaittiin huomattavasti suurempi systolisen / diastolisen verenpaineen lasku valsartaani / hydroklooritiatsidi-yhdistelmällä 160 / 12,5 mg (17,8 / 13,5 mmHg) ) ja 160/25 mg (22,5 / 15,3 mmHg) verrattuna lumelääkkeeseen (1,9 / 4,1 mmHg) ja vastaaviin monoterapioihinsa, esim. hydroklooritiatsidiin 12,5 mg (7,3 / 7,2 mmHg), hydroklooritiatsidiin 25 mg (12,7 / 9,3 mmHg) ja valsartnaan 160 mg ( 12,1 / 9,4 mmHg) Lisäksi merkittävästi suurempi osa potilaista vastasi (diastolinen paine
Kontrolloiduissa kliinisissä tutkimuksissa, joissa käytettiin valsartaania + hydroklooritiatsidia, seerumin kaliumpitoisuus pieneni annoksesta riippuen. Seerumin kaliumpitoisuuden lasku tapahtui useammin potilailla, jotka saivat 25 mg hydroklooritiatsidia kuin potilailla, jotka saivat 12,5 mg. Valsartaanin / hydroklooritiatsidin kontrolloiduissa kliinisissä tutkimuksissa hydroklooritiatsidin kaliumia alentavaa vaikutusta heikensi valsartaanin kaliumia säästävä vaikutus.
Valsartaanin ja hydroklooritiatsidin yhdistelmän hyödyllisiä vaikutuksia sydän- ja verisuonikuolleisuuteen ja sairastuvuuteen ei tällä hetkellä tunneta.
Epidemiologiset tutkimukset ovat osoittaneet, että pitkäaikainen hydroklooritiatsidihoito vähentää sydän- ja verisuonitautikuolleisuuden ja sairastuvuuden riskiä.
Valsartaani
Valsartaani on suun kautta aktiivinen spesifinen angiotensiini II (Ang II) -reseptoriantagonisti, joka vaikuttaa selektiivisesti AT1 -reseptorin alatyyppiin ja on vastuussa angiotensiini II: n tunnetuista vaikutuksista. Plasman Ang II -tasojen nousu valsartaanin aiheuttaman AT1 -reseptorien estämisen seurauksena voi stimuloida vapautettuja AT2 -reseptoreita, mikä näyttää tasapainottavan AT1 -reseptorien toimintaa. Valsartaanilla ei ole osittaista agonistiaktiivisuutta AT1-reseptorissa, ja sillä on paljon suurempi (noin 20 000-kertainen) affiniteetti AT1-reseptoriin kuin AT2-reseptoriin. Valsartaani ei sitoudu muihin hormonireseptoreihin tai ionikanaviin, jotka tunnetaan niiden merkityksestä sydän- ja verisuonijärjestelmän säätelyssä.
Valsartaani ei estä ACE: tä, joka tunnetaan myös nimellä kininaasi II, joka muuttaa Ang I: n Ang II: ksi ja hajottaa bradykiniiniä. Koska ACG: hen tai bradykiniinin tai aineen P vaikutuksiin ei ole vaikutusta, angiotensiini II -reseptorin salpaajiin ei todennäköisesti liity yskää. Kliinisissä tutkimuksissa, joissa valsartaania verrattiin ACE: n estäjään, kuivan yskän ilmaantuvuus oli merkittävä (P.
Valsartaanin anto valtimoverenpainetautia sairastaville potilaille alentaa verenpainetta vaikuttamatta sykkeeseen.
Useimmilla potilailla verenpainetta alentava vaikutus alkaa 2 tunnin kuluessa yhden suun kautta otetun annoksen antamisen jälkeen ja verenpaineen lasku saavutetaan 4-6 tunnin kuluessa. Verenpainetta alentava vaikutus säilyy yli 24 tuntia annostelun jälkeen. Toistuvalla annostelulla, mikä tahansa annos, suurin verenpaineen lasku saavutetaan yleensä 2-4 viikon kuluessa ja se säilyy pitkäaikaisen hoidon aikana. saadaan liittämällä lääke hydroklooritiatsidiin.
Valsartaanin äkillinen lopettaminen ei liittynyt rebound -verenpaineeseen tai muihin haittavaikutuksiin.
Hypertensiivisillä potilailla, joilla on tyypin 2 diabetes ja mikroalbuminuria, valsartaanin on osoitettu vähentävän virtsan albumiinin erittymistä. vs. amlodipiini (5-10 mg / od) 332 tyypin 2 diabetesta sairastavalla potilaalla (keski-ikä: 58 vuotta; 265 miestä), joilla on mikroalbuminuria (valsartaani: 58 mcg / min; amlodipiini: 55,4 mcg / min), normaali tai kohonnut verenpaine ja ehjä munuaisten toiminta (kreatiniini
Diovan Reduction of Proteinuria (DROP) -tutkimuksessa arvioitiin edelleen valsartaanin tehoa albumiinin erittymisen vähentämisessä virtsaan 391 hypertensiopotilaalla (BP = 150/88 mmHg), joilla oli tyypin 2 diabetes, albuminuria (keskiarvo = 102 mcg / min; 20) -700 mcg / min) ja ehjä munuaisten toiminta (keskimääräinen seerumin kreatiniini = 80 mcmol / l). Potilaat satunnaistettiin saamaan yksi kolmesta eri annoksesta valsartaania (160, 320 ja 640 mg / vrk) ja heitä hoidettiin 30 viikon ajan. Tämän tutkimuksen tarkoituksena oli määrittää optimaalinen valsartaaniannos Yhdistyneiden arabiemiirikuntien vähentämiseksi tyypin 2 diabetesta sairastavilla hypertensiivisillä potilailla. 30 viikon kuluttua Yhdistyneiden arabiemiirikuntien prosentuaalinen muutos pieneni merkittävästi, 36% lähtötilanteesta. Valsartaanilla 160 mg (95%: n luottamusväli) : 22--47%) ja 44% valsartaanilla 320 mg (95%: n luottamusväli: 31--54%). Todettiin, että 160-320 mg valsartaania vähensi kliinisesti merkittävästi Yhdistyneitä arabiemiirikuntia tyypin 2 diabetesta sairastavilla hypertensiivisillä potilailla.
Muu: reniini-angiotensiini-aldosteronijärjestelmän kaksoissulku
Kahdessa suuressa satunnaistetussa kontrolloidussa tutkimuksessa (ONTARGET (ONgoing Telmisartan Alone ja yhdessä Ramipril Global Endpoint Trial) ja VA Nephron-D (The Veterans Affairs Nephropathy in Diabetes)) on tutkittu ACE: n estäjän ja antagonistin yhdistelmän käyttöä. angiotensiini II -reseptori.
ONTARGET oli tutkimus, joka tehtiin potilailla, joilla on ollut sydän- tai aivoverisuonisairaus tai tyypin 2 diabetes, johon liittyy todisteita elinvaurioista.VA NEPHRON-D oli tutkimus, joka tehtiin potilailla, joilla oli tyypin 2 diabetes ja diabeettinen nefropatia.
Nämä tutkimukset eivät osoittaneet merkittävää myönteistä vaikutusta munuaisten ja / tai kardiovaskulaarisiin tuloksiin ja kuolleisuuteen, kun taas hyperkalemian, akuutin munuaisvaurion ja / tai hypotension riskiä havaittiin monoterapiaan verrattuna.
Nämä tulokset ovat merkityksellisiä myös muille ACE: n estäjille ja angiotensiini II -reseptorin salpaajille, kun otetaan huomioon niiden samanlaiset farmakodynaamiset ominaisuudet.
Siksi ACE: n estäjiä ja angiotensiini II -reseptorin salpaajia ei tule käyttää samanaikaisesti potilailla, joilla on diabeettinen nefropatia.
ALTITUDE (Aliskiren -tutkimus tyypin 2 diabeteksessa käyttäen sydän- ja verisuonitautien ja munuaissairauksien päätetapahtumia) oli tutkimus, jonka tarkoituksena oli tarkistaa etu, joka liittyy aliskireenin lisäämiseen ACE -estäjän tai angiotensiini II -reseptorin antagonistin vakiohoitoon potilailla, joilla on diabetes mellitus. Tyyppi 2 ja krooninen munuaissairaus , sydän- tai verisuonitauti tai molemmat. hyperkalemiaa, hypotensiota ja munuaisten vajaatoimintaa) raportoitiin useammin aliskireeniryhmässä kuin lumelääkeryhmässä.
Hydroklooritiatsidi
Tiatsididiureettien vaikutuspaikka on pääasiassa munuaisten distaalisessa kierteisessä putkessa, ja suuren affiniteetin reseptorin läsnäolo munuaiskuoressa on osoitettu olevan ensisijainen sitoutumiskohta tiatsididiureettien vaikutukselle ja kuljetuksen estämiselle. tiatsidien vaikutusmekanismi tapahtuu estämällä Na + Cl- kuljetusta, mahdollisesti kilpailemalla Cl-sivuston kanssa, mikä vaikuttaa elektrolyyttien reabsorptiomekanismiin: lisäämällä suoraan "erittymistä" natriumia ja klooria vastaavina määrinä ja vähentävät epäsuorasti plasman tilavuutta tällä diureettisella vaikutuksella, mistä seuraa plasman reniiniaktiivisuuden lisääntyminen, aldosteronin eritys ja virtsakaliumin menetys ja seerumin kaliumin lasku. Rengiini-aldosteronisidos on angiotensiini II: n välityksellä, joten seerumin kaliumpitoisuuden lasku on vähemmän selvää, kun samanaikaisesti annetaan valsartaania, se on pienempi kuin hydroklooritiatsidi-monoterapian yhteydessä.
05,2 "Farmakokineettiset ominaisuudet -
Valsartaani / hydroklooritiatsidi
Hydroklooritiatsidin systeeminen saatavuus vähenee noin 30%, kun sitä annetaan samanaikaisesti valsartaanin kanssa. Yhteiskäyttö hydroklooritiatsidin kanssa ei vaikuta merkittävästi valsartaanin kinetiikkaan. Havaittu yhteisvaikutus ei vaikuta valsartaanin ja hydroklooritiatsidin käyttöön. Koska kontrolloidut kliiniset tutkimukset ovat osoittaneet selkeän verenpainetta alentavan vaikutuksen, joka on parempi kuin kahdella erikseen annetulla vaikuttavalla aineella tai lumelääkkeellä.
Valsartaani
Imeytyminen
Pelkästään oraalisen annon jälkeen valsartaanin huippupitoisuudet saavutetaan 2-4 tunnin kuluttua. Sen keskimääräinen absoluuttinen hyötyosuus on 23%. Ruoka vähentää valsartaanialtistusta (mitattuna AUC -arvolla, plasmakonsentraatiokäyrän alla) noin 40% ja huippupitoisuus plasmassa (Cmax) noin 50%, vaikka noin 8 tuntia plasman valsartaanipitoisuuksien antamisen jälkeen sekä paastotussa että ei-paastoavassa kohteessa. AUC -arvon pienenemiseen ei kuitenkaan liity kliinisesti merkittävää terapeuttisen vaikutuksen heikkenemistä, joten valsartaani voidaan ottaa ruoan kanssa tai ilman.
Jakelu
Valsartaanin vakaan tilan jakautumistilavuus laskimonsisäisen annon jälkeen on noin 17 litraa, mikä osoittaa, että valsartaani ei jakaudu laajasti kudoksiin. Valsartaani sitoutuu voimakkaasti (94--97%) seerumin proteiineihin, pääasiassa seerumin albumiiniin.
Biotransformaatio
Valsartaani ei muutu suuressa määrin biotransformaatiossa, koska vain noin 20% annoksesta erittyy metaboliitteina. Plasmassa on havaittu pieniä hydroksyloidun metaboliitin pitoisuuksia (alle 10% valsartaanin AUC -arvosta), joka on farmakologisesti inaktiivinen.
Eliminaatio
Valsartaanilla on monieksponentiaalinen hajoamisen kinetiikka (t½α ulosteet (noin 83% annoksesta) ja virtsa (noin 13% annoksesta), pääasiassa muuttumattomana lääkkeenä. Laskimonsisäisen annon jälkeen plasman puhdistuma on noin 2 l / h. Munuaispuhdistuma on 0,62 l / h (noin 30% plasman kokonaispuhdistumasta) Valsartaanin eliminaation puoliintumisaika on 6 tuntia.
Hydroklooritiatsidi
Imeytyminen
Suun kautta annettuna hydroklooritiatsidi imeytyy nopeasti (tmax = noin 2 tuntia) Terapeuttisella alueella keskimääräinen AUC -nousu on lineaarinen ja suhteessa annokseen.
Ruoan vaikutuksella hydroklooritiatsidin imeytymiseen, jos sitä esiintyy, on vain vähän kliinistä merkitystä: hydroklooritiatsidin absoluuttinen hyötyosuus suun kautta annettuna on 70%.
Jakelu
Näennäinen jakautumistilavuus on 4-8 l / kg. Kiertävä hydroklooritiatsidi sitoutuu seerumin proteiineihin (40-70%), pääasiassa seerumin albumiiniin. Hydroklooritiatsidia kertyy myös punasoluihin noin kolme kertaa suurempia määriä kuin plasmassa.
Eliminaatio
Hydroklooritiatsidi eliminoituu pääasiassa muuntamattomana yhdisteenä. Eliminaation loppuvaiheessa hydroklooritiatsidi eliminoituu plasmasta, ja sen keskimääräinen puoliintumisaika on 6-15 tuntia. Yli 95% hydroklooritiatsidin imeytyneestä annoksesta erittyy muuttumattomana yhdisteenä virtsaan. Munuaispuhdistuma koostuu passiivisesta suodatuksesta ja aktiivisesta erittymisestä munuaistiehyessä.
Erityisryhmät
Eläkeläiset
Joillakin iäkkäillä potilailla havaittiin hieman suurempi systeeminen valsartaanialtistus kuin nuorilla, mutta tällä ei kuitenkaan ole osoitettu olevan kliinistä merkitystä.
Rajoitetut tiedot viittaavat siihen, että hydroklooritiatsidin systeeminen puhdistuma on pienentynyt sekä terveillä että hypertensiivisillä vanhuksilla verrattuna nuoriin terveisiin vapaaehtoisiin.
Munuaisten vajaatoiminta
Suositelluilla Combisartan -annoksilla annosta ei tarvitse muuttaa potilailla, joiden glomerulusten suodatusnopeus on 30-70 ml / min. Kombisartaanin antamisesta potilaille, joilla on vaikea munuaisten vajaatoiminta (glomerulusten suodatusnopeutta ja plasman proteiineja ei poisteta dialyysillä, ei ole tietoa, kun taas hydroklooritiatsidi voidaan poistaa dialyysillä, ei ole tietoja.
Munuaisten vajaatoiminnan yhteydessä hydroklooritiatsidin keskimääräiset huippupitoisuudet ja AUC-arvot nousevat ja virtsan eliminaationopeus pienenee.AUC-arvon 3-kertainen nousu havaittiin lievää tai kohtalaista munuaisten vajaatoimintaa sairastavilla potilailla. Vaikeaa munuaisten vajaatoimintaa sairastavilla potilailla on havaittu AUC: n 8-kertainen nousu Hydroklooritiatsidi on vasta-aiheinen potilaille, joilla on vaikea munuaisten vajaatoiminta (ks. Kohta 4.3).
Maksan vajaatoiminta
Farmakokineettisessä tutkimuksessa, joka tehtiin potilailla, joilla oli lievä (n = 6) tai kohtalainen (n = 5) maksan vajaatoiminta, valsartaanialtistus kasvoi noin kaksinkertaiseksi verrattuna terveisiin vapaaehtoisiin (ks. Kohdat 4.2 ja 4.4). potilailla, joilla on vaikea maksan vajaatoiminta (ks. kohta 4.3). Maksasairaus ei vaikuta merkittävästi hydroklooritiatsidin farmakokinetiikkaan.
05.3 Prekliiniset tiedot turvallisuudesta -
Suun kautta annetun valsartaanin / hydroklooritiatsidin yhdistelmän mahdollista toksisuutta tutkittiin rotilla ja apinoilla (marmoset) enintään 6 kuukautta kestäneissä tutkimuksissa.
Kroonisen toksisuuden tutkimuksissa assosiaatiosta johtuvat muutokset johtuivat todennäköisimmin valsartaanista.Toksikologisesti kohde-elin oli munuainen, jonka reaktio oli apinoilla paljon voimakkaampi kuin rotalla. Yhdistelmä aiheutti munuaisvaurioita (nefropatia ja tubulaarinen basofilia, plasman urean, plasman kreatiniinin ja seerumin kaliumpitoisuuden suureneminen, virtsan määrän ja virtsa -elektrolyyttien nousu 30 mg / kg / vrk valsartaania + 9 mg / kg / vrk hydroklooritiatsidia rotilla) ja 10 + 3 mg / kg / vrk apinoilla), todennäköisesti munuaisten hemodynamiikan muutoksen vuoksi. Nämä annokset rotilla ovat 0,9 ja 3,5 kertaa suurin suositeltu ihmisannos (MRHD) valsartaanille ja hydroklooritiatsidille mg / m². Apinoilla nämä annokset ovat 0,3 ja 1,2 kertaa enimmäisannos. valsartaania ja hydroklooritiatsidia (mg / m²) (laskelmissa oletetaan, että suun kautta annettava valsartaaniannos on 320 mg / vrk yhdessä 25 mg / vrk hydroklooritiatsidia ja 60 kg painavan potilaan kanssa).
Suuret annokset valsartaanin / hydroklooritiatsidin yhdistelmää aiheuttivat punasolujen indeksien (erytrosyyttimäärä, hemoglobiini, hematokriitti) vähenemisen 100 + 31 mg / kg / vrk rotalla ja 30 + 9 mg / kg / vrk apinalla. rotilla 3,0 ja 12 kertaa suurin suositeltu ihmisen valsartaaniannos (MRHD) ja hydroklooritiatsidi (mg / m²). Apinoilla nämä annokset ovat 0,9 ja 3,5 kertaa suurin suositeltu ihmisannos (MRHD) valsartaanille ja hydroklooritiatsidille mg / m² (laskelmissa oletetaan, että suun kautta otettava valsartaaniannos on 320 mg / vrk yhdessä 25 mg / vrk hydroklooritiatsidin ja 60 kg painava potilas).
Apinoilla havaittiin mahalaukun limakalvon vaurioita (30 + 9 mg / kg / vrk). Yhdistelmä johti myös afferenttisten valtimoiden hyperplasiaan munuaisissa (600 + 188 mg / kg / vrk rotalla ja 30 + 9 mg / kg / vrk apinalla). Nämä apinan annokset edustavat 0,9 ja 3 .5 kertaa valsartaanin ja hydroklooritiatsidin suositeltu ihmisen enimmäisannos (MRHD) mg / m². Rotilla nämä annokset edustavat 18 ja 73 kertaa ihmisen suositeltua valsartaaniannosta (MRHD) ja hydroklooritiatsidia (mg / m²) (laskelmissa oletetaan, että suun kautta otettava valsartaaniannos on 320 mg / vrk yhdessä 25 mg / vrk hydroklooritiatsidin kanssa) ja 60 kg painava potilas).
Edellä mainitut vaikutukset näyttävät johtuvan suurten valsartaaniannosten farmakologisesta vaikutuksesta (angiotensiini II: n aiheuttaman reniinin vapautumisen esto, reniiniä tuottavien solujen stimulaatio) ja ilmenevät myös ACE: n estäjien kanssa. valsartaaniannoksia ihmisillä.
Valsartaanin ja hydroklooritiatsidin yhdistelmän mutageenisuutta, kromosomaalista hajoamista tai karsinogeenisuutta ei ole testattu, koska näiden kahden aineen välillä ei ole todettu yhteisvaikutuksia.Nämä testit kuitenkin suoritettiin erikseen valsartaanin ja hydroklooritiatsidin kanssa, eivätkä ne osoittaneet mutageenisuutta, kromosomaalista hajoamista tai karsinogeenisuutta.
Rotille emolle toksiset valsartaaniannokset (600 mg / kg / vrk) raskauden viimeisinä päivinä ja imetyksen aikana johtivat eloonjäämisasteen pienenemiseen, painonnousun heikkenemiseen ja kehityksen hidastumiseen (ruston irtoaminen) ja korvakäytävän avautumiseen. Nämä annokset rotilla (600 mg / kg / vrk) ovat noin 18 kertaa suurin suositeltu ihmisannos (mg / m²) (laskelmissa oletetaan, että oraalinen annos on 320 mg / vrk potilaalle, joka painaa 60 kg). .
Samanlaisia tuloksia havaittiin valsartaanilla / hydroklooritiatsidilla rotilla ja kaneilla. Rotilla ja kaneilla tehdyissä alkio-sikiön kehitystutkimuksissa (segmentti II) valsartaani / hydroklooritiatsidilla ei todettu teratogeenisuutta, mutta emolle toksisuuteen liittyvää sikiötoksisuutta havaittiin.
06.0 FARMASEUTTISET TIEDOT -
06.1 Apuaineet -
Tabletin ydin:
Mikrokiteinen selluloosa,
Vedetön kolloidinen piidioksidi,
Krospovidoni,
Magnesiumstearaatti
Pinnoite:
Hypromelloosi,
Makrogoli 8000,
Talkki,
Punainen rautaoksidi (E 172),
Titaanidioksidi (E 171).
06.2 Yhteensopimattomuus "-
Ei oleellinen.
06.3 Voimassaoloaika "-
3 vuotta
06.4 Säilytystä koskevat erityiset varotoimet -
Säilytä enintään 30 ° C: n lämpötilassa.
Säilytä alkuperäispakkauksessa.Herkkä kosteudelle.
06.5 Välipakkauksen luonne ja pakkauksen sisältö -
PVC / PE / PVDC / Al- tai PVC / PVDC / Al -läpipainopakkaukset
14, 28, 56, 98, kalenteripakkauksissa, 280 kalvopäällysteistä tablettia
Jaettavat yksikköannospakkaukset PVC / PE / PVDC / Al tai PVC / PVDC / Al
56x1, 98x1, 280x1 kalvopäällysteiset tabletit.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
06.6 Käyttö- ja käsittelyohjeet -
Ei erityisiä ohjeita.
07.0 "MYYNTILUVAN HALTIJA" -
A.Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi, 3 - Firenze
08.0 MYYNTILUVAN NUMERO -
AIC n. 034134039-160 mg / 12,5 mg kalvopäällysteiset tabletit, 14 tablettia PVC / PE / PVDC / Al -läpipainopakkauksessa
AIC n. 034134041 - 160 mg / 12,5 mg kalvopäällysteiset tabletit, 28 tablettia läpipainopakkauksessa PVC / PE / PVDC / Al AIC n. 034134054 - 160 mg / 12,5 mg kalvopäällysteiset tabletit, 56 tablettia PVC / PE / PVDC / Al -läpipainopakkauksessa
AIC n. 034134066 - 160 mg / 12,5 mg kalvopäällysteiset tabletit, 98 tablettia PVC / PE / PVDC / Al -läpipainopakkauksessa
AIC n. 034134078-160 mg / 12,5 mg kalvopäällysteiset tabletit, 98x1 tablettia PVC / PE / PVDC / Al -läpipainopakkauksessa
AIC n. 034134080-160 mg / 12,5 mg kalvopäällysteiset tabletit, 280 (10x28) tablettia PVC / PE / PVDC / Al -läpipainopakkauksessa
AIC n. 034134092 - 160 mg / 12,5 mg kalvopäällysteiset tabletit, 280 (20x14) tablettia PVC / PE / PVDC / Al -läpipainopakkauksessa
09.0 MYYNTILUVAN MYYNTILUVAN TAI UUDISTAMISPÄIVÄMÄÄRÄ -
Myyntiluvan myöntämisen päivämäärä: 25. heinäkuuta 2004
Viimeisimmän uudistamisen päivämäärä: 29. toukokuuta 2010
10.0 TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ -
Kesäkuuta 2015